Серцева недостатність
Содержание
Визначення. Серцева недостатність (СН) — порушення структури та функції серця, що призводить до нездатності останнього забезпечувати кровообіг киснем та енергією відповідно до метаболічних потреб тканин організму.
СН, згідно з ЄТК, 2016, — це синдром, при якому пацієнти мають типові симптоми (задишка, набряки, втомлюваність) та ознаки (підвищення тиску в яремній вені, хрипи в легенях, периферичні набряки), викликані порушенням структури та/або функції серця, що призводить до зменшення серцевого викиду та/або підвищення внутрішньосерцевого викиду у спокої та при фізичному навантаженні. Перед тим як виникають клінічні симптоми СН, розвиваються структурні або функціональні зміни (систолічна чи діастолічна дисфункція) в міокарді (табл. 2.139).
Таблиця 2.139. Препарати, які спричиняють і посилюють СН (Наукове узгодження АНА, 2016)
|
Група препаратів |
Представники |
|
НПЗП |
|
|
Анестезіологічні препарати |
|
|
Препарати для лікування при ЦД |
|
|
ААП |
|
|
Антигіпертензивні препарати |
|
|
Протигрибкові препарати |
|
|
Протипухлинні препарати |
|
|
Гематологічні препарати |
|
|
Препарати, які застосовуються в пульмонології |
|
|
Ревматологічні препарати |
|
|
Урологічні препарати |
|
Поширеність СН у популяції становить від 2 до 3% і різко зростає з віком. Так, поширеність СН серед осіб віком 70–80 років коливається у межах 10–20%. 50% хворих помирають протягом 4 років від моменту виникнення захворювання; 40% пацієнтів, госпіталізованих із СН, помирають або повторно госпіталізуються протягом року.
Етіологія. Виділяють такі причини синдрому серцевої недостатності [11, 28, 49]:
І. Ураження серцевого м’яза (міокардіальна недостатність).
1. Первинні:
- міокардити, ДКМП.
2. Вторинні:
- гострий ІМ, хронічна ІХС;
- гіпо- та гіпертиреоз;
- ураження серця при системних захворюваннях сполучної тканини;
- токсико-алергічні ураження міокарда.
ІІ. Гемодинамічне перевантаження шлуночків серця.
1. Підвищення опору до вигнання крові (збільшення постнавантаження):
- системна АГ, легенева АГ; стеноз гирла аорти, стеноз легеневої артерії.
2. Збільшення наповнення камер серця (збільшення переднавантаження):
- регургітація мітрального клапана, регургітація аортального клапана, недостатність клапана легеневої артерії, регургітація тристулкового клапана;
- вроджені вади серця зі скидом крові зліва направо.
ІІІ. Порушення наповнення шлуночків серця.
1. Мітральний і трикуспідальний стеноз.
2. Ексудативний та констриктивний перикардит, тампонада серця.
3. Захворювання з підвищеною жорсткістю міокарда та діастолічною дисфункцією:
- ГКМП, амілоїдоз серця, фіброеластоз, ендоміокардіальний фіброз;
- виражена гіпертрофія міокарда (в тому числі при АГ, аортальному стенозі).
ІV. Підвищення метаболічної потреби тканин (СН з високим серцевим викидом).
1. Гіпоксичні стани:
- анемії, хронічне легеневе серце.
2. Підвищення обміну речовин:
- гіпертиреоз;
- вагітність.
Дані про вміст натрію у фармакологічних препаратах наведено в табл. 2.140.
Таблиця 2.140. Фармакологічні препарати з високим вмістом натрію
|
Препарат |
Вміст натрію в формі випуску |
|
Алендронова кислота, шипучі таблетки |
650 мг натрію в 1 табл. |
|
Ампіцилін/сульбактам, розчин для ін’єкцій |
115 мг натрію в 1,5 г амп. |
|
Азитроміцин, розчин для ін’єкцій |
114 мг в 500 мг амп. |
|
47 мг в 1 табл. 23,7 мг/мл |
|
|
Метронідазол, розчин для ін’єкцій |
790 мг в 500 мг амп. |
|
Нафцилін, розчин для ін’єкцій |
132 мг в 2 г амп. |
|
Омепразол/бікарбонат натрію |
304 мг в 1 капс. 406 мг в одній пластині |
|
Оксацилін, розчин для ін’єкцій |
128 мг в 2 г амп. |
|
Піперацилін/тазобакам, розчин для ін’єкцій |
128 мг в 2,25 г амп. 192 мг в 3,375 г амп. 256 мг в 4,5 г амп. |
|
Поліетиленгліколь, порошок для приготування розчину |
1,46 г/л |
|
Розчин фосфату натрію |
4,4 г/118 мл |
|
Полістаролсульфат натрію, суспензія |
1500 мг/60 мл |
|
Тикарцилін/клавуланат калію, розчин для ін’єкцій |
429 г в 3,1 г амп. |
Вміст натрію у фарамакологічних препаратах слід обов’язково враховувати, застосовуючи їх у лікуванні хворих із СН [46].
Найчастішими причинами СН є ІХС (включаючи гострий ІМ, постінфарктний кардіосклероз), АГ, клапанні вади серця. Частка ІХС та АГ становить близько 75% випадків СН.
Патогенез СН складний і до кінця не вивчений. Раніше вважалося, що СН — це гемодинамічна хвороба; нині вона розглядається як нейрогуморальна та енергетична проблема з подальшими гемодинамічними змінами.
До провідних патогенетичних механізмів формування та прогресування СН належать:
1. Гіперактивація нейрогуморальних систем організму (симпатоадреналової системи, РААС, антидіуретичного гормону, передсердного натрійуретичного пептиду).
2. Збільшення синтезу ендотеліну, тромбоксану, ангіотензину ІІ, що призводить до вазоконстрикції (збільшення постнавантаження) та зменшення синтезу вазодилататорів (оксиду азоту, простацикліну) і перевантаження серця, виникнення дисфункції ендотелію.
На початкових етапах розвитку СН відбувається активація цих систем, в результаті чого розвивається систолічна та діастолічна дисфункції серця, які мають адаптивний характер і направлені на збереження достатнього серцевого викиду, системного АТ і перфузії органів і тканин. Компенсаторно-пристосована реакція серця та судин відбувається за рахунок підвищення ЧСС, підвищення серцевого викиду з наступним розвитком гіпертрофії, збільшення постнавантаження (вазоконстрикція), переднавантаження та ОЦК (фізіологічна затримка натрію і води) тощо.
Тривала і надмірна активація нейрогуморальних систем призводить до надмірної затримки натрію та води в організмі (набряковий синдром); різкого збільшення загального периферичного судинного опору (порушення перфузії органів і тканин); надмірного збільшення перед- і постнавантаження, що призводить до зниження інотропної та насосної функції серця; стимуляції синтезу колагену та розвитку кардіофіброзу; розвитку некрозу кардіоміоцитів, прогресивного ураження серцевого м’яза та формування міогенної дилатації серця. Внаслідок цих змін відбувається зниження утворення енергії для величезної роботи серця в перекачуванні крові та її доставки до тканин організму, що має першочергове значення. Розрізняють ГСН та ХСН.
Компенсаторні механізми при СН:
1. Механізм Франка — Старлінга (посилення систоли при діастолічному перевантаженні).
2. Ремоделювання міокарда:
а) ГЛШ (зумовлює зменшення навантаження на одиницю маси серцевого м’яза):
- концентрична (при перевантаженні тиском);
- ексцентрична (при перевантаженні об’ємом і дилатацією);
б) дилатація ЛШ.
3. Рефлекс Бейнбриджа, який виникає в порожнистих венах і передсердях.
4. Підвищення функції симпатичної нервової системи у відповідь на зниження перфузії органів і тканин (полегшує умови функціонування серцево-судинної системи за рахунок акселерації метаболічних процесів, тахікардії, мобілізації крові з депо).
5. Активація РААС (у відповідь на зниження ниркового кровотоку).
6. Стимуляція секреції передсердного натрійуретичного чинника і антидіуретичного гормону.
7. Вазоконстрикція.
8. Затримка натрію і води, збільшення ОЦК.
2.9.1. Гостра серцева недостатність
Визначення. Гостра лівошлуночкова СН — це клінічний синдром, що супроводжується раптовою нездатністю серця забезпечувати кровопостачання органів та систем, в яких відбуваються важливі метаболічні процеси.
ГСН поділяється на гостру лівошлуночкову та правошлуночкову (див. ТЕЛА) СН. При ГЛШН часто виникає набряк легень.
Набряк легень — це раптовий клінічний синдром, в основі якого лежить підвищена гідратація тканини легень, спричинена зниженням їхньої функціональної здатності.
ГСН на догоспітальному етапі розвитку гострого ІМ виникає в 4–5% випадків, а летальність у розвитку подібного ускладнення сягає 9,9%. Серед пацієнтів, госпіталізованих з приводу ГСН різної етіології, первинна СН становить у середньому 32,7% випадків.
Реєстрація ГСН на фоні гострого ІМ дозволила встановити підвищення госпітальної смертності з 6% (при збереженні функції ЛШ) до 12% у разі розвитку набряку легень та до 80% — при кардіогенному шоку поряд зі зростанням щорічної смертності до 30–40%. Гостра декомпенсована СН належить до захворювань із дуже поганим прогнозом стосовно життя пацієнта: рівень госпітальної смертності становить 5%; смертність у 30-денний термін після виписки зі стаціонару — 10%; протягом року помирають близько 40% хворих.
Причини гострої лівошлуночкової СН і фактори, що погіршують її перебіг [28, 60]:
1. Декомпенсація ХСН; фактори, що спричиняють швидке наростання ГСН.
2. ГКС:
- ІМ/нестабільна стенокардія зі значним ступенем ішемії та ішемічної дисфункції;
- ускладнення гострого ІМ механічного походження;
- інфаркт ПШ.
3. Гіпертензивний криз.
4. Гостра аритмія (ШТ, ФШ, ФП чи ТП, інші надшлуночкові тахікардії).
5. Клапанна регургітація/ендокардит/розрив сухожильних хорд серця, погіршення перебігу раніше розвиненої клапанної регургітації.
6. Тяжка форма гострого міокардиту.
7. Тампонада серця.
8. Розшарування аорти.
9. Кардіоміопатія в післяпологовий період.
10. Фактори, що спричиняють швидше наростання ГСН:
- недотримання режиму лікування;
- перевантаження об’ємом;
- інфекції, зокрема пневмонія чи септицемія;
- тяжка форма інсульту головного мозку;
- стан після значного хірургічного втручання;
- погіршення функції нирок;
- бронхіальна астма;
- зловживання лікарськими засобами;
- зловживання алкогольними напоями;
- феохромоцитома, ЦД.
11. Синдроми високого серцевого викиду:
- септицемія;
- тиреоїдний криз;
- анемія;
- синдром шунта.
Патогенез. Основні патогенетичні ланки розвитку набряку легень [11, 25, 28]:
1) активація симпатичної НС, РААС, збільшення синтезу ендотеліну-1, тромбоксану і зменшення синтезу оксиду азоту та простацикліну, що сприяє розвитку гіпоксемії та гіпоксії органів і тканин;
2) зниження скоротливої здатності ЛШ з розвитком систолічної та діастолічної дисфункції міокарда; чим більша діастолична дисфункція ЛШ, тим більше знижується ФВ і більше зростає КСО та КДО;
3) підвищення гідростатичного тиску в капілярах, що призводить до підвищення кінцевого діастолічного тиску в ЛШ і збільшення КДО ЛШ. Коли гідростатичний тиск становить 20–30 мм рт. ст., він зрівнюється з онкотичним тиском і відбувається активне проникнення плазми крові в інтерстицію легень і в порожнину альвеол;
4) на фоні ГСН відбувається ураження нирок із порушенням функцій та ураженням ендотелію канальців — виникає кардіоренальний синдром.
Класифікація. T. Kіllіp, І.T. Kіmbal (1967) виділяють чотири класи набряку легень при ІМ:
1 клас — ознаки дисфункції ЛШ не визначаються;
2 клас — протодіастолічний ритм галопу, помірний чи середньотяжкий застій в легенях, вислуховуються вологі хрипи (<50% поверхні легень), гіпервентиляція;
3 клас — тяжкий набряк легень (>50% поверхні легень) з вираженими вологими хрипами — тяжка СН.
4 клас — кардіогенний шок (САТ <90 мм рт. ст., олігоурія, ціаноз).
Вперше виникла СН може виникати гостро (наприклад при ІМ) або підгостро (поступово) в період невизначеного часу, а може персистувати чи минати (тоді пацієнти стають компенсованими), але ризик повторного нападу зберігається (рекомендації ESC, 2012).
Клінічні профілі пацієнтів із ГСН наведені в табл. 2.141.
Таблиця 2.141. Клінічні профілі пацієнтів із ГСН
|
Застійні явища (–) |
Застійні явища (+)
|
|
|
Гіпоперфузія (–) |
Теплий – сухий |
Теплий – вологий |
|
Гіпоперфузія (+)
|
Холодний – сухий |
Холодний – вологий |
Класифікація ГСН:
- Некомпенсована застійна ГСН — це первинна чи гостра декомпенсація ХСН з характерними скаргами і симптомами.
- ГСН із АГ або гіпертензивними кризами, яка поєднується з гіпертензією з відносно збереженою скорочувальною властивістю ЛШ без рентгенологічних ознак набряку легень.
- Набряк легень підтверджений рентгенологічно з характерними клінічними симптомами.
- Кардіогенний шок зі зниженням насосної функції серця після корекції переднавантаження.
- ГСН з високим серцевим викидом характеризується підвищеним ХОК і ЧСС.
- Правошлуночкова ГСН характеризується синдромом малого серцевого викиду з підвищенням венозного тиску в яремних венах, збільшенням печінки та артеріальною гіпотензією. Трапляється при хронічній легеневій патології з легеневою гіпертензією, ТЕЛА, гострому ІМ ПШ тощо.
2.9.1.1. Гостра лівошлуночкова недостатність
Клініка. ГЛШН супроводжується нападом інспіраторної задишки, яка різко збільшується при незначному фізичному навантаженні, ортопное. Виникає тахіпное, ціаноз, притуплення перкуторного звуку над легенями; вислуховуються звучні дрібно-, середньо- і великопухирчасті хрипи, які мають тенденцію до зростання. Рентгенологічно визначається інтерстиційний набряк, посилення легеневого малюнку, іноді ущільнення по ходу міждольової щілини, а при накопиченні транссудату в альвеолах — гомогенне затемнення високої інтенсивності різної форми [46, 49].
Діагностичні критерії ГЛШН наведено в алгоритмі 2.92.
|
Алгоритм 2.92. Критерії діагностики ГЛШН (набряку легень) [17] Інтерстиційний набряк легень характеризується появою раптового нападу інспіраторної ядухи частіше вночі (вагус), інколи вдень. Хворому важко лежати, він сідає, хоче відкрити кватирку, але не може (найменше фізичне зусилля збільшує задишку). Хворий блідий, покривається холодним потом, визначається ціаноз губ та нігтів. Може виникати сухий кашель. Частота дихання становить 30–35 уд./хв. Над легенями визначається притуплений (набряк інтерстиції) та тимпанічний звук (коливання стінок альвеол зменшується за рахунок зниження їхньої еластичності, тому при перкусії легень коливається повітря, що знаходиться в альвеолах). Вислуховується крепітація або сухі хрипи. Пульс частий, слабкого наповнення. Межі серця та аускультація зумовлені основним захворюванням. Якщо невідкладна допомога неефективна, інтерстиційний набряк легень переходить в альвеолярну стадію протягом декількох хвилин (рис. 2.15).
Альвеолярний набряк. Перебіг ще тяжчий. Виникає транссудація рідини в альвеоли з утворенням стійкої білкової піни. Розвивається клекотання в легенях, яке вислуховується на відстані. Виникає кашель, виділяється пінисте харкотиння рожевого кольору (інколи до 3–5 л), зумовлене еритроцитами, що проникають через стінку альвеол. Розвивається альвеолярно-капілярний блок і різко порушується дифузія кисню в кров. Зростає ціаноз. Вислуховуються вологі великокаліберні хрипи, спочатку в нижніх, а потім — в середніх і верхніх сегментах легень. Вени шиї набухають. Розрізняють блискавичну форму набряку легень, яка закінчується летально протягом кількох хвилин; гостру, що триває 2–4 год; підгостру — 4–12 год; затяжну — >12 год (до декількох діб). ЕКГ-критерії: синусова тахікардія, зміщення сегмента ST від ізолінії, P-mіtrale, зменшення чи збільшення зубця Т, суправентрикулярні або шлуночкові екстрасистоли, ФП. Критерії газового складу крові: визначається артеріолярна гіпоксемія (зниження рО2 в крові) та гіперкапнія (підвищення рСО2 в крові). Рентгенологічні критерії: інтерстиційний набряк (лінії Керлі), посилений легеневий малюнок; альвеолярний набряк — застій крові в легенях, центральна форма — симетричне гомогенне затемнення, дифузна — тіні різної інтенсивності в легенях, фокусна — обмежене або зливне затемнення у формі кола; застійні явища в легенях розсмоктуються протягом 2–3 діб, рідше — 7–10 діб. Критерії двомірної ехоКГ: ознаки основного захворювання серця, розширення ЛШ та ПШ, ЛП, зниження ФВ, систолічна та діастолічна дисфункція. При катетеризації серця з використанням плаваючого катетера Свана — Ганза (через яремну вену його вводять у ПШ і легеневу артерію) визначають тиск заклинення в легеневих артеріях (норма — 15–18 мм рт. ст.). Лабораторні критерії основного захворювання з характерними етіологічними змінами. |
Фактори, що спричиняють розвиток резистентності до лікування:
- тяжкі захворювання серця (ІМ, міокардити, кардіоміопатії тощо), супутні захворювання (бронхіальна астма, ХОЗЛ, ЦД, ТЕЛА, грип);
- інтоксикація серцевими глікозидами;
- виникнення тяжких аритмій та блокад серця (ФП, ТП, шлуночкова ПТ, повна АV-блокада);
- введення препаратів, що пригнічують скоротливу здатність серця (ББА, АК, ААП І класу) і підвищують навантаження на міокард (допамін, норепінефрин, ізопреналін);
- надмірне введення плазмозамінюючих речовин (альбумін людини, декстран + розчин натрію хлориду тощо), що посилюють приплив крові до правих відділів серця;
- виражена артеріальна гіпоксемія, гіпоксія, декомпенсований респіраторний та метаболічний ацидоз і алкалоз тощо.
Цілі лікування пацієнтів із ГСН за рекомендаціями Європейського товариства інтенсивної терапії (2005) та ESC, 2016 [49]
Клінічні:
↓ симптомів (задишки та/чи стомлюваності);
↓ клінічних ознак;
↓ маси тіла;
↑ діурезу;
↑ оксигенації.
Лабораторні:
- нормалізація рівня електролітів у сироватці крові;
↓ вмісту остаточного азоту, сечовини крові та/чи креатиніну;
↓ концентрації білірубіну в сироватці крові;
↓ рівня МНП у плазмі крові.
Гемодинамічні:
↓ тиску заклинення в легеневій артерії <18 мм рт. ст.;
↑ серцевого викиду та/чи УО.
Результати:
↓ тривалість перебування у відділенні інтенсивної терапії:
↓ тривалість перебування в лікарні;
↑ інтервалу перед повторною госпіталізацією;
↓ смертності.
Переносимість:
- низька частота вибування пацієнтів з курсу лікування;
- низька частота побічних реакцій.
Примітки: ↑ збільшення; ↓ зменшення.
В Україні невідкладна терапія при ГСН відображена в джерелах літератури і наказах МОЗ України [63]. Схема невідкладної допомоги при набряку легень представлена в алгоритмах 2.93 і 2.94.
|
Алгоритм 2.93. Надання невідкладної допомоги при набряку легень з підвищеним АТ [17] Мета терапії — зниження САТ на 20–30%. Крок 1. Усунення гіперкатехоламінемії, гіпервентиляції та нормалізація емоційного статусу: морфін — 0,3–0,5 мл 1% розчину (3–5 мг) в/в (високі дози спричиняють гіпотонію, пригнічення дихання, блювання, особливо у хворих похилого віку). Крок 2. Розвантаження малого кола кровообігу: фуросемід — 40–80 мг або 0,5–1 мг/кг в/в чи торасемід 20–40 мг в/в. Препарат у високих дозах (>1 мг/кг) може супроводжувати рефлекторне збільшення вазоконстрикції на тлі швидкої втрати значних обсягів внутрішньосудинної рідини. Крок 3. Зменшення переднавантаження (венозного притоку крові) та зниження тиску в легеневій артерії: 1) накладання турнікетів на три кінцівки на 20 хв; 2) нітропрусид натрію — 50 мг (0,5–5 мкг/кг/хв) в/в крапельно (тривале застосування препарату у високих дозах недоцільне); 3) несиритид — новий вазодилататор для в/в введення (рекомбінантний мозковий натрійуретичний гормон), який спочатку вводять 2 мг/кг струминно, потім 0,01 мг/кг/хв до 48 год; його недоцільно призначати при ХНН, артеріальній гіпотензії, аортальному стенозі; 4) нітрогліцерин — 2–5 мл 1% розчину (ізосорбіду динітрат — 20 мг) в/в крапельно. Крок 4. Оксигенація та руйнування піни в альвеолах: 1) інгаляція киснево-спиртової суміші; 2) антифомсилан (інгаляція 2–3 мл 10% спиртового розчину). |
Примітка. Усі лікувальні заходи проводять одночасно; при бронхообструктивному синдромі показане введення теофіліну 240–480 мг в/в.
|
Алгоритм 2.94. Надання невідкладної допомоги при набряку легень зі зниженим системним АТ [17] Крок 1. Підвищення скоротливої, насосної функції міокарда та системного АТ (але ці препарати здатні викликати проаритмогенну дію): 1) допамін — 1–2 мл 0,5% розчину чи 5–20 мкг/кг/хв в/в крапельно; тривала інфузія допаміну (>24–48 год) спричиняє розвиток толерантності та частково гемодинамічний ефект; 2) добутамін — 1–2 мл 0,5% розчину чи 5–20 мкг/кг/хв в/в крапельно; препарат не рекомендується пацієнтам із некоронарогенним стенозом аортального та/чи мітрального отвору; 3) поєднане застосування цих препаратів. Для підвищення інотропної функції серця необхідно призначати левосимендан по 12–24 мкг/кг в/в протягом 10 хв; 0,05–0,2 мкг/кг/хв в/в крапельно; за наявності гіпотензії терапію слід починати з інфузії, минаючи болюсне введення, яке підвищує інотропну функцію серця, розширює артеріоли і венули за рахунок відкриття АТФ-чутливих калієвих каналів судинної стінки, в тому числі КА. Ефект левосимендану зберігається до 7 наступних днів після припинення інфузії; толерантність до препарату не виникає; вплив на ФВ, УО, ЧСС і тиск заклинювання легеневої артерії чітко проявляється на 5-й хвилині в/в введення. Крок 2. Зменшення альвеолярно-капілярної проникності (переважно при респіраторному дистрес-синдромі) та підвищення системного АТ: преднізолон 60–90 мг (до 1000 мг/добу) в/в крапельно. Крок 3. Зменшення переднавантаження (венозного притоку крові) та зниження тиску в легеневій артерії: 1) накладання турнікетів на три кінцівки на 20 хв; 2) нітрогліцерин — 1–5 мл 1% розчину, нітросорбіду тринітрат — 20 мг в/в крапельно при САТ >110 мм рт. ст. Крок 4. Розвантаження малого кола кровообігу: фуросемід — 40–80 мг або 0,5–1 мг/кг в/в чи торасемід — 20–40 мг в/в. Крок 5. Призначення піногасників: 1) інгаляція киснево-спиртової суміші; 2) інгаляція 2–3 мл 10% розчину антифомсилану. Крок 6. Внутрішньоаортальна балонна контрапульсація виконується у спеціалізованих кардіологічних відділеннях при кардіогенному шоку, розшаровуючій аневризмі аорти, аортальній регургітації, ураженні периферичних артерій, фінальній стадії ХСН, коли прогресивно знижується АТ. При цьому внутрішньоаортальний балончик (обсяг становить від 15 до 50 мл) встановлюється в грудному відділі низхідної аорти. Катетер закріплюється на апараті для внутрішньоаортальної контрапульсації, нагнітається гелій в діастолу, а в систолу всмоктується з балончика; в діастолу поліпшується коронарний кровотік і кровопостачання міокарда, що дозволяє відновити гемодинамічну стабільність [4]. |
Примітки: 1) при підвищенні САТ до ≥110 мм рт. ст. можна обережно вводити нітропрусид натрію; 2) допамін слід вводити одночасно з нітропрусидом натрію (підвищує серцевий викид, знижує тиск наповнення ЛШ).
Уточнення відносно введення інотропних засобів при ГСН наведено у табл. 2.142.
Таблиця 2.142. Введення інотропних засобів при ГСН (за рекомендаціями Європейського товариства інтенсивної терапії, 2012)
|
Лікарський засіб |
Болюсне введення |
Швидкість в/в інфузії |
|
Добутамін |
Не застосовують |
2–20 мг/кг/хв (дія на β-рецептори) |
|
Допамін |
Не застосовують |
<3 мкг/кг/хв: вплив на нирки (β-рецептори); 3–5 мкг/кг/хв: інотропний ефект (вплив на β-рецептори); >5 мкг/кг/хв (вплив на β-рецептори, судинозвужувальний вплив (на α-рецептори)) |
|
Левосимендан |
12–24 мкг/кг* протягом 10 хв |
0,1 мкг/кг/хв; можна знизити до 0,05 або підвищити до 0,2 мкг/кг/хв |
|
Норепінефрин |
Не застосовують |
0,2–1,0 мкг/кг/хв |
|
Епінефрин |
1 мг можна ввести в/в під час реанімації, а також повторно через 3–5 хв |
0,05–0,5 мкг/кг/хв |
Примітки. Приєднання левосимендану до норепінефрину та добутаміну призводить до підвищення серцевого індексу.
*У країнах, представлених у ESС, обмежено дозвіл на продаж препаратів. Доза, рекомендована на цей час. У пацієнтів з артеріальною гіпотензією терапію необхідно починати без болюсного введення. Рекомендація категорії ІІb, рівень доказовості С.
Показання і схема дозування вазодилататорів при ГСН наведені в табл. 2.143.
Таблиця 2.143. Показання і схема дозування вазодилататорів при ГСН (за рекомендаціями Європейського товариства інтенсивної терапії, 2012)
|
Препарат |
Показання |
Схема дозування |
Основні побічні ефекти |
Інше |
|
Нітрогліцерин |
ГСН, коли рівень АТ адекватний |
Почати з 20 мкг/хв, підвищувати дозу до 200 мкг/хв |
Артеріальна гіпотензія, головний біль |
Толерантність при тривалому застосуванні |
|
Ізосорбіду динітрат |
ГСН, коли рівень АТ адекватний |
Почати з 1 мг/год, підвищувати дозу до 10 мг/год |
Артеріальна гіпотензія, головний біль |
Толерантність при тривалому застосуванні |
|
Нітропрусид натрію |
Гіпертензивний криз, кардіогенний шок (у поєднанні з інотропними засобами) |
0,3–5 мкг/кг/хв/ |
Артеріальна гіпотензія, токсичність у зв’язку з утворенням ізоціонату |
Лікарський засіб чутливий до дії світла |
|
Несиритид |
Гостра декомпенсована СН |
Болюсно 2 мкг/кг + в/в крапельно 0,015–0,03 мкг/кг/хв |
Артеріальна гіпотензія |
В алгоритмі 2.95 наведено схему надання невідкладної допомоги при набряку легень, згідно з рекомендаціями групи AHА/ACC/HFSA (2017).
|
Алгоритм 2.95. Надання невідкладної допомоги при набряку легень залежно від висоти АТ 1. САТ <70 мм рт. ст.:
2. САТ 70–100 мм рт. ст.:
3. САТ >100 мм рт. ст.: добутамін (2–20,0 мкг/кг/хв). 4. САТ >110 мм рт. ст.: нітрогліцерин (починати зі швидкості 10–20 мкг/кг/хв, надалі залежно від клінічного ефекту). |
Дозування та спосіб введення діуретиків залежно від ступеня СН наведено в табл. 2.144.
Таблиця 2.144. Дозування та спосіб введення діуретиків залежно від ступеня СН
|
Тяжкість затримки рідини |
Діуретик |
Доза, мг |
Коментар |
|
Помірна |
Фуросемід |
20–40 |
Перорально або в/в. Титрування дози |
|
Торасемід |
0,5–1,0 10–20 |
Моніторування вмісту калію, магнію, натрію, креатиніну та АТ |
|
|
Тяжка |
Фуросемід |
40–100 |
в/в |
|
Фуросемід (інфузія) |
5–40 мг/год |
Інфузія фуросеміду ефективніша, ніж болюсне введення |
|
|
Буметамід |
1–4 |
Перорально або в/в |
|
|
Торасемід |
20–100 |
Перорально або в/в |
|
|
Рефрактерність до фуросеміду |
Додати торасемід |
10–20 (до 100) |
Порушення функції нирок не відображається на фармакологічних властивостях торасеміду, оскільки він метаболізується на 80% у печінці |
|
Гідрохлоротіазид |
25 мг двічі на добу |
Комбінація з тіазидами краща, ніж високі дози петльових діуретиків |
|
|
Метолазон |
2,5 мг 1 раз на добу |
Більший ефект досягається при КК <30 мг/хв |
|
|
Спіронолактон |
25–50 мг 1 раз на добу |
Оптимальний вибір дози препарату за відсутності ХНН і гіперкаліємії |
|
|
Рефрактерність до петльових діуретиків і тіазидів |
Додавання допаміну для ниркової вазодилатації чи добутаміну як інотропного засобу |
За наявності ХНН слід розглянути питання про застосування ультрафільтрації або гемодіалізу |
Особливості лікування аритмій при ГСН наведено в табл. 2.145.
Таблиця 2.145. Лікування пацієнтів з аритмією при ГСН за рекомендаціями Європейського товариства інтенсивної терапії [49]
|
ФШ або ШТ з відсутністю пульсу |
Виконують дефібриляцію при 200–300–360 Дж (рекомендується двофазна дефібриляція з максимальним розрядом 200 Дж). У разі резистентності до перших розрядів парентерально вводять епінефрин у дозі 1 мг або вазопресин у дозі 40 МО та/чи аміодарон у дозі 150–300 мг парентерально |
|
ШТ |
Якщо стан пацієнта нестабільний — виконують кардіоверсію; за стабільного стану можливе застосування аміодарону чи лідокаїну для досягнення медикаментозної кардіоверсії |
|
Синусова тахікардія чи надшлуночкова тахікардія |
Застосування ББА, якщо вони переносяться пацієнтом, з урахуванням клінічного стану й параметрів гемодинаміки:
Рідко застосовуються:
|
|
ФП або ТП |
За можливості — кардіоверсія. Для сповільнення AV-провідності можна застосовувати дигоксин у дозі 0,125–0,25 мг в/в або болюсно, ББА чи аміодарон. Аміодарон може зумовити медикаментозну кардіоверсію без порушення гемодинаміки в ЛШ. Пацієнтові необхідне також лікування препаратами гепарину |
|
Брадикардія |
Атропін у дозі 0,25–0,5 мг в/в до досягнення сумарної дози 1–2 мг. Тимчасово — ізопреналін у дозі 1 мг в 100 мл ізотонічного розчину натрію хлориду в/в крапельно з максимальною швидкістю 75 мг/год (2–12 мкг/хв). Якщо брадикардія не усувається за допомогою атропіну, як тимчасовий захід необхідно застосовувати черезшкірну або черезвенну електрокардіостимуляцію. Теофілін можна застосовувати у пацієнтів з гострим ІМ, у яких брадикардія не усувається введенням атропіну в дозі 0,25–0,5 мг/кг болюсно з подальшою інфузією зі швидкістю 0,2–0,4 мг/кг/год |
Стандарти лікування при ГСН за рекомендаціями доказової медицини наведені в табл. 2.146, особливості діагностики та лікування захворювань, що лежать в основі ГСН — в табл. 2.147.
Таблиця 2.146. Доказовість фармакотерапії при ГСН за рекомендаціями доказової медицини
|
Засоби |
Клінічні рекомендації |
Клас, рівень доказовості |
|
ББА |
При ГСН за наявності хрипів ББА застосовують з обережністю. Для лікування хворих з ішемією міокарда і тахікардією рекомендується застосовувати метопролол |
ІІb, С |
|
У пацієнтів із гострим ІМ з метою стабілізації ГСН на ранньому етапі необхідно застосовувати ББА |
ІІа, В |
|
|
У хворих на ХСН застосування ББА необхідно починати тоді, коли стан пацієнта стабілізується після ГСН (зазвичай через 4 дні) |
І, А |
|
|
Добутамін |
Застосування добутаміну показане за наявності периферичної гіпоперфузії (артеріальна гіпотензія, погіршення функції нирок із застоєм або без застою) чи набряку легень, стійких хрипів для відновлення об’єму при застосуванні діуретиків і вазодилататорів |
ІІа, С |
|
Левосимендан |
Застосування левосимендану показане в пацієнтів із симптомами СН з низьким серцевим викидом на тлі систолічної дисфункції серця без тяжкої артеріальної гіпотензії |
ІІа, В |
Таблиця 2.147. Особливості діагностики та лікування захворювань, що лежать в основі ГСН, згідно з рекомендаціями доказової медицини
|
Захворювання |
Клінічні рекомендації |
Клас, рівень доказовості |
|
ІХС, |
ЕхоКГ-дослідження необхідне всім пацієнтам із гострим ІМ і симптомами СН з метою з’ясування функціонального стану серця |
|
|
При кардіогенному шоку внаслідок розвитку ГКС коронарну ангіографію та реваскуляризацію необхідно виконати якнайшвидше |
І, С |
|
|
Пацієнтам з ІМ не рекомендується метаболічна підтримка за допомогою введення глюкози, інсуліну й калію у високих дозах (за винятком пацієнтів із ЦД) |
ІІ, А |
|
|
Коли стан гемодинаміки продовжує залишатися нестабільним протягом декількох годин, можна розглянути доцільність введення постійного катетера в легеневу артерію |
ІІ, В |
|
|
Тромбоз штучного клапана серця, ускладнений ГСН |
Розвиток цього тромбозу асоціюється з високою летальністю. Цим пацієнтам необхідно виконувати рентгенографію грудної клітки і ехоКГ |
І, В |
|
Тромболітичні засоби застосовують при правобічних штучних клапанах у пацієнтів групи високого ризику, в яких можливе оперативне втручання. Хірургічне втручання краще виконувати при лівошлуночковому тромбозі штучного клапана серця |
ІІа, В |
|
|
Ниркова недостатність, ускладнена ГСН |
У пацієнтів із тяжкою дисфункцією нирок виконання перед процедурою гемодіалізу ефективне для запобігання розвитку нефропатії. Розвиток ниркової недостатності може відбуватися при введенні контрастних середовищ (тому їх можна вводити в надмалих кількостях). Відмова від застосування лікарських засобів із нефротоксичними властивостями (НПЗП, попередня терапія АСК та/чи фенолдопамом) |
ІІb, В |
|
Аритмія при ГСН |
При гострій ФП не рекомендується застосовувати верапаміл і дилтіазем, оскільки вони погіршують перебіг СН і спричиняють розвиток AV-блокади ІІІ ступеня. При ФП успішно застосовують аміодарон і ББА з метою контролю ЧСС і профілактики рецидивів аритмії |
І, А |
|
Необхідно нормалізувати рівень калію і магнію в плазмі крові, особливо у пацієнтів із шлуночковими аритміями |
ІІb, В |
|
|
Застосування аміодарону і ББА може запобігти повторному розвитку ФШ як причини чи наслідку ГСН |
І, А |
|
|
У разі розвитку шлуночкової аритмії, а також у пацієнтів із нестабільною гемодинамікою необхідно негайно виконати ангіографію і ЕФД. За наявності локалізованих проаритмогенних субстратів виконують радіочастотну абляцію |
ІІb, С |
|
|
ГСН, зумовлена гострим ІМ |
ЕхоКГ дасть змогу діагностувати розрив міжшлуночкової перегородки, величину скидання крові зліва направо, а також наявність мітральної недостатності |
І, С |
|
Хірургічне втручання необхідно виконувати якнайшвидше при розриві міжшлуночокової перегородки, оскільки розрив може збільшитись і спричинити кардіогенний шок |
І, С |
|
|
Гостра мітральна регургітація |
Пацієнтам із гострою тяжкою мітральною регургітацією і набряком легень або кардіогенним шоком необхідне екстрене оперативне втручання |
І, С |
Профілактика. Після купірування набряку легень і стабілізації легеневої та центральної гемодинаміки необхідно здійснювати превентивне лікування у вигляді моно- чи комбінованої терапії такими засобами:
- іАПФ самостійно чи в поєднанні з тіазидними та петльовими діуретиками;
- іАПФ (або БРА) + діуретик + пролонговані нітрати;
- іАПФ + діуретик + триметазидин;
- іАПФ + діуретик + ББА карведилол.
Дози зазначених препаратів підбирають оптимальні.
2.9.1.2. Гостра правошлуночкова недостатність
Визначення. Гостра правошлуночкова недостатність — синдром, який швидко прогресує і характеризується виникненням системної затримки рідини внаслідок порушення наповнення ПШ та/чи зниження його насосної функції. Найчастіше цей синдром виникає при збільшенні перед- та післянавантаження на ПШ з подальшою дилатацією його камери та розвитком регургітації на тристулковому клапані. На сьогодні важко оцінити поширеність гострої правошлуночкової недостатності.
Головні причини розвитку гострої правошлуночкової недостатності:
- ГЛШН;
- ТЕЛА;
- гостра ішемія міокарда.
Гостра правошлуночкова недостатність трапляється у 3–9% госпіталізацій з приводу ГСН. При цьому госпітальна летальність при гострій правошлуночковій недостатності становить 5–17%. Останнім часом науковці та клініцисти все більше уваги приділяють вивченню функції та дисфункції ПШ.
Етіологія розвитку гострої правошлуночкової недостатності (ЄТК, 2016):
- ГЛШН.
- Ішемія або ІМ ПШ.
- Гостра ТЕЛА.
- Загострення ХОЗЛ або гіпоксія.
- Гостре ураження легень або гострий респіраторний дистрес-синдром.
- Хронічна легенева гіпертензія.
- Сепсис.
- Захворювання перикарда, надшлуночкова ПТ та ШТ.
- Вроджені та набуті вади серця.
- Кардіоміопатії, міокардит.
- Кардіохірургічні втручання.
- Гематологічні захворювання.
Патогенез. При гострій правошлуночковій недостатності відбувається гостра дилатація ПШ, міжшлуночкова перегородка зміщується вліво як у систолу, так і діастолу. Зміщення міжшлуночкової перегородки спричиняє компресію ЛШ, порушує його наповнення і призводить до зниження скоротливості. Гостра дилатація ПШ призводить до підвищення тиску в порожнині перикарда, що, в свою чергу, знижує розтягнення ЛШ та його наповнення (перенавантаження) і призводить до різкого зниження УО ЛШ [11].
У пацієнтів із пре- або посткапілярною хронічною легеневою гіпертензією в термінальній стадії відбувається розвиток гіпертрофії та дилатації ПШ, що призводить до трикуспідальної регургітації та зниження ФВ.
При гострій правошлуночковій недостатності відбувається венозний застій; дисфункція ПШ спричиняє підвищення тиску в правому передсерді.
Клінічні та біохімічні маркери при гострій правошлуночковій недостатності наведені в табл. 2.148.
Таблиця 2.148. Клінічні ознаки та біохімічні маркери гострої правошлуночкової недостатності (ЄТК, 2016)
|
Клінічні ознаки |
Біохімічні маркери |
|
Гіпоксемія |
Підвищення рівня лактату |
|
Ознаки застою у великому колі кровообігу |
Підвищення рівня натрійуретичних пептидів (НУП типу В або NT-проНУП типу В) |
|
Розтягнення яремних вен, печінково-яремних рефлекс |
Підвищення рівнів кардіальних тропонінів І або Т |
|
Периферичні набряки, прекардіальний випіт, застійна гепатоспленомегалія, асцит, анасарка |
Порушення показників функціонального стану печінки (наприклад підвищення активності трансаміназ, рівня білірубіну, пролонгований протромбіновий час) |
|
Ознаки дисфункції ПШ |
Порушення функціонального стану нирок (азот сечовини крові, креатинін) |
|
Третій серцевий тон, систолічний шум трикуспідальної регуртації, пульсація печінки, ознаки супутньої дисфункції ЛШ. Парадоксальний пульс |
Рівні D-димера |
Особливості діагностики, перебігу та лікування ТЕЛА, легеневої гіпертензії наведені в розділі 3.
ІМ ПШ
Гострий ІМ ПШ зазвичай є некрозом міокарда його нижньої стінки і виникає в результаті раптової оклюзії проксимального відділу правої КА. Незважаючи на те що у 30–50% пацієнтів з гострим ІМ нижньої стінки ЛШ може залучатися і ПШ, такі явища, як тяжка гіпотензія та низький серцевий викид, трапляються нечасто внаслідок широкого впровадження реперфузійної терапії. Такі ускладнення, як брадикардія, AV-блокади високого ступеня, ШТ та розрив міжшлуночкової перегородки, частіше виникають у пацієнтів з ІМ ПШ.
Застосування препаратів, які знижують перенавантаження ПШ (наприклад нітрати, діуретики), може бути небезпечним, при цьому слід ретельно підійти до проблеми оптимізації волемічного стану з метою запобігання порушення гемодинаміки.
Також важливим аспектом є запобігання брадикардії чи її корекція за допомогою атропіну або теофіліну. AV-блокади високого ступеня зазвичай негайно відповідають на реперфузію. Якщо цього не стається, може виникати потреба в кардіостимуляції.
Гостра правошлуночкова недостатність в умовах відділення інтенсивної терапії
Гостра правошлуночкова недостатність часто трапляється у практиці відділень інтенсивної терапії. Основною її причиною є гострий респіраторний дистрес-синдром, за якого поширеність гострої правошлуночкової недостатності становить 25–50%, що залежить від ступеня тяжкості й режиму механічної вентиляції. Більшість пацієнтів з гострим респіраторним дистрес-синдромом перебувають на вентиляції з позитивним тиском наприкінці видиху. Гостра правошлуночкова недостатність легко діагностується за допомогою ехоКГ, при цьому черезстравохідна ехоКГ може застосовуватися для моніторингу інкубованих пацієнтів.
Клапанні вади (ЄТК, 2016)
Гостра дисфункція ПШ можлива як при лівобічних, так і при правобічних клапанних вадах серця. При появі лівобічних клапанних вад виникає ситуація, коли величина центрального венозного тиску може бути недостатньою для підтримання легеневого кровотоку в умовах підвищеного тиску наповнення ЛП, що призводить до гострої правошлуночкової недостатності. Трикуспідальна недостатність — найчастіша правобічна клапанна вада, залучена до патогенезу гострої дисфункції ПШ.
Правобічний інфекційний ендокардит становить близько 5–10% усіх випадків інфекційного ендокардиту, він найпоширеніший серед ін’єкційних наркоманів. Правобічний ендокардит може виникати на нативних і штучних клапанах, при вроджених вадах серця, а також на імплантованих пристроях. Гостра дисфункція ПШ може виникати в результаті деструкції тристулкового клапана та гострої трикуспідальної недостатності, які призводять до перевантаження ПШ об’ємом та його дилатації.
Лікування при гострій правошлуночковій недостатності наведено в табл. 2.149.
Таблиця 2.149. Лікувальні заходи у пацієнтів з гострою правошлуночковою недостатністю (ЄТК, 2016)
|
Стратегія |
Властивості та застосування |
Застереження |
|
Оптимізація волемічного стану |
||
|
Навантаження рідиною, фізіологічний розчин або розчин Рінгера лактатний >200 мл/15–30 хв |
Розглянути питання у пацієнтів з декомпенсованою недостатністю ПШ, нормальним центральним венозним тиском, низьким АТ |
Навантаження рідиною може викликати перерозтягнення шлуночків, погіршення шлуночкової взаємозалежності та зниження серцевого викиду |
|
Діуретики |
||
|
Якщо пацієнт не отримує планової діуретичної терапії, доцільною є початкова доза 20–40 мг в/в; у разі планової діуретичної терапії початкова доза фуросеміду має бути принаймні еквівалентною пероральній |
Введення в/в петльових діуретиків рекомендоване всім пацієнтам із симптомами/ознаками перевантаження рідиною з метою їх регресу |
Може спричиняти погіршення функціонального стану нирок і гіпокаліємію |
|
Діуретична терапія може призначатися як у формі інтермітивних болюсів, так і тривалою інфузією |
||
|
Питання про комбінування петльових діуретиків із тіазидними або спіронолактоном може розглядатися в пацієнтів із резистентним набряковим синдромом або недостатньою клінічною відповіддю на діуретичну терапію |
||
|
Вазопресори та інотропи |
||
|
Норепінефрин 0,2–1,0 мкг • кг-1 • хв-1 |
Стимулює інотропну функцію ПШ, підвищує системний АТ, сприяє позитивній шлуночковій взаємодії, відновлює коронарний перфузійний градієнт |
Надмірна вазоконстрикція може погіршувати тканинну перфузію |
|
Добутамін 2–20 мкг • кг-1 |
Стимулює інотропну функцію ПШ, знижує тиск наповнення у шлуночках |
Може посилювати артеріальну гіпотензію, якщо не комбінувати із вазопресором, особливо за наявності лівошлуночкової недостатності. Може індукувати чи погіршувати перебіг аритмій |
|
Левосимендан 0,1–0,2 мкг • кг-1 • хв-1 (болюсне введення у дозі 6–12 мк/кг необов’язкове і не рекомендоване, якщо САТ <90 мм рт. ст.). Швидкість інфузії може бути зменшена до 0,05 мкг • кг-1 • хв-1 або збільшена до 0,2 мкг • кг-1 • хв-1) |
Поєднує властивості стимуляції інотропії ПШ та легеневої вазодилатації; позитивно впливає на порушення правошлуночково-артеріальної взаємодії |
Може посилювати артеріальну гіпотензію. Може індукувати або погіршувати перебіг аритмій |
|
Механічна підтримка кровообігу |
||
|
Екстракорпоральна мембранна оксигенація/екстракорпоральна підтримка життя |
Швидка короткочасна підтримка; може застосовуватися разом з оксигенатором |
Ускладнення при застосуванні впродовж тривалішого періоду (>5–10 днів) |
|
Мікроаксіальна помпа, приєднана до черезшкірного катетера |
Обмежена спроможність помпи; у разі кардіогенного шоку чи потреби у встановленні помпи з високим потоком надають перевагу екстракорпоральній підтримці життя |
|
|
Паракорпоральні правошлуночкові допоміжні пристрої |
Можуть застосовуватися впродовж більш тривалого періоду (наприклад, тижні або місяці); можуть поєднуватися з оксигенаторами у випадку необхідності легеневої підтримки |
|
Таким чином, діагностика, лікування та невідкладна терапія гострої правошлуночкової недостатності вивчена значно ліпше, ніж ГЛШН. ЄТК у 2016 р. гострій правошлуночковій недостатності приділило значно більше уваги. Але поряд з цим при гострій правошлуночковій недостатності є ще багато «білих плям», які в майбутньому потрібно вирішувати шляхом проведення глибоких наукових, клінічних та рандомізованих плацебо-контрольованих досліджень.
2.9.2. Хронічна серцева недостатність
Визначення. ХСН — нездатність серця забезпечувати рівень кровотоку, відповідний до метаболічних (перш за все енергетичних) потреб.
ХСН — найбільш часте й серйозне захворювання серцево-судинної системи, що призводить до стійкої втрати працездатності та значного скорочення тривалості життя хворих. Частота виявлення ХСН за останні 20 років підвищилась удвічі, що зумовлено покращенням ранньої діагностики та збільшенням середньої тривалості життя. Ризик смерті при початкових проявах ХСН становить 5–10%, при розгорнутій симптоматиці — 30–40%. П’ятирічна виживаність при всіх формах ХСН становить <30% у чоловіків і <40% у жінок.
Декомпенсацією СН називають гостре, підгостре та хронічне поглиблення СН під впливом низки факторів (ішемія міокарда, ІМ, гостра клапанна недостатність АГ, ШТ, ТЕЛА, інфекції, НПЗП тощо). Про стабільну ХСН йдеться у тому разі, коли на тлі підтримувального лікування щонайменше впродовж останнього місяця не спостерігається прогресування клінічної симптоматики і відсутні явні ознаки затримки рідини.
Етіологія ХСН розглянута вище.
Основні патогенетичні ланки ХСН [14, 49, 63]:
1. При ХСН спочатку відбуваються енергетичні, нейрогуморальні, а потім — гемодинамічні зміни в системі кровообігу.
2. Відбувається зниження енергетичного обміну, активація симпатоадреналової системи для підтримання АТ на оптимальному рівні та перфузія життєво важливих органів і тканин в умовах зниженого серцевого викиду. Збільшення синтезу катехоламінів призводить до підвищення загального периферичного опору артеріальних судин та збільшення постнавантаження; збільшення венозної вазоконстрикції — до зростання венозного повернення крові до серця, тобто збільшення переднавантаження.
3. Активується РААС. Збільшується синтез ангіотензину ІІ, альдостерону, посилюється реабсорбція натрію та води в ниркових канальцях, що призводить до збільшення ОЦК, підвищення навантаження на серце, затримки натрію, води та виникнення набряків.
4. Виникає ендотеліальна дисфункція за рахунок збільшення синтезу вазопресорів (ендотеліну-1, ангіотензину ІІ, тромбоксану) та зменшення утворення вазодилататорів (оксиду азоту, простацикліну).
5. Збільшується продукція антидіуретичного гормону (вазопресину), внаслідок чого підвищується реабсорбція натрію в ниркових канальцях під впливом альдостерону, що призводить до зростання ОЦК, артеріальної та венозної вазоконстрикції.
6. Порушується синтез передсердного натрійуретичного гормону, що зменшує реабсорбцію натрію і води в канальцях і збільшує клубочкову фільтрацію, а також гальмує синтез реніну, ангіотензину ІІ, альдостерону.
7. Виникає гіпертрофія міокарда, перенавантаження міокарда та його ураження, від чого знижується скоротлива здатність серця. Встановлено, що спочатку виникає ремоделювання серця, діастолічна, а потім систолічна дисфункція міокарда, яка сприяє розвитку гіпоксії органів і тканин та виникненню набрякового синдрому.
8. У результаті цих складних змін відбувається розвиток енергетичної недостатності серця, що є ключовою ланкою патогенезу СН.
Класифікація ХСН. VІ Національний конгрес кардіологів України (2000) прийняв класифікацію СН, за основу якої взята класифікація М.Д. Стражеска та В.Х. Василенка.
Класифікація ХСН за М.Д. Стражеском та В.Х. Василенком [19, 35]
Клінічні стадії: І, ІІА, ІІБ, ІІІ.
І стадія — початкова, прихована недостатність кровообігу. Суб’єктивні та об’єктивні ознаки СН у спокої відсутні. Задишка, тахікардія, ціаноз з’являються виключно під час фізичного навантаження. Працездатність збережена.
ІІ стадія супроводжується ознаками СН у спокої: задишка і тахікардія більш виражені.
ІІА стадія — задишка і тахікардія виникають у разі невеликого фізичного навантаження. Наявні ознаки недостатності одного зі шлуночків: застій у малому колі кровообігу при недостатності лівих відділів серця і застій у великому колі при недостатності правих відділів серця. Характерні ціаноз, блідість шкіри, помірне збільшення печінки, її болючість, набряки на ногах, які з’являються під вечір і минають до ранку; значно знижена толерантність до фізичних навантажень.
ІІБ стадія — спостерігається недостатність усіх відділів серця (застій як у малому, так і у великому колі кровообігу). Характерні акроціаноз, тахікардія, накопичення рідини в черевній порожнині (асцит), легенях (гідроторакс), перикарді (гідроперикард). Порушення гемодинаміки значні та стійкі, працездатність різко обмежена.
ІІІ стадія — термінальна, незворотна, дистрофічна, кахектична. У внутрішніх органах і тканинах виникають глибокі незворотні дистрофічні зміни (кардіальний цироз печінки, за сучасною термінологією — фіброз печінки); відбувається повна втрата працездатності.
Варіанти СН:
- зі зниженою ФВ ЛШ (ФВ ЛШ ≤40%);
- зі збереженою ФВ ЛШ (ФВ ЛШ >40%).
Класифікація функціонального стану хворих із СН за клінічними критеріями NYHA, 1964
І ФК — пацієнти із захворюваннями серця, в яких під час звичайних фізичних навантажень не виникає задишки, втоми чи серцебиття.
ІІ ФК — пацієнти із захворюваннями серця та помірним обмеженням фізичної активності. При цьому задишка, втома, серцебиття спостерігаються під час виконання звичайних фізичних навантажень.
ІІІ ФК — пацієнти із захворюваннями серця та вираженим обмеженням фізичної активності. У стані спокою скарги відсутні, але навіть під час незначних фізичних навантажень виникають задишка, втома, серцебиття.
ІV ФК — пацієнти із захворюваннями серця, в яких будь-який рівень фізичної активності спричиняє зазначені вище симптоми. Останні виникають і в стані спокою.
У діагнозі ХСН необхідно зазначити: клінічну стадію (І, ІІА, ІІБ, ІІІ), ФК за класифікацією NYHA (І, ІІ, ІІІ, ІV). Орієнтовна відповідність клінічних стадій СН і ФК: І стадія відповідає ІІ ФК; ІІА стадія — ІІІ ФК; ІІБ стадія — ІV ФК; ІІІ стадія — ІV ФК. Визначення варіантів СН (зі зниженою чи зі збереженою ФВ ЛШ) можливе лише за наявності відповідних даних ехоКГ-дослідження.
Варіанти СН
При ХСН виникає систолічна та діастолічна дисфункція.
Систолічна дисфункція виникає у більшості випадків ГСН та ХСН, яка характеризується такими гемодинамічними порушеннями:
- зниженням УО, ХОК, ФВ, дилатацією ЛП, збільшенням КДР >55 мм;
- підвищенням кінцевого діастолічного тиску (тиску наповнення) ЛШ;
- збільшенням КДО — шлуночкова (міогенна) дилатація;
- застоєм крові в малому та великому колах кровообігу (відповідно при ліво- та правошлуночковій СН).
У 25–30% пацієнтів із ХСН визначається діастолічна дисфункція шлуночків, яка характеризується такими гемодинамічними змінами:
- значним та раннім підвищенням кінцевого діастолічного тиску (тиску наповнення шлуночків);
- застоєм крові в венозному руслі малого та великого колах кровообігу;
- малозміненими чи нормальними показниками УО, ХОК;
- відсутністю значної дилатації шлуночків (малозмінений КДО), дилатацією ЛП;
- ФВ ЛШ >45%;
- концентричною ГЛШ;
- ознаками порушення діастолічного наповнення при допплер-ехоКГ.
Для діагностики первинної діастолічної СН потрібні три підстави: 1) симптоми СН; 2) збережена чи незначно знижена систолічна функція ЛШ (ФВ 45–50%); 3) ознаки порушення релаксації ЛШ, розтяжності ЛШ або діастолічної жорсткості. Крім того, потрібно обов’язково встановити, чи не уражені легені.
На початковій стадії діастолічної дисфункції типовим є порушення розслаблення міокарда, яке характеризується зниженням розслаблення міокарда, зменшенням швидкості раннього трансмітрального потоку (Е), компенсаторним збільшенням передсердно-залежної швидкості цього потоку (А) і як наслідок — зниженням співвідношення Е/А (рис. 2.16 і 2.17).
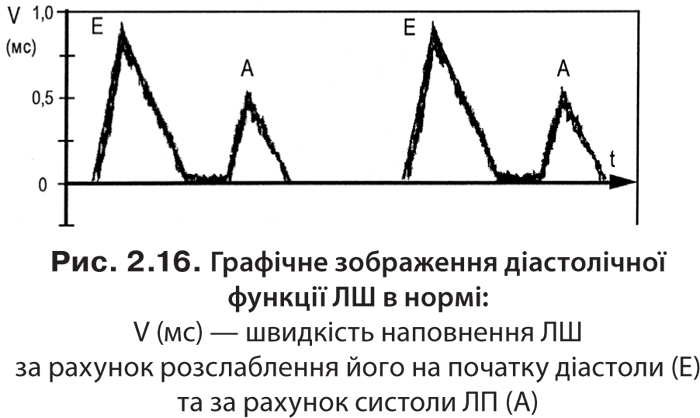
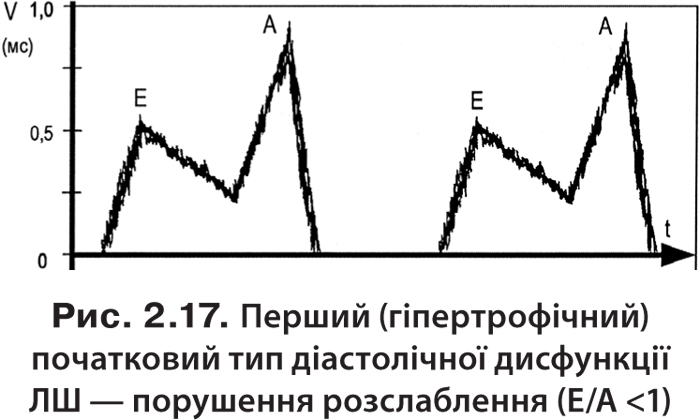
У пацієнтів між порушенням розслаблення і рестриктивним типом діастолічного наповнення співвідношення Е/А і тривалість сповільнення (ДТ) можуть бути не змінені — це псевдонормальний тип наповнення ЛШ. Цей тип відрізняється від нормального зменшенням швидкості Е, що визначається за допомогою тканинної допплер-ехоКГ (рис. 2.18).
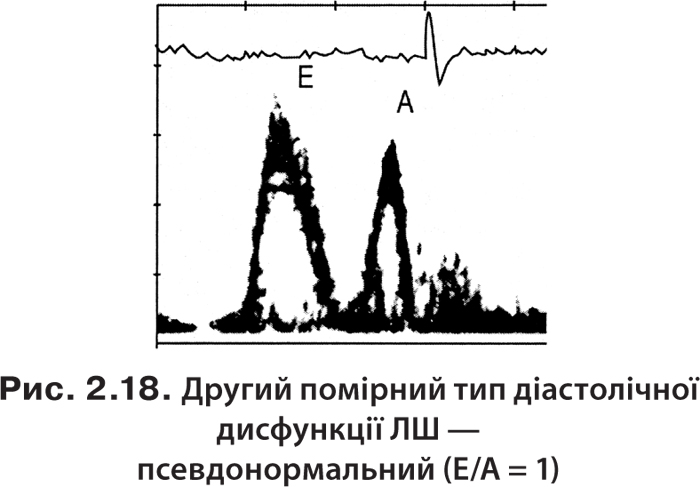
У пацієнтів із тяжкими хворобами серця може визначатися рестриктивний тип наповнення зі збільшенням швидкості Е, скороченням часу сповільнення піку Е (ДТ) і помірним збільшенням співвідношення Е/А. Збільшена швидкість раннього наповнення ЛШ (Е) зумовлена підвищенням тиску в ЛП, що й призводить до збільшення раннього діастолічного трансмітрального градієнта тиску (рис. 2.19).
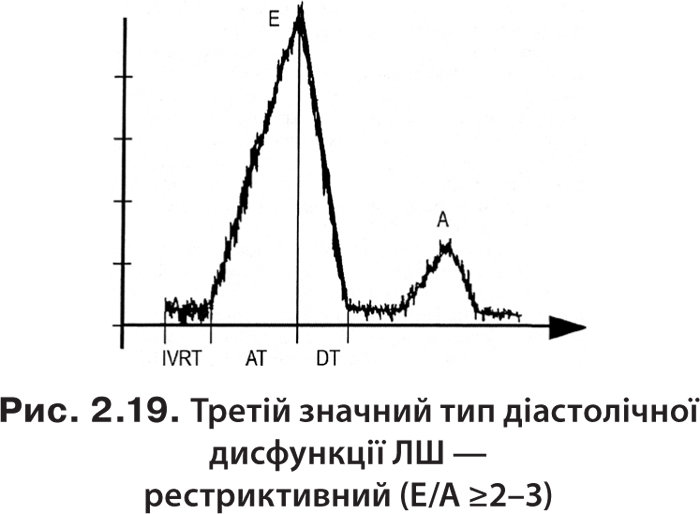
Слід зазначити, що три типи діастолічної дисфункції ЛШ (порушення розслаблення, псевдонормальний і рестриктивний) відповідають легкій, середньотяжкій і тяжкій дисфункцїі.
При діастолічній дисфункції визначається зниження здатності розслаблення та зменшення розтягнення міокарда — «жорстке» серце. У хворих з ізольованим порушенням діастолічної функції збільшується кінцевий діастолічний тиск, а ФВ та КДО знаходяться в межах норми. При порушенні розслаблення та виникненні зниження розтягнення ЛШ відбувається застій крові в легенях. У результаті обмеження наповнення шлуночків може спостерігатися зниження УО та серцевого викиду, незважаючи на нормальну чи навіть підвищену ФВ. При захворюваннях серця та судин порушення діастолічної функції спостерігається у >30% випадків. Перш за все діастолічна дисфункція ЛШ спостерігається при АГ, ІХС, ГКМП, рестриктивних ураженнях серця, амілоїдозі серця та констриктивному перикардиті. У хворих із систолічною дисфункцією вони можуть погіршувати її функціональний стан.
До клінічних симптомів хронічної лівошлуночкової СН належать задишка при фізичному навантаженні, ортопное, набряк легень, кардіогенний шок, які супроводжуються застоєм крові в малому колі кровообігу. При хронічній правошлуночковій СН у великому колі кровообігу визначається підвищення пульсації набухлих шийних вен, збільшення печінки, периферичні набряки, а в пізніх стадіях захворювання — накопичення рідини в порожнинах (асцит, гідроторакс, гідроперикард).
Стадія СН відтворює стан клінічної еволюції цього синдрому, тоді як ФК пацієнта є динамічною характеристикою, що може змінюватися під впливом лікування. Діастолічна дисфункція міокарда відображена на рис. 2.16–2.19 [58].
Визначення варіантів СН зі зниженою ФВ ЛШ або зі збереженою ФВ ЛШ можливе лише за наявності даних ехоКГ. ФК хворого встановлюють за клінічними критеріями; іноді, за необхідності, він може бути об’єктивізований даними інструментальних методів дослідження.
Приклади формулювання діагнозу:
- ІХС: постінфарктний кардіосклероз, перенесений Q-ІМ передньоверхівкової стінки ЛШ (дата). Хронічна аневризма передньоперегородкової ділянки ЛШ. СН ІІА стадії зі зниженою ФВ ЛШ, ІІІ ФК.
- ДКМП, постійна форма ФП. СН ІІБ стадії зі зниженою ФВ ЛШ, ІV ФК.
- ДКМП, вторинна недостатність мітрального клапана, постійна форма ФП, CHA2DS2-VASc 3 бали, HAS-BLED 2 бали. СН ІІБ стадії зі зниженою ФВ ЛШ, ФК ІV.
- ГКМП з обструкцією виносного тракту ЛШ. СН ІІА стадії зі збереженою ФВ ЛШ, NYHA ІІІ.
- Дегенеративно-кальцинуюча хвороба клапанів серця: критичний аортальний стеноз. СН ІІА стадії із систолічною дисфункцією ЛШ, NYHA ІІІ.
- Хронічна ревматична хвороба серця, активність І ступеня, комбінована мітральна вада з перевагою стенозу, СН ІІБ стадії зі зниженою ФВ ЛШ, NYHA ІV.
Якщо у хворого наявна стабільна стенокардія напруження, в діагнозі зазначають тільки ФК останньої; ФК пацієнта з ХСН за NYHA не наводять.
Клініка ХСН наведена в класифікації. У більшості випадків клінічні прояви гострої та ХСН зумовлені переважно систолічною дисфункцією шлуночків. Внаслідок порушення розслаблення та виникнення зниження розтягнення ЛШ виникає застій крові в легенях. У результаті обмеження наповнення шлуночків можливе зниження УО та серцевого викиду, незважаючи на нормальну чи навіть підвищену ФВ.
Найтиповіші ознаки ХСН, діастолічної функції ЛШ та найтиповіші лабораторні відхилення при СН — табл. 2.150–2.152.
Таблиця 2.150. Найтиповіші патологічні ехоКГ-зміни при ХСН та їх клінічна оцінка
|
Показник |
Патологічне відхилення |
Про що може свідчити |
|
ФВ ЛШ |
Зниження (≤40%) |
Систолічна дисфункція ЛШ |
|
Сегментарний рух стінок ЛШ |
Акінез, гіпокінез, дискінез |
ІМ, ішемія |
|
КДР і КДО ЛШ |
Збільшення (розмір ≥60 мм, індекс КДО >97 мл/м2) |
Дилатація. Перевантаження об’ємом |
|
КСР ЛШ |
Збільшення (розмір ≥45 мм, індекс КСО >43 мл/м2) |
СН. Перевантаження об’ємом |
|
Розмір ЛП |
Збільшення (передньо-задній розмір ≥40 мм, індекс об’єму >34 мл/м2) |
Систолічна чи діастолічна дисфункція ЛШ. Дисфункція мітрального клапана |
|
Інтеграл швидкості викиду крові в аорту |
Зменшення (<15 см) |
Зменшення УО |
|
Показник |
Патологічне відхилення |
Про що може свідчити |
|
Структура та функція клапанів |
Стеноз і/або недостатність |
Ревматична або неревматична вада може бути причиною СН |
|
Максимальна швидкість регургітації на трикуспідальному клапані |
Збільшення (>3,4 м/с) |
Підвищений систолічний тиск у ПШ |
|
Систолічна екскурсія площини трикуспідального кільця |
Зменшення (<16 мм) |
Систолічна дисфункція ПШ |
|
Розрахунковий систолічний тиск у легеневій артерії |
>40 мм рт. ст. |
Легенева гіпертензія |
|
Нижня порожниста вена |
Дилатація; відсутність колабування на вдиху |
Правосерцева недостатність, венозна гіпертензія |
|
Стан перикарда |
Випіт. Потовщення. Кальцифікація |
Гідроперикард. Тампонада. Гострий або хронічний перикардит (зокрема зумовлений системними захворюваннями сполучної тканини). Уремія. Метастази пухлин |
Таблиця 2.151. Орієнтовна клінічна оцінка допплерівських показників діастолічної функції ЛШ
|
Показник |
Відхилення |
Про що може свідчити |
|
Відношення Е/А трансмітрального потоку |
Тип погіршеної релаксації (<1) |
Сповільнення розслаблення ЛШ, нормальний тиск наповнення ЛШ |
|
Рестриктивний тип (>2) |
Високий тиск наповнення ЛШ, перевантаження об’ємом |
|
|
Норма (1–2) |
Неінформативний (може бути «псевдонормальним») |
|
|
Оцінка трансмітрального потоку під час проби Вальсальви |
Трансформація «псевдонормального» типу у тип порушеної релаксації |
Підвищений тиск наповнення ЛШ, «демаскований» за допомогою проби Вальсальви |
Примітка. Е/А — співвідношення максимальних швидкостей відповідно раннього та пізнього діастолічного наповнення ЛШ за даними дослідження трансмітрального кровотоку. Визначення цих показників рекомендоване у пацієнтів із ХСН та збереженою ФВ ЛШ з метою об’єктивізації діастолічної недостатності ЛШ.
Таблиця 2.152. Найтиповіші лабораторні відхилення при СН
|
Аномалія |
Можливі причини |
Інтерпретація/алгоритм реагування |
|
Виражена ниркова дисфункція (ШКФ <60 мл/хв/1,73 м2, креатинін >150 мкмоль/л) |
|
|
|
Гіпокаліємія (<3,5 ммоль/л) |
|
|
|
Гіперкаліємія (>5,5 ммоль/л) |
|
|
|
Гіпонатріємія (<135 ммоль/л) |
|
|
|
Гіперурикемія (>500 мкмоль/л) |
|
|
|
Підвищення рівня тропоніну |
|
|
|
Підвищення печінкових ферментів |
|
|
|
Підвищення або зниження рівнів тиреоїдних гормонів |
|
|
|
МНВ >3,5 |
|
|
|
Анемія (Нb <120 г/л у жінок, <130 г/л у чоловіків) |
|
|
|
Низький рівень альбуміну в плазмі крові |
|
|
Остаточна оцінка вірогідності наявності СН та рівня ризику здійснюється за результатами клінічного огляду та обстежень.
Додаткові дослідження за показаннями (ВАКУ, 2018) [60]:
1. Магнітно-резонансне дослідження серця.
2. Стрес-ехоКГ.
3. Черезстравохідна ехоКГ.
4. Коронарна ангіографія.
5. КТ серця.
6. Холтерівське моніторування ЕКГ.
7. Тест із фізичним навантаженням.
8. Концентрація натрійуретичного пептиду у плазмі крові.
9. Кардіоспецифічні ферменти.
10. МНВ.
11. ТТГ.
12. Феритин у плазмі крові, насичення трансферину залізом.
13. Катетеризація правих відділів серця.
14. Ендоміокардіальна біопсія.
Стратифікація серцево-судинного ризику (ВАКУ, 2018) [60]
Оцінка клінічного прогнозу. Можливості індивідуального прогнозування перебігу ХСН є обмеженими, враховуючи те, що відомі з літератури відповідні прогностичні маркери відображають імовірність виживаності великих груп хворих, а не окремих пацієнтів. Втім, для визначення оптимальної стратегії ведення хворих лікареві слід враховувати доступні для визначення у звичайній клінічній практиці ознаки, наявність кожної з яких у пацієнтів із ХСН асоційована з поганим прогнозом виживаності.
Чинники, що спричиняють декомпенсацію клінічного стану хворих на ХСН:
- ГКС;
- неконтрольована АГ;
- суправентрикулярні аритмії, насамперед ФП;
- тяжкі розлади при брадикардії;
- стійка ШТ;
- вірусні інфекції, загострення хронічних бронхообструктивних захворювань;
- пневмонія;
- тромбоемболія легеневої артерії;
- прогресування ниркової чи печінкової недостатності;
- декомпенсація ЦД;
- виникнення чи прогресування анемії;
- виникнення або прогресування дисфункції щитоподібної залози (гіпо- чи гіпертиреоз);
- вагітність;
- зловживання алкоголем;
- недотримання рекомендацій щодо застосування фармпрепаратів;
- недотримання рекомендацій щодо вживання рідини;
- неадекватно призначена підтримувальна терапія;
- ятрогенія (призначення ліків зі списку, протипоказаних при ХСН; масивна інфузійна терапія з приводу супутнього захворювання без урахування наявної ХСН тощо).
Актуальною проблемою при ХСН є розвиток резистентності до лікування.
Фактори ризику резистентності до лікування ХСН [17, 41, 49, 63]:
- недіагностовані чи погано контрольовані супутні захворювання (ІМ, вади серця, ЦД, бронхіальна астма, бронхообструктивні захворювання легень, хронічні гепатити та цирози печінки, ХНН та печінкова недостатність тощо);
- кардіомегалія, що супроводжується значним зниженням інотропної та насосної функції серця і ФВ (становить ≤35%), розвиток набрякового синдрому;
- виражена гіпертрофія різних відділів міокарда, що призводить до ремоделювання серця;
- тяжкі порушення ритму серця (ФП, ТП, ШТ, повна АV-блокада тощо);
- відсутність сечогінних засобів серед застосованих препаратів, що призначаються при лікуванні СН;
- невиконання хворим призначень лікаря, неадекватне фізичне навантаження, надмірне споживання кухонної солі та рідини, що має вирішальне значення;
- артеріальна гіпоксемія, гіпоксія, гіпокаліємія, гіпомагніємія;
- підвищення в крові вмісту ГК, естрогенів, альдостерону, антидіуретичного гормону, активація симпатоадреналової системи, ренін-ангіотензинової системи;
- застосування деяких антигіпертензивних засобів (празозин, гідралазин), що затримують рідину в організмі;
- декомпенсований метаболічний та респіраторний ацидоз та алкалоз;
- зменшення кількості клубочків і канальців у нирках, зниження ниркового кровообігу, клубочкової фільтрації, розвиток протеїнурії.
Визначення рівня мозкового натрійуретичного пептиду (BNP) та N-термінального фрагмента попередника BNP (NT-pro BNP) все частіше використовується для діагностики та оцінки тяжкості СН (табл. 2.153). Комбінація ліків, що спричиняють резистентність до лікування і є потенційно шкідливими для пацієнтів із симптомною ХСН (табл. 2.154).
Таблиця 2.153. Потенційні причини підвищення рівня натрійуретичних пептидів (AHA/ACC/HFSA, 2017)
|
Кардіальні причини |
Некардіальні причини |
|
|
Таблиця 2.154. Ліки або комбінації ліків, що спричиняють резистентність до лікування і є потенційно шкідливими для пацієнтів із симптомною ХСН (NYHA ІІ–ІV) та систолічною дисфунцією ЛШ (доказова база)
|
Фармакологічні засоби |
Потенційні негативні ефекти |
|
НПЗП, в тому числі інгібітори ЦОГ-2 |
|
|
ГК |
|
|
АК (окрім амлодипіну та фелодипіну) |
|
|
ААП І класу. Дронедарон |
|
|
Моксонідин |
|
|
Блокатори α-адренорецепторів |
|
|
Трициклічні антидепресанти |
|
|
Антрацикліни. Трастузумаб |
|
|
Приєднання БРА (або інгібітора реніну) до комбінації |
|
Лікування при ХСН
Мета лікування хворих на ХСН:
1. Поліпшення клінічного статусу.
2. Поліпшення функціональних можливостей.
3. Запобігання госпіталізації та зниження смертності.
Етапність надання медичної допомоги (ВАКУ, 2018) [60]
Медична допомога пацієнтам із СН надається на первинному, вторинному (спеціалізована — амбулаторна і стаціонарна) та третинному (високоспеціалізована — амбулаторна та стаціонарна) рівнях медичної допомоги.
Первинна медична допомога пацієнтам із СН надається лікарями загальної практики — сімейними лікарями та дільничними лікарями-терапевтами — в амбулаторіях, амбулаторіях загальної практики — сімейної медицини, сільських лікарських амбулаторіях, в центрах первинної медико-санітарної допомоги, на прийомі у лікаря або в денному стаціонарі за місцем проживання (перебування) пацієнта (номенклатура згідно з Наказом МОЗ України від 28.10.2002 р. № 385 «Про затвердження переліків закладів охорони здоров’я, лікарських, провізорських посад та посад молодших спеціалістів з фармацевтичною освітою у закладах охорони здоров’я» та Наказу МОЗ України від 05.10.2011 р. № 646 «Порядок медичного обслуговування громадян центрами первинної медичної (медико-санітарної) допомоги»).
Вторинна медична допомога на амбулаторному рівні надається лікарями-кардіологами в діагностичних центрах, поліклініках — центральних міських, міських, центральних районних, районних, в центрах з медичних консультацій та діагностики (консультативно-діагностичних центрах), спеціалізованих медичних центрах (номенклатура згідно з наказом МОЗ України від 28.10.2002 р. № 385).
Вторинна медична допомога на стаціонарному рівні надається у спеціалізованих кардіологічних відділеннях багатопрофільних лікарняних закладів: у багатопрофільних лікарнях (клінічних лікарнях) інтенсивного лікування, лікарнях відновного (реабілітаційного) лікування, лікарнях (клінічних лікарнях) планового лікування, обласних центрах кардіологічної допомоги (номенклатура згідно з наказом МОЗ України від 28.10.2002 р. № 385 та Наказом МОЗ України та НАМН України від 24.07.2013 р. № 621/60 «Про систему кардіологічної допомоги у закладах охорони здоров’я України»).
Третинна медична допомога надається у науково-дослідних установах, кардіохірургічних центрах — регіонального, міжрегіонального, обласного рівня, відділеннях кардіохірургії закладів охорони здоров’я, центрах рентгеноендоваскулярної діагностики та лікування із функцією реперфузійних втручань (номенклатура згідно з наказом МОЗ України та НАМН України від 24.07.2013 р. № 621/60, Наказом МОЗ України та НАМН України від 11.03.2013 р. № 193/20 «Про систему кардіохірургічної допомоги в Україні» та Наказом МОЗ України та НАМН України від 18.03.2013 р. № 211/24 «Про організацію і роботу системи з рентгеноендоваскулярної діагностики та лікування у закладах охорони здоров’я України»).
Лікування хворих на ХСН ІІІ–ІV ФК зі зниженою ФВ ЛШ наведено в алгоритмі 2.96.
Важливу роль у лікуванні пацієнтів із ССЗ відіграє розпорядок дня (табл. 2.155).
Таблиця 2.155. Розпорядок дня пацієнта із ХСН
|
Показник |
ФК ХСН (NYHA) |
||
|
І–ІІ |
ІІІ |
ІV |
|
|
Денна повноцінна активність (год) |
10–12 |
6–8 |
1–2 |
|
Денна знижена активність (год) |
3–4 |
6–8 |
>8 |
|
Денний сон (год) |
– |
1–2 |
>2 |
|
Нічний сон (год) |
7–8 |
8 |
>8 |
|
Обов’язкова тривалість динамічного фізичного навантаження (хв) |
45 |
30 |
10–15 |
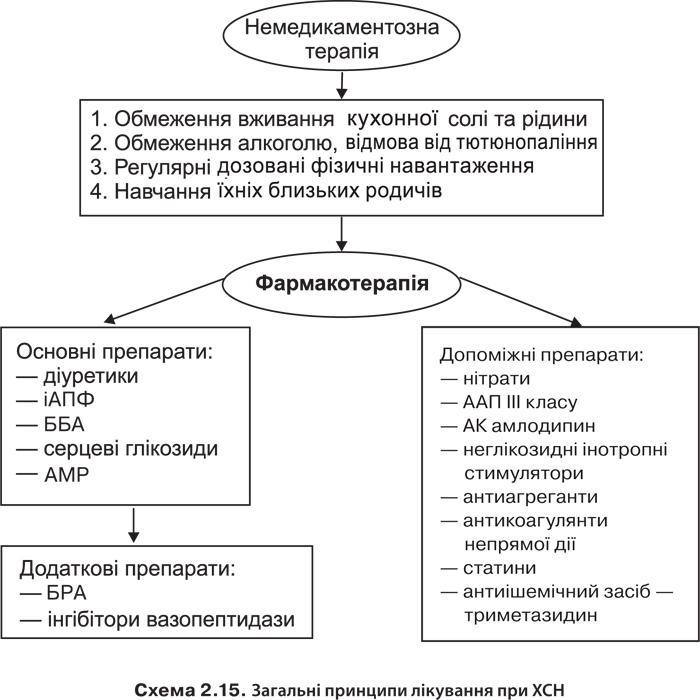
При ХСН проводять розвантаження системи кровообігу: 1) нейрогуморальне розвантаження (іАПФ, БРА, АМР, ББА); 2) гемодинамічне розвантаження (івабрадин, дигоксин, нітрати); 3) метаболічне розвантаження (антиішемічний засіб — триметазидин). Лікування при ХСН систематизовано в алгоритмі 2.97 і представлено схемами 2.14 і 2.15.
|
Алгоритм 2.97. Принципи лікування при ХСН [60] Крок 1. Зменшення навантаження на серце: 1) зменшення фізичного та психоемоційного перевантаження; 2) обмеження вживання рідини до 1 л і кухонної солі до 2–4 г/добу. Крок 2. Лікування основного захворювання (ІХС, АГ, аритмії, анемія, захворювання легень). Крок 3. Підвищення інотропної та насосної функції серця: 1) іАПФ, які зменшують систолічну дисфункцію ЛШ, нейрогуморальні та електролітні зміни, запобігають виникненню РСС, при їх непереносимості застосовують БРА); 2) серцевий глікозид дигоксин по 0,25 мг/добу при ФП; 3) симпатоміметичні засоби (допамін, добутамін, левосимендан — синтезатор кальцію на тлі артеріальної гіпотензії). Крок 4. Виведення надмірної кількості рідини:
Крок 5. Полегшення роботи серця шляхом зниження ЧСС і покращення діастолічної функції: ББА (карведилол, бісопролол, метопролол сукцинат, небіволол) та блокатор Іf-каналів івабрадин. Крок 6. Запобігання виникненню тромбоемболій: 1) антикоагулянти прямої дії: гепарин — 10–20 тис. ОД/добу, НМГ еноксапарин натрій — 0,4 мл/добу та їхні аналоги; 2) антикоагулянти непрямої дії — варфарин, ривароксабан, апіксабан, дабігатран; 3) антитромбоцитарні препарати (АСК, клопідогрель, прасугрел). Крок 7. Механічне видалення рідини: абдоменоцентез, торакоцентез, ультрафільтрація. Крок 8. Хірургічне лікування і різні пристрої:
|

Є переконливі дані, що фізичні вправи при СН покращують функцію ендотелію і переносимість фізичного навантаження. Хворим дозволяють будь-які фізичні навантаження (крім бігу), якщо вони нормально їх переносять.
Найефективнішими препаратами в лікуванні при ХСН є 1) ББА; 2) іАПФ; 3) БРА; 4) діуретики (петльові та АМР). Серцеві глікозиди менш ефективні в лікуванні цих пацієнтів (їх застосовують перорально при ФП) [29, 49].
Діуретики в лікуванні при ХСН. У хворих на ХСН найефективнішою може бути комбінація трьох діуретиків: фуросемід + гіпотіазид + спіронолактон. Ефективність торасеміду вища, ніж фуросеміду. У РКД TORІС торасемід знижував загальну смертність на 51,5%, кардіальну смертність — на 59,7%, РСС — на 65,8%. Препарат не порушує електролітний, ліпідний та вуглеводний обміни (метаболічно нейтральний) [14].
Торасеміду властива не тільки виражена протинабрякова, але й антигіпертензивна дія. У торасеміду вища біодоступність, ефективність його така сама, як фуросеміду, але при рефрактерній СН він ефективніший. Торасемід метаболічно нейтральний, оскільки він не впливає негативно на підвищення вмісту глюкози в крові та показники ліпідного обміну.
Комбінація петльових діуретиків з допаміном і добутаміном є ефективним засобом при ГСН.
АМР — це теж діуретики, які застосовуються з середини 60-х років ХХ сторіччя. АМР властива перш за все антиальдостеронова дія; вони здатні збільшувати діурез на 25%, зменшують загальну і серцево-судинну смертність. При ХСН ІІІ–ІV ФК з-поміж препаратів цієї групи найчастіше застосовують спіронолактон у дозі 25–50 мг/добу та селективний антагоніст альдостерону еплеренон у дозі 25–50 мг/добу. Доведено, що поєднання трьох нейрогуморальних модуляторів (спіронолактону чи еплеренону + ББА + іАПФ) є найбільш доцільним у лікуванні ХСН тяжких резистентних форм (!).
Отже, діуретики застосовуються для усунення набрякового синдрому, зменшення кількості госпіталізацій, однак вони не сповільнюють прогресування ХСН і не покращують прогноз хворих (окрім АМР). Лікування при ХСН розпочинають із тіазидних діуретиків, а у разі їхньої неефективності або недостатньої ефективності призначають петльові діуретики в комбінації з АМР. З-поміж петльових діуретиків тільки торасемід здатний блокувати РААС, оскільки він ефективніший, не чинить негативного впливу на вуглеводний і жировий обмін та не спричиняє синдрому рикошету.
Вивченню впливу діуретиків при ХСН на кінцеві точки присвячено чимало рандомізованих плацебо-контрольованих досліджень з доказової медицини. За їхніми даними, у хворих із тяжкою ХСН використання високих доз петльових діуретиків призводить до резистентності й погіршення виживаності пацієнтів, а застосування іАПФ у високих дозах — до зниження смертності. Тому при тяжкій ХСН слід призначати петльові діуретики у невисоких дозах і комбінувати їх з іАПФ, БРА чи спіронолактоном. Високі дози петльових та тіазидних діуретиків можуть призводити до виникнення фатальних аритмій за рахунок гіпокаліємії та активації РААС.
У дослідженні RALES (1999) доведено, що при ХСН ІІІ–ІV ФК після застосування спіронолактону спостерігається зниження загальної та серцево-судинної смертності. Діуретики зазвичай повинні поєднуватися з іАПФ і БРА.
Дози призначення діуретиків та їхні побічні реакції наведені в табл. 2.156, 2.157.
Таблиця 2.156. Дози діуретиків, зареєстрованих в Україні, для лікування при ХСН
|
Препарат |
Початкова доза, мг |
Цільова доза, |
Максимальна доза, мг |
Основні побічні реакції |
|
Петльові діуретики |
||||
|
Фуросемід |
20–40 |
40–240 |
250–500 |
Гіпокаліємія, гіпомагніємія, гіпонатріємія |
|
Торасемід |
5–10 |
10–20 |
100–200 |
Порушення кислотно-основного стану |
|
Тіазиди і тіазидоподібні діуретики |
||||
|
Гідрохлоротіазид |
25 |
25–50 |
50–100 |
Гіпокаліємія, гіпомагніємія, гіпонатріємія |
|
Індапамід |
2,5 |
2,5–5 |
2,5–5 |
Порушення кислотно-основного стану |
|
Калійзберігаючі діуретики (АМР) |
||||
|
Спіронолактон |
25–50 |
25–50 |
100–200 |
Гіперкаліємія, гінекомастія |
|
Еплеренон |
25 |
25–50 |
25–50 |
Гіперкаліємія |
Таблиця 2.157. Найтиповіші прояви побічної дії діуретиків (салуретиків) і тактика лікаря
|
Побічна дія |
Тактичні варіанти |
|
Гіпокаліємія. Гіпомагніємія |
|
|
Гіпонатріємія |
|
|
Дегідратація |
|
|
Наростання рівня креатиніну |
|
Останнім часом дуже багато уваги приділяється лікуванню ХСН іАПФ і БРА. іАПФ мають такі властивості:
1) знижують активність симпатоадреналової системи, РААС, зменшують синтез ендотеліну, тромбоксану та підвищують концентрацію в крові оксиду азоту і простацикліну, що призводить до зменшення вазоконстрикції та збільшення вазодилатації;
2) сповільнюють процеси ремоделювання серця, судин та інших органів;
3) сприяють зворотному розвитку гіпертрофії міокарда, зменшують систолічну дисфункцію;
4) перешкоджають розвитку прогресування дилатації ЛШ;
5) сповільнюють формування інтерстиційного фіброзу міокарда;
6) знижують діастолічну ригідність ЛШ;
7) спричиняють коронарну вазодилатацію за рахунок збільшення синтезу оксиду азоту та брадикініну;
8) покращують регіонарний кровотік у нирках, головному мозку, скелетних м’язах та інших органах; знижують ризик виникнення аритмій.
Правила призначення та контролю лікування іАПФ та БРА:
1. Відмінити активну діуретичну терапію чи знизити дозу діуретиків за 24 год до призначення першої дози іАПФ.
2. Відмінити або знизити дози препаратів із системною вазодилатуючою дією (насамперед нітратів).
3. Не починати лікування цими препаратами при рівнях САТ <90 мм рт. ст., К+ у плазмі крові >5,0 ммоль/л, креатиніну в плазмі крові >220 мкмоль/л.
4. Вимірювати АТ, рівень К+ та креатиніну в плазмі крові через 1–2 тиж після кожного наступного підвищення дози іАПФ.
Застосування різних іАПФ у лікуванні ХСН призводить до однакової клінічної ефективності: зниження частоти повторних госпіталізацій у зв’язку з регресом ХСН або зниження ризику смертельного перебігу захворювання і підвищення виживаності хворих.
іАПФ застосовують (табл. 2.158) за наявності симптомів СН чи дисфункції ЛШ без клінічних проявів. Дозу іАПФ підвищують поступово, кожні 1–2 тиж (з одночасним визначенням електролітів у крові) до оптимальної.
Таблиця 2.158. Рекомендовані початкові та підтримувальні дози іАПФ для лікування при СН [11, 14, 49, 63]
|
Препарат |
Початкова доза |
Цільова доза |
|
Каптоприл |
6,25 мг 3 рази на добу |
50 мг 3 рази на добу |
|
Еналаприл |
2,5 мг 2 рази на добу |
20 мг 2 рази на добу |
|
Лізиноприл |
2,5–5,0 мг 1 раз на добу |
20–40 мг 1 раз на добу |
|
Раміприл |
2,5 мг 1 раз на добу |
10,0 мг на добу |
|
Трандолаприл |
0,5 мг 1 раз на добу |
4 мг 1 раз на добу |
НПЗП знижують ефективність іАПФ за рахунок блокади синтезу простацикліну. Особливо слід уникати цього поєднання при набряковому синдромі, але комбінація АСК в дозі 75–100 мг/добу з іАПФ можлива і широко застосовується. Доцільно комбінувати іАПФ з антиагрегантом клопідогрелем (рівень доказовості С). Для профілактики ХСН при ІХС можливе застосування двох іАПФ — периндоприлу і раміприлу (рівень доказовості А). Є спостереження, що на початковій і латентній стадії СН іАПФ запобігають розвитку клінічної стадії СН.
Для лікування при ХСН застосовуються такі іАПФ: каптоприл, еналаприл, лізиноприл, раміприл та трандолаприл. За даними РКД вони зумовлювали зниження частоти повторних госпіталізацій (у зв’язку з регресом декомпенсації серця), смертності та підвищення виживаності хворих.
БРА є альтернативою іАПФ. Вважають, що ця група препаратів однаково ефективно знижує смертність і частоту ускладнень. При гострому ІМ, ускладненому СН чи дисфункцією ЛШ, застосування БРА (табл. 2.159) або іАПФ водночас знижує смертність. Підходи до початку терапії БРА відповідають таким до застосування іАПФ.
Таблиця 2.159. Рекомендовані дози БРА, при застосуванні яких відзначали зниження смертності та частоти розвитку ускладнень у пацієнтів із ХСН
|
Препарат |
Початкова доза |
Цільова доза |
|
Кандесартан |
4–8 мг |
32 мг |
|
Лозартан |
25–50 мг |
150 мг |
|
Валсартан |
20–40 мг 2 рази на добу |
160 мг 2 рази на добу |
ББА широко застосовують для лікування хворих на ХСН. Під впливом ББА спостерігається:
- негативний хронотропний ефект (зниження ЧСС);
- негативний інотропний ефект за рахунок зменшення роботи серця;
- негативний дромотропний ефект (сповільнюється АV-провідність);
- зниження активності симпатоадреналової системи та РААС;
- антиаритмічний ефект і підвищення порогу ФШ за рахунок антифібриляторної дії;
- антигіпертензивний, антиаритмічний, антиангінальний (антиішемічний), антиадренергічний та антифібриляторний ефекти;
- сповільнення чи блокування процесів ремоделювання серця;
- покращення діастолічної функції;
- відновлення чутливості β-адренорецепторів до зовнішніх регуляторних стимулів;
- збільшення серцевого викиду при тривалій терапії;
- зменшення загибелі кардіоміоцитів (за рахунок некрозу чи апоптозу).
Доказовою медициною переконливо доведено, що при ХСН із ББА потрібно застосовувати карведилол, бісопролол, метопрололу сукцинат, які значно знижують смертність і подовжують термін життя. Останні дані свідчать, що небіволол порівняно з плацебо у пацієнтів із ХСН віком старше 70 років знижує тільки комбінований показник загальної смертності і частоту госпіталізацій при ССЗ (рандомізоване дослідження SENІORS). За даними РКД карведилол підвищував виживаність хворих порівняно з короткодіючим метопрололу тартратом. Поєднане застосування ББА та іАПФ ефективніше знижувало смертність при ХСН, ніж монотерапія цими препаратами [49, 63]. Одночасне застосування іАПФ, БРА та АМР не рекомендується, оскільки виникає ризик розвитку гіперкаліємії.
Якщо попередню дозу ББА хворі переносять добре, то через кожні 1–2 тиж її можна подвоювати. У разі розвитку артеріальної гіпотензії спочатку знижують дозу вазодилататора, а за необхідності на короткий термін знижують також дозу ББА. ББА у комбінації з іАПФ удвічі знижують смертність при СН.
У рекомендаціях ЄТК (2016) зазначається, що ББА — препарати, які збільшують ФВ при СН. При застосуванні ББА у хворих з СН в перші 3–5 днів можлива затримка рідини в організмі й наростання симптомів декомпенсації серця протягом 1–2 тиж.
Згідно з даними РКД СOPERNІСUS, СІBІS-ІІ, MERІT-HF, при ХСН під впливом ББА відбувається суттєве зменшення летальності на 34% на тлі зниження ЧСС на 10–15 уд./хв в результаті покращення енергозабезпечення серця, збільшення коронарного кровотоку за рахунок подовження діастоли і підвищення активності парасимпатичної НС, що позитивно впливає на ремоделювання серця під впливом зменшення токсичного впливу катехоламінів. Поряд з цим ББА зменшують РСС в результаті підвищення електричної стабільності міокарда, зниження активності симпатичної і підвищення активності парасимпатичної НС.
Серцеві глікозиди зменшують ЧСС, задишку, набряки, збільшують діурез, ФВ, але суттєво не знижують смертність, хоча покращують якість життя. Серцеві глікозиди застосовуються у хворих на ХСН у поєднанні з ФП.
Фармакологічна дія серцевих глікозидів:
- підвищення скоротливої функції — позитивна інотропна дія;
- зниження ЧСС — негативна хронотропна дія;
- уповільнення провідності в AV-з’єднанні — негативна дромотропна дія;
- підвищення збудливості — негативна батмотропна дія;
- опосередкована і пряма діуретична дія.
Протипоказання для призначення серцевих глікозидів:
- брадикардія (ЧСС <55 уд./хв);
- AV-блокада ≥ І ступеня;
- гострий ІМ і нестабільна стенокардія;
- шлуночкові екстрасистоли;
- синдроми WPW, слабкості синусного вузла і Морганьї — Адамса — Стокса;
- гіпокаліємія і ХНН; мікседема;
- всі прояви дигіталісної інтоксикації.
Івабрадин показаний пацієнтам із синусовим ритмом та ФВ ЛШ <35%, в яких ЧСС лишається не нижче 70 уд./хв на фоні прийому оптимізованої рекомендованої схеми фармакотерапії, та включає іАПФ (за непереносимості — БРА), ББА у максимально переносимих дозах та АМР. Призначення івабрадину також може бути розглянуто у пацієнтів із ХСН, синусовим ритмом та ФВ ЛШ <35%, в яких ЧСС лишається не менше 70 уд./хв, які отримують іАПФ (або БРА), АМР (або БРА), але не переносять ББА. Івабрадин — інгібітор Іf-каналів синусового вузла при СН сприяє покращенню насосної функції серця та діє виключно на зниження ЧСС, в результаті чого серце ефективніше розслабляється і скорочується. Отже, сприяючи ефективному розслабленню та скороченню ЛШ, івабрадин, на відміну від ББА, яким притаманний негативний інотропний ефект, достовірно:
- збільшує УО, зберігає серцевий викид та збільшує ФВ ЛШ;
- знижує ризик повторних госпіталізацій при СН та серцево-судинну смертність на 18–26% (дослідження ШИФТ, 2010).
Триметазидин. Згідно з останніми європейськими та українськими рекомендаціями з діагностики та лікування ХСН, у пацієнтів із СН і стенокардією триметазидин, якщо його додають до ББА, посилює позитивні ефекти терапії, зокрема при СН зі зниженою ФВ ЛШ, зменшує ФК СН, збільшує тривалість фізичного навантаження та покращує функцію ЛШ. Застосовується у комплексному лікуванні при ІХС.
Препарати заліза в/в, а саме карбоксимальтоза, можуть бути розглянуті у симптомних пацієнтів з ХСН та ФВ ЛШ <40%, які мають лабораторні ознаки залізодефіциту (феритин у сироватці крові <100 мкг/л або феритин у сироватці крові 100–299 мкг/л у поєднанні з насиченням трансферину залізом <20%), з метою зменшення вираженості клінічної симптоматики, поліпшення переносимості фізичних навантажень та покращення якості життя.
Омега-3-ПНЖК. Їх призначення з метою зниження ризиків смерті та госпіталізації з серцево-судинних причин може бути розглянуте у пацієнтів із симптомною (NYНА II–IV ФК) СН зі зниженою ФВ, які отримають іАПФ (або БРА), ББА та АМР.
Медикаментозне лікування пацієнтів із СН зі збереженою ФВ. Єдиного стандарту лікування цих хворих не існує. Принциповий алгоритм допомоги передбачає адекватне лікування (фармакологічне або хірургічне) основного захворювання.
Інгібітори неприлізину/БРА — ферменту, що викликає розпад натрійуретичного пептиду, брадикініну, адреномедуліну та інших вазоактивних пептидів, які перешкоджають розвитку вазоконстрикції, затримці натрію та ремоделюванню серця і судин. Рекомендовано призначати сакубітрил/валсартан замість іАПФ для лікування пацієнтів із СН зі зниженою ФВ.
Пероральні антикоагулянти показані таким категоріям пацієнтів із ХСН:
а) з постійною, персистуючою та пароксизмальною формами ФП за наявності факторів ризику тромбоемболій із сумою балів за шкалою СНА2DS2VASс >1;
б) з перенесеним епізодом артеріальної тромбоемболії будь-якої локалізації чи венозної тромбоемболії;
в) з візуалізованим(-ими) тромбом(-ами) у будь-якій з порожнин серця — лише непрямі пероральні антикоагулянти (АВК);
г) з неоперованим мітральним стенозом — лише непрямі пероральні антикоагулянти;
д) з протезованими клапанами серця — лише непрямі пероральні антикоагулянти.
Прийом непрямих антикоагулянтів (АВК варфарину) повинен супроводжуватися регулярним моніторингом МНВ, яке має підтримуватися у межах 2,0–3,0, а у хворих із протезованими клапанами серця — 2,5–3,5. Лікування НОАК (інгібітори Ха-фактора), на відміну від варфарину, не потребує лабораторного контролю показників згортання крові, але має здійснюватися з урахуванням стану ниркової функції та віку пацієнта, згідно з інструкціями для їх застосування.
Антитромбоцитарні засоби. АСК (75–100 мг/добу) та клопідогрель — в комбінації чи окремо — показані пацієнтам із ХСН на фоні ІХС з ГКС, перкутанними втручаннями, стенокардією, перенесеним ІМ — відповідно до чинних стандартів лікування зазначених категорій пацієнтів.
У практичній роботі лікаря-кардіолога і терапевта часто бувають хворі, резистентні до діуретиків. Тактика застосування діуретиків у лікуванні цих пацієнтів наведена в алгоритмі 2.98.
|
Алгоритм 2.98. Тактика застосування діуретиків при резистентній формі ХСН [17] Крок 1. Лікування одним діуретиком у середніх терапевтичних добових дозах:
Крок 2. Лікування одним діуретиком у максимальній добовій дозі:
Для підвищення ефективності лікування фуросемід, торасемід застосовують одночасно перорально, в/в або в/м. Крок 3. Комбіноване застосування діуретиків перорально і парентерально:
Крок 4. Комбіноване застосування діуретиків з іншими препаратами:
|
Схема лікування при резистентній формі ХСН шляхом корекції патогенетичних факторів представлена в алгоритмі 2.99.
|
Алгоритм 2.99. Лікування при резистентній формі ХСН шляхом корекції патогенних факторів [17] Крок 1. Зменшення перед- і постнавантаження серця:
Крок 2. Зменшення перед- і постнавантаження та набрякового синдрому Комбінація іАПФ з діуретиками (еналаприл, гідрохлоротіазид + еналаприл, гідрохлоротіазид + лізиноприл). Крок 3. Корекція змін переднавантаження серця, набрякового синдрому та порушень нейрогуморальних систем:
Крок 4. Комбіноване лікування при резистентній формі ХСН призначенням серцевих глікозидів при ФП:
Крок 5. Ізольована ультрафільтрація крові. Штучне серце. Трансплантація серця. |
Детально тактика лікування при резистентній формі СН при різних патологічних станах відображена в табл. 2.161.
Таблиця 2.161. Практичні рекомендації щодо лікування петльовими діуретиками
|
Проблема |
Тактика застосування препаратів |
|
Гіпокаліємія/гіпомагніємія |
|
|
Гіпонатріємія |
|
|
Гіперурикемія/ подагра |
|
|
Гіповолемія/ дегідратація |
|
|
Недостатня відповідь або резистентність до діуретика |
|
|
Ниркова недостатність (надмірний рівень сечовини/азоту сечовини і/або креатиніну) |
|
Актуальним є питання лікування при ХСН залежно від різних стадій розвитку захворювання (табл. 2.162).
Таблиця 2.162. Сучасні методи лікування при різних стадіях ХСН
|
Медикаментозні та інші методи лікування |
Стадії ХСН за класифікацією |
|||
|
І |
ІІА |
ІІБ |
ІІІ |
|
|
іАПФ (еналаприл, каптоприл, раміприл, лізиноприл, периндоприл) |
++ |
++ |
++ |
++ |
|
БРА (кандесартан, лозартан і валсартан; при неперенесенні — іАПФ) |
++ |
++ |
++ |
++ |
|
ББА (карведилол, бісопролол, метопрололу сукцинат, небіволол) |
+ |
++ |
++ |
++ |
|
АМР (спіронолактон, еплеренон) |
– |
+ |
++ |
++ |
|
Діуретики — при набряковому синдромі |
– |
+ |
++ |
++ |
|
Серцеві глікозиди (дигоксин — при ФП та синусовому ритмі з ФВ <30%) |
– |
+ |
++ |
++ |
|
Антикоагулянти (ривароксабан, апіксабан, варфарин — при ФП, тромбах у порожнинах серця, штучних клапанах серця) |
++ |
++ |
++ |
++ |
|
Статини (при ХСН ішемічного походження) |
++ |
++ |
++ |
++ |
|
ІКД (після зупинки серця, реанімації, при ФВ <35%, злоякісних шлуночкових аритміях) |
+ |
+ |
++ |
++ |
|
Ресинхронізація (трикамерна стимуляція серця) (при ФВ <35% та QRS >120 мс) |
– |
– |
+ |
+ |
|
Хірургічні методи лікування (трансплантація серця, штучний ЛШ, зовнішній каркас) |
– |
– |
+ |
+ |
Примітки: 1. + лікування показане; ++ лікування особливо необхідне. 2. Результати РКД не підтверджують ефективність статинів при ХСН (ESC, 2012).
Схему комбінованого лікування при рефрактерній ХСН різних стадій наведено в табл. 2.163, лікарські засоби (або їх комбінації), які здатні завдати шкоди пацієнтам, — в табл. 2.164.
Таблиця 2.163. Комбіноване лікування при різних стадіях рефрактерної ХСН
|
Комбінації препаратів |
Стадії ХСН за класифікацією |
|||
|
І |
ІІА |
ІІБ |
ІІІ |
|
|
іАПФ + діуретики + триметазидин |
+ |
++ |
++ |
|
|
БРА + діуретики+ триметазидин |
+ |
++ |
++ |
|
|
іАПФ + ББА + триметазидин |
+ |
+ |
++ |
++ |
|
БРА + ББА |
+ |
+ |
++ |
++ |
|
іАПФ + ББА + івабрадин |
+ |
++ |
++ |
|
|
БРА + ББА + АМР + триметазидин |
+ |
++ |
++ |
|
|
іАПФ + ББА + ААП + діуретик + триметазидин |
+ |
++ |
++ |
|
|
БРА + ББА + АМР + діуретик + триметазидин |
+ |
++ |
++ |
|
Примітки: + лікування показане; ++ лікування необхідне.
Таблиця 2.164. Лікарські засоби (або їх комбінації), які здатні завдати шкоди пацієнтам із маніфестною (ІІ–ІV ФК) ХСН зі зниженою ФВ ЛШ (ВАКУ, 2018) [60]
|
Рекомендації |
Клас рекомендацій |
|
Не рекомендовано призначати тіазолідиндіони (глітазони) пацієнтам із СН, оскільки ці засоби підвищують ризик погіршення перебігу СН і потребу в госпіталізації з цього приводу |
ІІІ |
|
Не рекомендовано призначати НПЗП або інгібітори ЦОГ-2 пацієнтам із СН, оскільки такі засоби підвищують ризик погіршення перебігу СН і потребу в госпіталізації з цього приводу |
ІІІ |
|
Не рекомендовано призначати дилтіазем або верапаміл пацієнтам із СН зі зниженою ФВ, оскільки ці засоби підвищують ризик погіршення перебігу СН і потребу в госпіталізації |
ІІІ |
|
Не рекомендовано додавати БРА (або інгібітор реніну) до комбінованого лікування іАПФ з АМР у пацієнтів із СН, оскільки це підвищує ризик розвитку ниркової дисфункції та гіперкаліємії |
ІІІ |
Незначні порушення функцій серця можна компенсувати медикаментами, однак, на жаль, серцеві препарати не можуть повністю відновити орган або зупинити подальше погіршення роботи серцевого м’яза і стінок серця. Коли медикаментозна терапія безсила, залишається остання надія — трансплантація. У світі широко використовується альтернатива донорському серцю — механічне (штучне) серце, яке вже імплантовано понад 5000 пацієнтів. Левову частку цих операцій виконано в Німеччині. Інновацію, яка успішно використовується в Європі, в Україні поки що застосовано лише раз, адже вартість механічного пристрою становить близько 100 тис. євро.
Трансплантація серця (ВАКУ, 2018) [60]
Показання та протипоказання до трансплантації серця наведено в табл. 2.165.
Таблиця 2.165. Трансплантація серця: показання і протипоказання
|
Показання та умови |
|
|
Протипоказання |
|
Ресинхронізаційна терапія [60]
Імплантація пристрою ресинхронізації шлуночків показана пацієнтам із ХСН, синусовим ритмом та ФВ ЛШ <40%, у яких тривалість комплексу QRS ≥130 мс за його морфології, що відповідає БЛНПГ, а також може бути розглянута в аналогічної категорії пацієнтів за тривалості комплексу QRS ≥150 мс при морфології останнього, що не відповідає графіці лівої ніжки пучка Гіса. Окрім цього, у пацієнтів зі зниженою ФВ ЛШ цьому підходу має надаватися перевага перед рутинною постійною правошлуночковою стимуляцією, якщо остання показана у зв’язку з AV-блокадою.
ІКД
ІКД показано з метою вторинної профілактики РСС пацієнтам, які перенесли епізод шлуночкової аритмії з нестабільною гемодинамікою, за умови їх очікуваного прогнозу виживаності >1 року у задовільному стані. ІКД також показано з метою первинної профілактики РСС пацієнтам із ХСН ІІ–ІІІ ФК за NYHA та ФВ ЛШ <35% за умови отримання ними оптимальної терапії впродовж останніх 3 міс та очікуваного прогнозу виживаності >1 року у задовільному функціональному стані, якщо етіологічним чинником ХСН є ІХС (крім пацієнтів, які перенесли ІМ менше ніж 40 днів тому) або ДКМП.
Серцевий глікозид дигоксин застосовують при ФП лише у разі відсутності ефекту від іАПФ, ББА і діуретиків, а спіронолактон — при ХСН ІІІ–ІV ФК. Хворі на ХСН обов’язково повинні зберігати такі посильні фізичні навантаження, як ходьба, оскільки більшість симптомів декомпенсації серця значно посилюються при детренуванні.
При рефрактерній СН за відсутності артеріальної гіпотензії тимчасово призначають сильні інотропні препарати (допамін, добутамін) або периферичний венодилататор нітропрусид натрію чи нітрогліцерин. Фонову терапію ББА, як правило, продовжують. Цим пацієнтам показане застосування левосимендану.
Особливості лікування при ХСН у пацієнтів похилого віку:
- застосування іАПФ або БРА у нижчих дозах, ніж у осіб молодого віку;
- застосування ББА, особливо з вазодилатуючою дією (карведилол, небіволол), досить добре переноситься хворими похилого віку;
- використання тіазидних діуретиків часто буває неефективним у зв’язку зі зниженою швидкістю клубочкової фільтрації;
- хворі на СН похилого віку можуть бути чутливішими до побічних реакцій дигоксину, ніж особи молодого віку;
- лікування івабрадином пацієнтів віком від 75 років починають з нижчої початкової дози — 2,5 мг двічі на добу;
- пацієнтам віком від 75 років з обережністю призначають триметазидин;
- при підвищеному рівні креатиніну в крові рекомендується починати терапію з низьких доз дигоксину.
Результати РКД з доказової медицини
За даними РКД, застосування неглікозидних інотропних засобів (добутамін, допамін, ібопамін, пімомедан) на тлі іАПФ та діуретиків призвело до зростання смертності при ХСН на 26–80%, що свідчить про недоцільність застосування стратегії «батога» при лівошлуночковій СН (!).
У РКД з доказової медицини повідомляється, що при застосуванні іАПФ і БРА у хворих на ХСН після ІМ спостерігається суттєве підвищення виживаності хворих (на 18–40%), зниження ризику повторного ІМ на 19–25%, що свідчить про необхідність обов’язкового їх застосування цими пацієнтами. При ХСН подовжують тривалість життя іАПФ, БРА і ББА, однак найкращий результат щодо цього дає застосування комбінації іАПФ з ББА карведилолом (!).
У РКД RALES доведено, що АМР спіронолактон при ХСН достовірно покращує прогноз, знижує смертність, перешкоджає прогресуванню ХСН і знижує частоту повторних госпіталізацій до стаціонару.
РКД довели, що пролонговані нітрати на тлі іАПФ або без застосування останніх не покращують прогнозу, а частіше, навпаки, підвищують смертність порівняно із хворими, які приймали іАПФ без нітратів. Єдиним винятком із цього правила є хворі на стенокардію, яким нітрати показані (!).
Застосування препаратів ендотеліну-1 (бозентан, тезозентан, енразентан), а також інгібіторів вазопептидаз (омапатрилату) та антагоністів імунозапальної активації не призвело до покращення прогнозу хворих на ХСН, тому ці препарати виключені з клінічної практики.
Вивчалася порівняльна ефективність різних діуретиків при ХСН. У РКД TORІС показано, що торасемід при ХСН більш сприятливо впливає на прогноз, ніж фуросемід (!).
У хворих із термінальною ХСН терапія іАПФ і ББА діє сприятливо, як і у хворих з декомпенсацією серця легкого та помірного ступеня тяжкості. При термінальній стадії ХСН у пацієнтів відзначають особливо високий ризик розвитку артеріальної гіпотензії та ХНН після застосування іАПФ чи ризик декомпенсації ХСН після застосування ББА. Саме тому при резистентній стадії ХСН ці препарати слід призначати обережно. іАПФ і ББА не слід застосовувати, якщо САТ у хворого <80 мм рт. ст. чи визначаються ознаки периферичної гіпоперфузії. Крім того, ББА не призначають хворим із вираженим набряковим синдромом. Терапію іАПФ і ББА розпочинають з дуже низьких доз. Поряд із цим клінічні дослідження з лізиноприлом та карведилолом показали, що навіть у низьких дозах ці препарати можуть бути корисними при лікуванні пацієнтів із резистентною формою ХСН. У літературі є докази, що АМР спіронолактон збільшує тривалість життя та знижує ризик госпіталізації у хворих із термінальною стадією ХСН зі збереженою функцією нирок.
За останні 30 років здійснено декілька тривалих проспективних досліджень з визначенням ефективності застосування ББА при ХСН. Основними з-поміж них є дослідження карведилолу в США, СІBІS-ІІ (бісопролол), СOPERNІСUS (карведилол). Усі ці дослідження були припинені раніше наміченого терміну, оскільки в усіх випадках спостерігалося покращення ФК СН, збільшення ФВ, зниження смертності та збільшення виживаності хворих. Таким чином, при ХСН ББА за ефективністю перевершують усі інші препарати, в тому числі іАПФ (!). ББА призначають при ХСН ІІ–ІІІ ФК, а доцільність їх застосування при ІV ФК ще остаточно не з’ясована. Застосування ББА рекомендують після стабілізації стану хворого через 2–3 міс. Після застосування ББА спостерігається позитивна динаміка, а максимальний ефект визначається через 6–9 міс.
Існують два захворювання, при яких ББА рутинно використовують не лише при ХСН, але й при ГСН: мітральний стеноз та ГКМП. Позитивну дію ББА у цих випадках пояснюють сповільненням ЧСС і збільшенням тривалості діастоли, діастолічного наповнення серця та зменшенням сили скорочення шлуночків. У результаті цих змін відбувається збільшення серцевого викиду, зменшення венозного застою крові в легенях та клінічне покращення.
Якщо провідними клінічними симптомами є задишка при фізичному навантаженні, ортопное і набряк легень, то найефективнішими є іАПФ, венозні дилататори та діуретики (чи їх поєднання). При ХСН ІІА стадії призначають гіпотіазид, ІІБ стадії — торасемід чи фуросемід, які застосовують у мінімальних дозах. Однак у період активної діуретичної терапії добовий діурез не повинен перевищувати 2–2,5 л/добу, оскільки надмірна діуретична терапія призводить до рефрактерного набрякового синдрому. При надмірній діуретичній терапії позаклітинна рідина не встигає перейти в судинне русло, різко падає ОЦК, тому виникає гіповолемія.
Лікування при ХСН залежно від вираженості дисфункції ЛШ наведено в табл. 2.166. Диференційоване лікування систолічної та діастолічної ХСН — алгоритм 2.100.
Таблиця 2.166. Диференційоване лікування при ХСН залежно від вираженості дисфункції ЛШ
|
Вираженість ХСН |
Фармакологічні препарати |
|
Безсимптомна дисфункція ЛШ |
1. іАПФ чи БРА. 2. ББА при перенесеному ІМ чи івабрадин при ЧСС >70 уд./хв. 3. АМР при ІМ, що виник нещодавно. 4. Триметазидин. 5. Серцеві глікозиди при ФП |
|
ХСН ІІ ФК за NYHA |
1. іАПФ чи БРА. 2. Діуретики при набряковому синдромі. 3. ББА чи івабрадин при ЧСС >70 уд./хв. 4. АМР при ІМ, що виник нещодавно. 5. Триметазидин. 6. Серцевий глікозид дигоксин при ФП |
|
ХСН ІІІ ФК за NYHA |
1. іАПФ чи БРА. 2. Діуретики в різних комбінаціях. 3. ББА чи івабрадин при ЧСС >70 уд./хв. 4. АМР. 5. Триметазидин. 6. Серцевий глікозид дигоксин при ФП |
|
ХСН IV ФК за NYHA, тяжка форма |
1. іАПФ у поєднанні з БРА як виняток. 2. Діуретики в різних комбінаціях. 3. ББА чи івабрадин при ЧСС >70 уд./хв. 4. АМР. 5. Триметазидин. 6. Серцевий глікозид дигоксин при ФП |
|
Алгоритм 2.100. Диференційне лікування при систолічній та діастолічній ХСН [17, 60] Крок 1. Лікування при систолічній ХСН:
Крок 2. Лікування діастолічної ХСН при окремих захворюваннях Збереження синусового ритму та зниження ЧСС до 50 уд./хв, що супроводжується подовженням діастоли:
|
Примітка. При діастолічній дисфункції міокарда недостатньо обґрунтоване лікування може бути більш небезпечним, ніж відсутність лікування.
Фармакотерапія при термінальній ХСН з метою зниження смертності і розвитку ускладнень:
- іАПФ або БРА, ББА, АМР.
Контроль симптомів:
- діуретики (петльові та тіазидні);
- серцеві глікозиди (в низьких дозах при ФП);
- антиішемічний препарат триметазидин.
Симптоматична терапія: короткотермінове застосування неглікозидних інотропних засобів.
Одним із новітніх методів лікування при ХСН є пересадка в міокард мезенхімальних стовбурових клітин з метою покращення скоротливої здатності серця. При ССЗ уже через 1 міс після трансплантації стовбурових клітин спостерігається покращення регіонарної перфузії та діастолічної функції ЛШ, покращення якості життя та стійкості до фізичних навантажень. Цей безпечний метод лікування можна використовувати у хворих, які чекають на проведення трансплантації серця, або для підготовки хворих на ХСН до реконструктивної операції на власному серці, а також до заміщення післяінфарктного фіброзного поля життєздатними кардіоміоцитоподібними клітинами. Отже, введення стовбурових клітин кісткового мозку в серце є ефективним методом лікування ХСН.
До препаратів, що не рекомендується застосовувати для лікування при ХСН, належать:
1. НПЗП (селективні та неселективні, а також АСК у дозі 325 мг/добу). Особливо не варто комбінувати НПЗП з іАПФ, БРА, діуретиками та АМР, оскільки відбувається значне зниження клінічної ефективності останніх і збільшується затримка рідини в організмі, що спричиняє розвиток набряку легень. АСК в низькій дозі (75 мг/добу), згідно з рекомендаціями доказової медицини, теж краще не призначати, оскільки це спричиняє наростанню ознак ХСН.
2. ГК, оскільки вони спричиняють затримку натрію в організмі людини, наростанню набрякового синдрому, підвищенню АТ.
3. ААП І класу — вони суттєво пригнічують скоротливу здатність серця, спричиняють прогресування ХСН і чинять проаритмічний ефект.
4. АК (верапаміл, дилтіазем та короткодіючі дигідропіридини) теж пригнічують інотропну функцію серця і спричиняють наростання ознак декомпенсації серця. Однак амлодипін мало пригнічує скоротливу здатність серця, і при ХСН на фоні АГ його застосовувати можна, особливо в комбінації з іАПФ або БРА.
5. Трициклічні антидепресанти активують симпатичну НС, спричиняють розвиток аритмій, ФШ та прогресування СН.
Фактори, що погіршують прогноз СН:
1. Похилий вік.
2. Зниження ФВ ЛШ <25%, а КДР >65 мм.
3. Рестриктивний тип діастолічної дисфункції, дилатація ЛП і збільшення пульсового АТ.
4. Аритмії: ФП, тахікардія; зниження варіабельності серцевого ритму.
5. Анемія.
6. Ознаки ішемії периферичних аритмій.
7. ХНН (кліренс креатиніну <60 мл/хв).
8. Стійкий резистентний до лікування набряковий синдром.
9. Високий рівень мозкового натрійуретичного гормону, маркерів некрозу міокарда і нейрогуморальної активації (тропоніни, норепінефрин, цитокіни, ендотелін-1, ангіотензин ІІ).
10. Асинхронність скорочення ЛШ (QRS >130 мс), повна БЛНПГ.
11. Депресія.
12. Дихання Чейн — Стокса.
13. Неадекватне лікування при ЦД.
Найвагоміші предиктори, які впливають на прогноз СН:
1. Демографічні ознаки: похилий вік, ішемічна етіологія, оживлення після РСС.
2. Клінічні ознаки: артеріальна гіпотензія, СН ІІІ–ІV ФК за NYHA, нещодавня госпіталізація з приводу СН.
3. Електрофізіологічні предиктори: широкий комплекс QRS, шлуночкові аритмії (менше значення мають тахікардія, Q-зубець, ГЛШ).
4. Функціональні (Exertіonal) предиктори: низький піковий VO2 (менше значення має зниження толерантності до фізичного навантаження).
5. Лабораторні предиктори: підвищення BNP|NT-proBNP, гіпонатріємія, підвищення тропонінів, збільшення кількості біомаркерів, нейрогуморальна активація.
6. Інструментальні предиктори: низька ФВ ЛШ (≤45%). Показники очікуваної низької виживаності у хворих на ХСН — табл. 2.167.
Таблиця 2.167. Показники очікуваної низької виживаності у хворих на ХСН
|
Клініко-демографічні |
Інструментальні |
Лабораторні |
|
|
|
Профілактика ХСН полягає в тривалому застосуванні іАПФ, БРА, ББА, діуретиків і серцевих глікозидів при постійній ФП на тлі активної терапії основного захворювання.
Відомо, що хворі на ХСН приблизно у 50% випадків помирають від РСС. З метою профілактики РСС у цих хворих доказова медицина рекомендує такі заходи:
1. Застосування ББА.
2. Застосування іАПФ, БРА, АМР (еплеренон, верошпірон), що призводить до зменшення шлуночкової екстрасистолії, ШТ. Допоміжне призначення АМР до іАПФ, БРА і ББА знижує ризик аритмічних ускладнень та покращує прогноз хворих на ХСН і з дисфункцією ЛШ.
3. Аміодарон при резистентній ХСН не знижує ризик РСС, тому його не слід призначати цим пацієнтам, а при ХСН ІІІ–ІV ФК він може навіть підвищувати ризик смерті за рахунок аритмогенної дії (!).
4. Застосування ІКД має позитивний ефект, знижує ризик РСС, однак це не заміна антиаритмічної терапії, а ефективне доповнення до неї. Оптимальним є поєднання ІКД із терапією ББА, що значно ефективніше запобігає виникненню РСС.
5. При ХСН ББА разом із блокаторами РААС (іАПФ, БРА, АМР, триметазидин) залишаються засобом вибору в профілактиці РСС.
Актуальним є питання профілактики РСС (ФШ, «пірует»-тахікардії, шлуночкової екстрасистолії ІІІ–V градації) при різних стадіях ХСН (табл. 2.168).
Усі наведені препарати при ХСН мають виражену антифібриляторну, антиаритмічну, нейрогуморальну модулюючу дію, тому вони знижують розвиток РСС (ФШ, «пірует»-тахікардії, шлуночкової екстрасистолії ІІІ–ІV градації за Лауном).
Важливу роль у лікуванні та профілактиці ХСН відіграє фізична реабілітація пацієнтів, яка рекомендується всім пацієнтам із ХСН І–ІV ФК на фоні стабільного перебігу декомпенсації, коли немає потреби екстрено застосовувати діуретики та інотропні засоби.
Таблиця 2.168. Профілактика РСС на різних стадіях ХСН
|
Засоби профілактики РСС |
Стадії ХСН за класифікацією Стражеска — Василенка |
|||
|
І |
ІІА |
ІІБ |
ІІІ |
|
|
ББА |
+ |
+ |
++ |
++ |
|
Аміодарон |
+ |
+ |
||
|
АМР |
+ |
+ |
+ |
|
|
ББА + аміодарон |
+ |
+ |
||
|
іАПФ |
++ |
++ |
++ |
++ |
|
БРА |
++ |
++ |
++ |
++ |
|
Триметазидин |
++ |
++ |
++ |
++ |
|
Івабрадин |
++ |
++ |
++ |
++ |
Примітки: + — лікування показане; ++ — лікування особливо необхідне.
Протипоказання до фізичної реабілітації:
- напади стенокардії у пацієнтів із низькою ФВ ЛШ;
- активний міокардит;
- стеноз клапанних отворів;
- ціанотичні вроджені вади;
- порушення ритму високої градації.
Фізична реабілітація повинна бути контрольованою; її слід широко застосовувати у кардіологічній практиці.
