Атеросклероз
ССЗ посідають перше місце серед причин смерті. У розвитку кардіології в Україні, Росії та інших країнах світу величезну роль відіграли такі знамениті кардіологи, як В.П. Образцов, М.Д. Стражеско, О.Л. Мясніков, Є.І. Чазов, Л.Т. Мала, Е. Браунвальд, кардіохірурги К. Бернардт, М.М. Амосов та багато інших вчених. У США від ССЗ щохвилини помирають двоє людей. Дуже поширеним захворюванням є атеросклероз.
Визначення. Атеросклероз (від грецьких слів athere — кашка, sсlerosіs — твердий) — це хронічне хвилеподібне захворювання, що характеризується виникненням у стінці артерій вогнищ ліпідної інфільтрації запалення та розростанням сполучної тканини з утворенням фіброзних бляшок, які звужують просвіт судини і порушують фізіологічну функцію уражених артерій, що призводить до порушень кровообігу. Атеросклероз — це епідемія ХХ і ХХІ століть. На це захворювання здебільшого страждають люди зрілого і похилого віку, хоча воно виникає і в 10–15-річних дітей та підлітків. Зазначимо, що наявність атеросклерозу, незалежно від його локалізації, суттєво впливає на тривалість життя. За результатами Фремінгемського дослідження, наявність в анамнезі цереброваскулярного захворювання зменшує тривалість життя на 17,4 року, перенесеного інфаркту міокарда (ІМ) — на 9,2 року, ішемічного інсульту — на 12 років.
Етіологічні фактори ризику атеросклерозу:
- АГ;
- тютюнопаління;
- ожиріння;
- дисліпідемії (підвищення вмісту в крові холестерину (ХС), тригліцеридів (ТГ), атерогенних ліпопротеїнів низької щільності (ЛПНЩ) та/чи зниження вмісту антиатерогенних ліпопротеїнів високої щільності (ЛПВЩ));
- спадкова схильність;
- порушення вуглеводного обміну (гіперглікемія, цукровий діабет (ЦД));
- гіподинамія;
- вік старше 50–60 років;
- стать (чоловіки);
- гіпергомоцистеїнемія;
- нераціональне харчування (вживання великої кількості жирів і вуглеводів) тощо.
Такі фактори, як тютюнопаління, гіподинамія та харчові звички, стосуються способу життя: вони можуть бути модифіковані (піддаються корекції). Модифіковані фактори ризику — підвищення рівня АТ, ЦД 2-го типу і дисліпідемії. Вік і чоловіча стать, спадковість належать до немодифікованих факторів ризику.
Основні фактори, патогенетичні ланки розвитку атеросклерозу
Розрізняють такі основні фактори розвитку атеросклеротичної бляшки (атерогенез):
- Ураження ендотелію артерії з розвитком дисфункції;
- Утворення ліпідних плям і смужок (стадія ліпоїдозу);
- Утворення фіброзної бляшки (стадія ліпосклерозу);
- Утворення ускладнень атеросклеротичної бляшки;
- Гостре чи хронічне запалення стінки артерії;
- Кількісні та якісні порушення ліпідного обміну;
- Генетичні фактори: збільшення генів аполіпопротеїнів (апо-) та генів ферментів.
Розглянемо їх детальніше:
1. При атеросклерозі виникає ендотеліальна дисфункція зі збільшенням синтезу вазопресорів: тромбоксану А2, ендотеліну-1, ангіотензину ІІ; зменшення утворення вазодилататорів: простацикліну, оксиду азоту тощо. Головними чинниками ушкодження ендотелію судин є АГ, тютюнопаління та дисліпідемія.
2. Ліпідні плями на аорті утворюються із пінистих клітин, які вміщують велику кількість ліпідів і Т-лімфоцитів. Ліпідні смужки дещо виступають над поверхнею ендотелію. Вони складаються із макрофагів, лімфоцитів, гладком’язових і пінистих клітин, в які входять ліпіди. Ліпідні плями та смужки утворюються в результаті відкладання ліпідів в інтимі артерій.
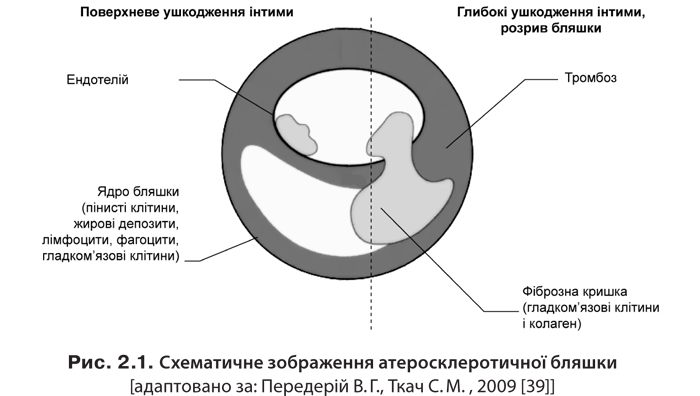
3. Утворення фіброзної бляшки відбувається в результаті патологічного процесу у вогнищах відкладання ліпідів та розростання молодої сполучної тканини, що веде до утворення ліпідного ядра. Навколо нього виникає зона сполучної тканини, багатої на клітинні елементи (макрофаги, пінисті та гладком’язові клітини, Т-лімфоцити), колагенові та еластичні волокна. З дозріванням сполучної тканини кількість клітинних елементів зменшується, а колагенові волокна потовщуються і формують сполучнотканинний каркас атеросклеротичної бляшки з утворенням «покришки», що відділяє ліпідне ядро від просвіту судини. Формується фіброзна бляшка, яка спричиняє зменшення просвіту судини та порушення кровообігу.
4. Формування ускладненої атеросклеротичної бляшки відбувається внаслідок прогресування атероматозного процесу. Відбувається значне збільшення ліпідного ядра, підвищення агрегації тромбоцитів, розвиток крововиливів у бляшку, стоншення її фіброзної капсули та руйнування покришки з утворенням тріщин, розривів і атеросклеротичних виразок. На основі виразок утворюються тромби, емболії, а згодом — атерокальциноз (відкладення солей кальцію в атероматозні маси, фіброзні тканини). Головним наслідком формування ускладненої атеросклеротичної бляшки є утворення пристіночного тромбу, який раптово та різко обмежує кровотік в артерії. У цей період формується нестабільна стенокардія, ІМ, ішемічний інсульт тощо.
5. При атеросклерозі відбувається гостре чи хронічне запалення стінки артерії, яке характеризується підвищенням вмісту С-реактивного білка (СРБ), фібриногену, інтерлейкіну-6 тощо.
6. Спостерігаються кількісні та якісні порушення ліпідного обміну.
Схематичне зображення атеросклеротичної бляшки ілюструє рис. 2.1, типи і ступінь атеросклеротичного звуження судини — рис. 2.2.

Класифікація дисліпідемій
На сучасному етапі для характеристики порушень ліпідного спектра крові використовують таку термінологію: дисліпідемія, гіперліпопротеїнемія та гіперліпідемія.
Термін «дисліпідемія» — найширший, оскільки він включає як підвищення рівня ліпідів та ліпопротеїнів вище за оптимальні значення, так і можливе зниження частини ліпідного спектра, а саме ЛПВЩ або альфа-ліпопротеїнів.
Термін «гіперліпопротеїнемія» означає будь-яке підвищення рівня ліпідів і ліпопротеїнів у плазмі крові вище оптимальних значень.
Термін «гіперліпідемія» — найбільш простий, оскільки для його використання досить визначення тільки підвищення ліпідів у крові ХС і ТГ вище оптимальних значень. Для характеристики гіперліпопротеїнемії найбільш уживаною є класифікація ВООЗ (табл. 2.1).
Таблиця 2.1. Класифікація гіперліпопротеїнемій за D. Fredrickson (1970)
|
Фенотип |
ХС у плазмі крові |
ТГ |
Зміни ліпопротеїнів |
Атерогенність |
|
І |
Підвищений |
Підвищені |
Підвищення хіломікронів |
Неатерогенний фенотип |
|
ІІa |
Підвищений |
В нормі |
Підвищення ЛПНЩ |
Висока |
|
ІІb |
Підвищений |
Підвищені |
Підвищення ЛПНЩ |
Висока |
|
ІІІ |
Підвищений |
Підвищені |
Підвищення ЛПНЩ |
Висока |
|
ІV |
Частіше в нормі |
Підвищені |
Підвищення ЛПДНЩ |
Помірна |
|
V |
Підвищений |
Підвищені |
Підвищення хіломікронів та ЛПДНЩ |
Низька |
При атеросклерозі найчастіше виявляють ІІа, ІІb та ІІІ атерогенні типи гіперліпопротеїнемії (табл. 2.2).
Таблиця 2.2. Клінічна класифікація гіперліпопротеїнемій
|
Первинні |
Вторинні |
|
1. Звичайна (полігенна) гіперліпопротеїнемія. 2. Сімейна (частіше моногенна) гіперліпопротеїнемія:
|
Найчастіші причини розвитку: ЦД, зловживання алкоголем, гіпотиреоз, хронічна ниркова недостатність (ХНН), нефротичний синдром, обструктивні захворювання печінки, лікування блокаторами бета-адренорецепторів (ББА), діуретиками, кортикоїдами та ін. |
Клінічна класифікація дисліпідемій (ВАКУ, 2018):
- Гіперхолестеринемія — при ізольованому підвищенні рівня загального ХС >5,0 ммоль/л (>190 мг/дл), що відповідає типу ІІа за D. Fredrickson.
- Сімейна гетерозиготна гіперхолестеринемія: рівень загального ХС >5,0 ммоль/л (<304 мг/дл), ХС ЛПНЩ >5,0 ммоль/л (<190 мг/дл).
- Сімейна гомозиготна гіперхолестеринемія: рівень загального ХС >16–18 ммоль/л (>508–684 мг/дл), ХС ЛПНЩ >13 ммоль/л (>494 мг/дл).
- Комбінована дисліпідемія: при комбіновановому підвищенні рівня загального ХС >5,0 ммоль/л (>190 мг/дл) та рівня ТГ >1,7 ммоль/л (>150 мг/дл), що відповідає типу ІІb та IІІ за D. Fredrickson.
- Гіпертригліцеридемія: при ізольованому підвищенні рівня ТГ >1,7 ммоль/л (>150 мг/дл), що відповідає типу І та IV за D. Fredrickson.
- Легка та помірна гіпертригліцеридемія (гетерозиготна): >1,7 ммоль/л (>150 мг/дл) та <10,0 ммоль/л (885 мг/дл).
- Тяжка гіпертригліцеридемія (гомозиготна): >10,0 ммоль/л (>885 мг/дл) (табл. 2.3).
Таблиця 2.3. Класифікація рівнів загального ХС, ТГ, ХС ЛПНЩ і ХС ЛПВЩ
|
ХС ЛПНЩ |
|
|
<100 мг/дл (<2,6 ммоль/л) |
Оптимальний |
|
100–129 мг/дл (2,7–3,3 ммоль/л) |
Вищий від оптимального |
|
130–159 мг/дл (3,4–4,1 ммоль/л) |
Гранично високий |
|
160–189 мг/дл (4,2–4,9 ммоль/л) |
Високий |
|
>190 мг/дл (>5,0 ммоль/л) |
Дуже високий |
|
Загальний ХС |
|
|
<200 мг/дл (<5,0 ммоль/л) |
Бажаний |
|
200–239 мг/дл (5,1–6,1 ммоль/л) |
Гранично підвищений |
|
>240 мг/дл (>6,2 ммоль/л) |
Високий |
|
ХС ЛПВЩ |
|
|
<40 мг/дл (<1,0 ммоль/л) |
Низький |
|
>60 мг/дл (>1,6 ммоль/л) |
Високий |
|
ТГ |
|
|
<150 мг/дл (<1,7 ммоль/л) |
Нормальний |
|
150–199 мг/дл (1,7–2,2 ммоль/л) |
Гранично високий |
|
200–499 мг/дл (2,3–5,6 ммоль/л) |
Високий |
|
>500 мг/дл (>5,6 ммоль/л) |
Дуже високий |
Класифікація та діагностика атеросклерозу
На жаль, загальноприйнятої клінічної класифікації атеросклерозу в Україні не існує. Нижче наведено Міжнародну класифікацію атеросклерозу (згідно з Міжнародною класифікацією хвороб (МКХ-10)).
Атеросклероз.
Включено:
- артеріолосклероз;
- артеріосклеротична хвороба судин;
- атерома;
- дегенерація:
- артеріальна;
- артеріоваскулярна;
- васкулярна;
- деформуючий або облітеруючий ендартеріїт сенільний:
- артеріїт;
- ендартеріїт.
Виключено:
- церебральний (І67.2);
- коронарний (І25.1);
- мезентеріальний (К55.1);
- легеневий (І27.0).
Атеросклероз аорти (І70.0).
Атеросклероз ниркової артерії (І70.1).
Нирка Гольдблата.
Виключено: атеросклероз ниркових артеріол.
Атеросклероз артерій кінцівок (І70.2):
- Атеросклеротична гангрена.
- Склероз (медіальний) Менкеберга.
Атеросклероз інших артерій (І70.8).
Генералізований і неуточнений атеросклероз (І70.9).
Примітка. Слід зазначити, що атеросклероз — це системне захворювання, і основні етапи атерогенезу не залежать від локалізації процесу (коронарні, церебральні чи інші артерії). Досить часто одночасно ушкоджуються кілька судин з наявністю чи відсутністю відповідних клінічних проявів. Залежно від локалізації атеросклеротичного ураження прояви захворювання можуть бути різними.
Найчастішими є клінічні прояви трьох основних басейнів:
1. ІХС (стенокардія, ІМ, раптова серцева смерть (РСС)).
2. Цереброваскулярна хвороба (транзиторна ішемічна атака, інсульт).
3. Атеросклероз периферичних судин (переміжна кульгавість, гангрена).
Усіх пацієнтів з ознаками атеросклеротичного ураження, незалежно від локалізації, розглядають як групу високого ризику. При цьому атеросклероз церебральних і периферичних артерій, а також ЦД називають еквівалентами ІХС.
Клінічні стандарти діагностики атеросклерозу наведені в алгоритмі 2.1.
|
Алгоритм 2.1. Діагностика атеросклерозу [17] 1. Несприятлива спадковість:
2. Фактори ризику вторинних дисліпідемій:
3. Клінічні критерії порушень ліпідного обміну:
4. Клінічні критерії атеросклерозу залежно від локалізації процесу:
5. В Європейських рекомендаціях з профілактики серцево-судинних захворювань у клінічній практиці (2003) відзначено, що найінформативнішими сучасними методами діагностики атеросклерозу є магнітно-резонансна томографія (МРТ), спіральна комп’ютерна томографія (КТ) і сонографія. |
Клінічні форми атеросклерозу детально описані в посібниках і підручниках. Норми, градації рівня та класифікація ХС, ЛПНЩ і ЛПВЩ наведені в табл. 2.4.
Таблиця 2.4. Норми ліпідного обміну у здорової людини
|
Фракція ліпідів |
Вміст у плазмі крові |
|
|
мг/дл |
ммоль/л |
|
|
Загальний ХС |
<200 |
<5,0 |
|
ТГ |
<150 |
<1,7 |
|
ЛПНЩ |
<100 |
<2,6 |
|
ЛПВЩ (чоловіки) |
>35 |
>1,0 |
|
ЛПВЩ (жінки) |
>40 |
>1,2 |
|
Хіломікрони (натще) |
Сліди |
Сліди |
У пацієнтів з ІХС, периферичним атеросклерозом, атеросклерозом сонних артерій, аневризмою черевного відділу аорти, ЦД рівень загального ХС повинен становити <4,5 ммоль/л (<175 мг/дл), а ХС ЛПНЩ <2,5 ммоль/л (<100 мг/дл). Для визначення атеросклерозу використовують коефіцієнт (індекс) атерогенності, який у чоловіків віком 40–60 років без клінічних проявів атеросклерозу становить 3,0–3,5. Коефіцієнт атерогенності у межах 3,5–4,0 асоціюється з помірним, а >4,0 — з високим ризиком розвитку атеросклерозу.
Запропоновані нові й переглянуто критерії NСER-ATP для встановлення діагнозу метаболічного синдрому. Цей діагноз установлюється за наявності як мінімум 3 із нижченаведених 5 критеріїв:
1. Центральне ожиріння: окружність талії >94 см у чоловіків, >80 см у жінок.
2. Підвищення рівня ТГ ≥1,7 моль/л (≥150 мг/дл).
3. Зниження рівня ХС ЛПВЩ <1,03 ммоль/л (<40 мг/дл) для чоловіків, <1,29 ммоль/л (<50 мг/дл) для жінок.
4. Підвищення АТ: систолічного (САТ) ≥130 мм рт. ст. та/чи діастолічного (ДАТ) ≥85 мм рт. ст., або лікування раніше діагностованої АГ.
5. Підвищення рівня глюкози в крові натще ≥6,1 ммоль/л (≥110 мг/дл), ≥5,6 ммоль/л (≥100 мг/дл) згідно з переглянутими критеріями або раніше діагностований ЦД 2-го типу (табл. 2.5).
Таблиця 2.5. Основні причини розвитку гіпер(дис)ліпідемій і зміни ліпідів крові
|
Підвищення рівня |
Зниження рівня ХС ЛПВЩ |
|
|
ХС ЛПНЩ |
ТГ |
|
|
|
|
Рентгенологічне дослідження дозволяє визначити подовження та розширення аорти, відкладення кальцію в її стінці, інколи — аневризматичне випинання аорти.
За допомогою ультразвукового дослідження (УЗД) визначають розширення аорти, потовщення, ущільнення та кальциноз різних артерій, наявність атеросклеротичних бляшок у стінках судин.
Допплерівське дослідження дозволяє визначити звуження чи оклюзію магістральних судин, прискорення лінійної швидкості крові, зміни індексу пульсації та індексу циркуляторного опору судин.
Найдостовірнішою ознакою звуження магістральної артерії є збільшення максимальної систолічної амплітуди лінійної швидкості кровотоку (Smax) і розширення спектра частот допплерівського сигналу (підвищення індексу спектрального розширення — SB) зі зниженням «вікна». Європейське товариство кардіологів (ЄТК) (2007) для діагностики ІХС і атеросклерозу та гендерних особливостей рекомендує використовувати МРТ, однак значення цього методу для діагностики стенозів КА поки остаточно не з’ясовано. Неінвазивне дослідження сонних артерій і артерій нижніх кінцівок для діагностики атеросклерозу є більш доступним, ніж дослідження коронарних і церебральних артерій. Нещодавно встановлено, що поширеність атеросклерозу артерій сітківки корелює з поширеністю ураження атеросклеротичної бляшки КА, а також зі змінами у плазмі крові загального ХС, ХС ЛПНЩ, ТГ та апопротеїну. Тому простий метод діагностики — офтальмоскопію — можна використовувати для виявлення асимптомних пацієнтів з високим ризиком серцево-судинних подій.
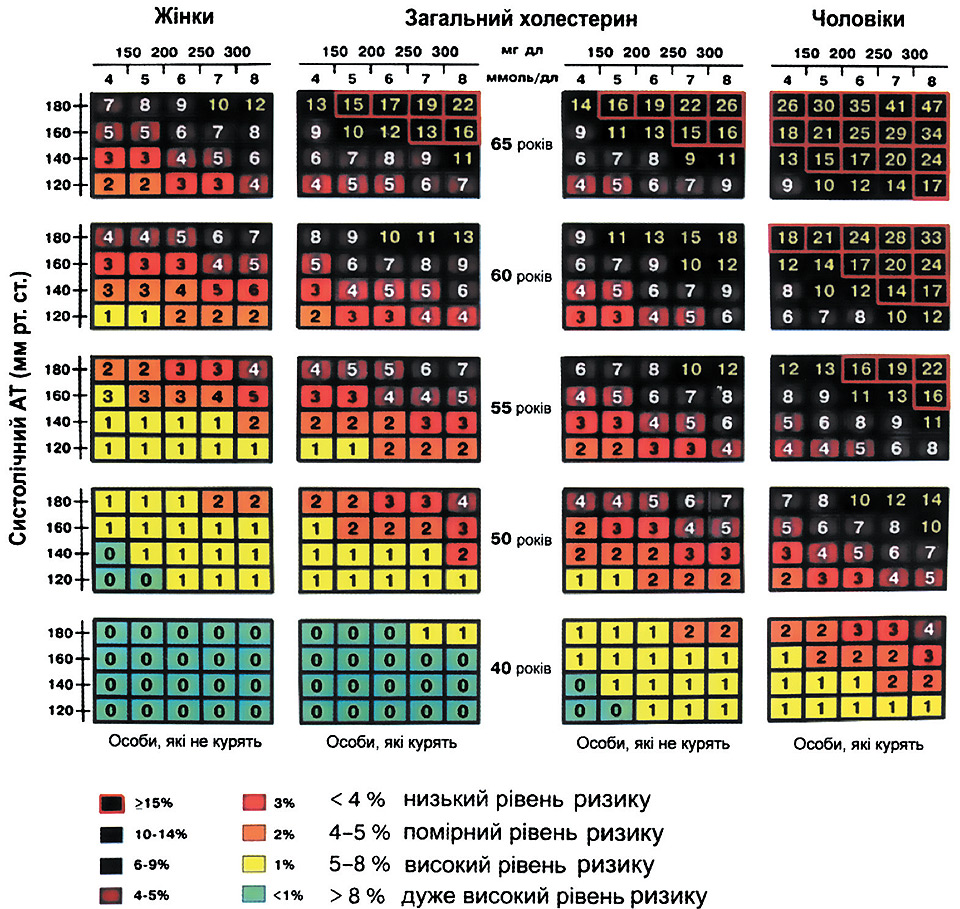
Оцінка 10-річного ризику фатальних ССЗ на основі різних показників наведена у шкалі SCORE (див. кольорову вкл., рис. 13). Розрізняють 4 рівні серцево-судинного ризику, які визначають за шкалою SCORE [60]:
1. Дуже високий ризик характеризується можливістю розвитку ІМ, гострого коронарного синдрому (ГКС), ХНН, інсульту, хвороби периферичних артерій, ЦД 2-го типу. Фатальний ризик ССЗ становить >10.
2. Для високого ризику характерним є підвищення окремих факторів ризику (АГ, сімейна дисліпідемія). Ризик фатальних ускладнень ССЗ упродовж 10 років за SCORE становить ≥5 та <10%.
3. Помірний ризик супроводжується абдомінальним ожирінням, гіподинамією, підвищенням загального ХС, ХС ЛПНЩ, ТГ, зниженням ХС ЛПВЩ, збільшенням рівня фібриногену, гомоцистеїну, СРБ, коли показник SCORE становить >1 та <5% на 10 років.
4. Низький ризик, коли показник SCORE становить <1%.
Рівні загального серцево-судинного ризику
Дуже високий ризик наявний у пацієнтів, які мають:
- документовані ССЗ за даними інвазивного або неінвазивного тестування (коронарної ангіографії, ядерного магнітного резонансу, реєстрації атеросклеротичної бляшки за даними УЗД сонних артерій), ІМ в анамнезі, наявність коронарної реваскуляризації, перкутанне коронарного втручання (ПКВ), аортокоронарного шунтування (АКШ) та інших артеріальних реваскуляризацій; ішемічний інсульт, захворювання периферичних артерій;
- ЦД 2-го типу, 1-го типу з наявністю ураження органа-мішені (наприклад мікроальбумінурія);
- помірна і тяжка ХХН (швидкість клубочкової фільтрації (ШКФ) <60 мл/хв/1,73 м2) — розрахований за допомогою таблиць на 10 років ризик SCORE ≥10%.
Високий ризик наявний у пацієнтів, які мають:
- значне підвищення тільки одного фактора ризику (загальний ХС >8 ммоль/л (>320 мг/дл); ХС ЛПНЩ >6 ммоль/л (>240 мг/дл); АТ >180/110 мм рт. ст.), сімейні дисліпідемії, тяжка АГ — розрахований за допомогою таблиць на 10 років ризик SCORE ≥5 та <10%.
Помірний ризик наявний у пацієнтів, які мають розрахований за допомогою таблиць на 10 років ризик SCORE ≥1 та <5%.
Низький ризик наявний у пацієнтів, які мають розрахований на 10 років ризик SCORE <1%.
У виданих 2011 р. спільних рекомендаціях ЄТК та Європейського товариства з атеросклерозу, присвячених дисліпідеміям, для визначення індивідуального серцево-судинного ризику у цього контингенту пацієнтів запропоновано чотири варіанти таблиці SCORE залежно від рівня ХС ЛПВЩ — 0,8; 1,0; 1,4 та 1,8 ммоль/л.
Шкала SCORE не використовується:
1) у пацієнтів із найвищим ступенем сумарного 10-річного серцево-судинного ризику, які потребують лікування згідно зі стандартами їхньої вторинної профілактики. Це такі пацієнти:
- з доведеними ССЗ атеросклеротичного генезу (ІХС, цереброваскулярні хвороби, аневризма аорти, атеросклероз периферичних артерій);
- з ЦД 1-го і 2-го типу;
- з ураженням органів-мішеней;
- з ХХН;
2) в осіб із дуже високими рівнями окремих факторів ризику (загальний ХС >8 ммоль/л, САТ >180 мм рт. ст.);
3) у осіб віком старше 65 років.
4) у осіб віком до 40 років, незалежно від наявності фактора ризику (за винятком дуже високих рівнів окремих факторів) — вони мають низький абсолютний ризик фатальних серцево-судинних ускладнень у наступні 10 років життя.
Оцінюючи ризик виникнення ускладнень системи кровообігу, слід мати на увазі, що він може бути значно вищим, ніж за шкалою SCORE:
- в осіб із гіподинамією чи ожирінням, особливо центральним;
- у людей із несприятливим щодо ССЗ сімейним анамнезом;
- в осіб із низьким соціальним статусом, тривожними і депресивними станами;
- при порушенні толерантності до глюкози, у хворих на ЦД (наявність ЦД підвищує ризик у 5 разів у жінок і у 3 рази — у чоловіків);
- у людей із низьким умістом ХС ЛПВЩ або з високим рівнем ТГ;
- за наявності ознак субклінічного атеросклерозу за даними УЗД сонних артерій, електронно-променевої чи мультиспіральної КТ;
- коли виявлено гіпертрофію лівого шлуночка (ГЛШ) (за даними ЕКГ або ехоКГ);
- коли підвищені рівні маркерів запалення (СРБ і фібриногену).
Програма лікування при дисліпідемії [60]
Перелік обов’язкових медичних послуг
Пацієнти з дисліпідемією повинні отримувати комплексне лікування (табл. 2.6), що включає:
1. Немедикаментозну терапію (дієта, корекція маси тіла, підвищення фізичної активності, припинення тютюнопаління) для досягнення оптимальних характеристик ліпідного профілю.
2. Медикаментозне лікування відповідно до різних варіантів дисліпідемій:
а) гіперхолестеринемія — статини, езетиміб, можлива їх комбінація;
б) комбінована дисліпідемія — статини, деяким пацієнтам можна рекомендувати комбінацію статинів і фібратів;
в) гіпертригліцеридемія — фібрати, омега-3-поліненасичені жирні кислоти (ПНЖК) та/чи статини.
3. У безсимптомних пацієнтів: якщо шляхом модифікації способу життя протягом 8–12 тиж не вдається досягти встановленої мети, слід розпочати медикаментозне гіполіпідемічне лікування відповідно до варіанта дисліпідемії.
4. У пацієнтів зі встановленою ІХС чи її еквівалентами терапію статинами необхідно розпочати одночасно із заходами немедикаментозної профілактики.
Перелік додаткових медичних послуг
1. При супутній АГ — антигіпертензивна терапія.
2. При супутньому ЦД — гіпоглікемічна терапія.
3. При тяжких формах сімейних дисліпідемій — можлива корекція ліпідного профілю методом аферезу.
Таблиця 2.6. Стратегія втручань залежно від загального серцево-судинного ризику і рівня ЛПНЩ
|
Загальний серцево-судинний ризик (SCORE), % |
Рівень ЛПНЩ |
||||
|
<70 мг/дл <1,8 мМ/л |
70–100 мг/дл 1,8–2,5 мМ/л |
100–155 мг/дл 2,5–4,0 мМ/л |
155–190 мг/дл 4,0–4,9 мМ/л |
>190 мг/дл >4,9 мМ/л |
|
|
<1 (низький ризик) |
Без втручань |
Без втручань |
Зміна способу життя |
Зміна способу життя |
Зміна способу життя, розглядати лікування, якщо не піддається контролю |
|
Клас/рівень |
І/С |
І/С |
І/С |
І/С |
ІІа/А |
|
≥1 до <5 (помірно підвищений ризик) |
Зміна способу життя |
Зміна способу життя |
Зміна способу життя, розглядати лікування, якщо не піддається контролю |
Зміна способу життя, розглядати лікування, якщо не піддається контролю |
Зміна способу життя, розглядати лікування, якщо не піддається контролю |
|
Клас/рівень |
І/С |
І/С |
ІІа/А |
ІІа/А |
І/А |
|
>5 до <10 (високий ризик) |
Зміна способу життя, розглядати лікування |
Зміна способу життя, розглядати лікування |
Зміна способу життя, призначити лікування негайно |
Зміна способу життя, призначити лікування негайно |
Зміна способу життя, призначити лікування негайно |
|
Клас/рівень |
ІІа/А |
ІІа/А |
ІІа/А |
І/А |
І/А |
|
≥10 (дуже високий ризик) |
Зміна способу життя |
Зміна способу життя, призначити лікування негайно |
Зміна способу життя, призначити лікування негайно |
Зміна способу життя, призначити лікування негайно |
Зміна способу життя, призначити лікування негайно |
|
Клас/рівень |
ІІа/А |
ІІа/А |
І/А |
І/А |
І/А |
Для збереження низького ризику в майбутньому, а також (особливо) для зниження високого ризику, необхідна модифікація способу життя, а в разі її неефективності — додавання медикаментозного лікування для досягнення основних цілей серцево-судинної профілактики, наведених у табл. 2.7.
У разі неможливості здійснювати контроль досягнення цільового рівня ХС ЛПНЩ (<1,8 ммоль/л) на рівні первинної ланки рекомендується контролювати рівень загального ХС — <4,0 ммоль/л або зниження на 50% початкового рівня. Перевага в досягненні цільових рівнів надається ХС ЛПНЩ (табл. 2.8).
Таблиця 2.7. Основні цілі серцево-судинної профілактики
|
Тютюнопаління |
Відмова від тютюнопаління в будь-якому вигляді |
|
Дієта |
Низькокалорійна дієта з обмеженням жирів, збільшення кількості овочів, фруктів і риби |
|
Фізична активність |
2,5–5 год середньої фізичної активності на тиждень чи 30–60 хв щодня |
|
Маса тіла |
Індекс маси тіла (ІМТ) 20–25 кг/м2, окружність талії <94 см (чоловіки), <80 см (жінки) |
|
АТ |
<140/90 мм рт. ст. |
|
ЦД |
HbA1c <7%, АТ <140/90 мм рт. ст. |
Таблиця 2.8. Цільові рівні показників ліпідограми
|
Показник ліпідограми, ммоль/л |
Ризик |
|||
|
низький |
помірний |
високий |
дуже високий |
|
|
Загальний ХС |
≤5,5 |
≤5,0 |
≤4,5 |
≤4,0 |
|
ЛПНЩ |
≤3,5 |
≤3,0 |
≤2,5 |
≤1,8 |
|
ТГ |
<1,7 |
|||
Корекція дисліпідемій [60, 77]
Лікувальні заходи загального характеру для збереження здорового способу життя [13, 14]
Величезне значення в лікуванні при атеросклерозі відіграє здоровий спосіб життя, який передбачає [66, 77]:
1. Відмову від шкідливих звичок.
2. Підтримання нормальної маси тіла.
3. Раціональне харчування.
4. Фізичні тренування.
Якщо хворий не веде здорового способу життя, ефективність медикаментозних і хірургічних методів лікування буде мінімальною. При багатьох ССЗ ефективність загальних заходів для дотримання здорового способу життя не тільки не поступається медикаментозним та хірургічним методам лікування, а й, навпаки, перевершує їх.
1. Відмова від шкідливих звичок включає відмову від тютюнопаління, зловживання алкоголем та переїдання. Майже всі ССЗ у дорослих людей пов’язані з цими шкідливими звичками. Людина набуває цих недоліків з усіма негативними наслідками переважно у віці від 18 до 30 років.
Тютюнопаління підвищує ризик ССЗ та РСС щонайменше втричі. Викурювання людиною 4 цигарок на день підвищує ризик розвитку ІХС у 4 рази, а викурювання 1 пачки на день — у 10 разів. Однак якщо людина відмовляється від тютюнопаління, то ризик ССЗ та їхніх ускладнень з боку серця знижується у 2 рази вже через 1–2 роки. Окрім цього, тютюнопаління у 20 разів підвищує ризик виникнення раку легені і ще більшою мірою — хронічного обструктивного захворювання легень (ХОЗЛ). Однак ніхто, окрім самого хворого, не змусить його відмовитися від тютюнопаління. Дуже влучно з цього приводу висловився Ед. Вейнер: «Відмовитися від тютюнопаління важко, проте померти від хвороби, спричиненої тютюнопалінням, буде значно легше».
Алкоголь. Погляди лікарів стосовно алкоголю змінились. Якщо вживати алкоголь з розрахунку не більше 30 мл спирту (70 мл горілки) на добу, то це не тільки не шкідливо, а навіть корисно для зниження розвитку ССЗ, спричинених атеросклерозом. Ця доза прирівнюється до 1 келиха (250 мл) сухого вина чи 1 кухля (500 мл) неміцного світлого пива. Однак користь остаточно не доведена. У деяких дослідженнях показано, що смертність зростає при перевищенні дози 15 мл спирту на добу. Не слід випивати всю тижневу «допустиму дозу» алкоголю за один день, оскільки ризик ССЗ при такому вживанні зростає. Водночас алкоголь є висококалорійним продуктом (1 мл спирту — 7 ккал), що спричиняє розвиток ожиріння. В останні роки рекомендується вживати до 20 мл етанолу для чоловіків і 10 мл етанолу для жінок на добу.
2. Раціональне харчування передбачає зниження калорійності їжі (обмеження кількості жирів і вуглеводів). Одним із показників раціонального харчування є нормальна маса тіла, яка визначається за розрахунком зріст (у см) мінус 100 (ідеальна маса тіла дорівнює зріст мінус 110). Окружність талії для жінок повинна становити не більше 80 см, для чоловіків — 94 см. При надмірній масі тіла підвищується вміст ХС у крові, підвищується АТ, виникає ЦД. Для збереження нормальної маси тіла необхідно менше їсти та вести активний спосіб життя (табл. 2.9).
Таблиця 2.9. Дієтичні рекомендації ЄТК та Європейського товариства з атеросклерозу
Рекомендовані продукти
|
Злаки |
Хліб грубого помелу, вівсяна каша, пластівці різних злаків, макаронні вироби |
|
Молочні продукти |
Знежирені: молоко, йогурт, сир |
|
Супи |
Овочеві, консоме |
|
Риба |
Варена, смажена без шкіри, тушкована |
|
Морепродукти |
Устриці, гребінці |
|
М’ясо та ін. |
Індичина, кури, телятина, дичина, кролик, молода баранина. Один-два рази на тиждень пісна яловичина, свинина, білок яйця |
|
Жири |
Поліненасичені олії: соняшникова, кукурудзяна, волоського горіха. Мононенасичені олії: оливкова, рапсова. «М’які» (негідрогенізовані) сорти маргарину, що містять багато моно- чи поліненасичених жирів |
|
Фрукти й овочі |
Усі свіжі та заморожені овочі, особливо бобові: свіжі та висушені боби, квасоля, сочевиця, нут (турецький горох), кукурудза, варена картопля, в тому числі «в мундирі». Усі свіжі чи сушені фрукти, консервовані фрукти без цукру |
|
Десерти |
Фруктове морозиво, желе, пудинги на збираному молоці, фруктові салати |
|
Кондитерські вироби |
Лукум, нуга, карамельні цукерки |
|
Горіхи |
Волоські, мигдаль, каштан |
|
Напої |
Чай, свіжі овочеві та фруктові соки |
|
Приправи |
Перець, гірчиця, пряні трави, спеції |
Продукти обмеженого вживання
|
Злаки |
Макаронні вироби з білого борошна і білий (шліфований) рис |
|
Молочні продукти |
Частково знежирене молоко, знежирені та нежирні сорти сиру, нежирний йогурт |
|
Супи |
Усі, що не увійшли до двох інших категорій |
|
Риба |
Риба, смажена на олії, що не рекомендується |
|
Морепродукти |
Мідії, омари, креветки, кальмари |
|
М’ясо та ін. |
Гусятина, качатина, сосиски, салямі, паштети, шкіра домашнього птаха, яйця |
|
Фрукти й овочі |
Картопля смажена чи фрі, приготовлені на олії, що не рекомендується |
|
Випічка |
Пісочні та бісквітні тістечка, приготовлені на ненасичених маргаринах і жирах |
|
Кондитерські вироби |
Марципан, халва |
|
Горіхи |
Бразильський горіх, кеш’ю, арахіс, фісташки |
|
Напої |
Алкогольні, нежирні напої з какао |
|
Приправи |
Салатні соуси з низьким вмістом жиру |
Продукти, які вживати не бажано
|
Злаки |
Круасани, булочки |
|
Молочні продукти |
Незбиране молоко, згущене молоко, вершки, штучне молоко, жирні сири та йогурти |
|
Супи |
Супи з високим вмістом жиру, крем-супи |
|
Риба |
Ікра, риба, смажена на жирі, що не рекомендується |
|
Жири |
Вершкове масло, шпиг, сало, топлений жир, пальмова олія, тверді маргарини, гідрогенізовані жири |
|
Фрукти й овочі |
Смажена картопля чи фрі, овочі, приготовлені на олії, що не рекомендується |
|
Десерти |
Вершкове морозиво, пудинги чи пиріжки, приготовлені з олією чи вершками |
|
Випічка |
Фабричні тістечка, бісквіти, пироги, пудинги тощо |
|
Кондитерські вироби |
Шоколад, ірис, вершкова помадка, кокосові палички |
|
Горіхи |
Кокосовий горіх, солоні горіхи |
|
Напої |
Шоколадні напої, ірландська кава, солодкі напої, заварна кава, безалкогольні напої |
|
Приправи |
Сіль, салатні соуси, майонез тощо |
Практично зменшення вживання насичених жирних кислот досягається за рахунок різкого обмеження чи повної відмови від вживання тваринних жирів (масло, сметана, жирне молоко, креми, морозиво) (табл. 2.10). Зниження ХС відбувається за рахунок обмеження чи відмови від яєчних жовтків та субпродуктів (печінка, нирки, мозок), жирних сортів м’яса. Крім того, необхідно відмовитися від вживання ковбас і сосисок, в яких багато «прихованих» або проміжних жирів. Основними харчовими продуктами повинні стати фрукти, овочі, злакові (каші на воді), вівсяні та ячмінні висівки, макарони, чорний хліб, куряче м’ясо, риба, знежирені молочні продукти, рослинна олія, трохи горіхів. ПНЖК: омега-6 містяться в соняшниковій, кукурудзяній чи соєвій олії, омега-3 — в морській рибі; мононенасичені жирні кислоти — в соняшниковій чи оливковій олії.
Таблиця 2.10. Склад дієти для корекції дисліпідемій
|
Інгредієнти |
Рекомендоване вживання |
|
Насичені жири |
<7% загальної кількості калорій |
|
Поліненасичені жири |
≤10% загальної кількості калорій |
|
Мононенасичені жири |
≤20% загальної кількості калорій |
|
Загальна кількість білків |
25–35% загальної кількості калорій |
|
Вуглеводи |
50–60% загальної кількості калорій |
|
Клітковина |
20–30 г/добу |
|
Білок |
≈15% загальної кількості калорій |
|
ХС |
<200 мг/дл |
|
Загальна кількість їжі |
Збалансована дієта (з урахуванням енергетичних затрат людини). Загальна калорійність повинна сприяти утриманню бажаної маси тіла і запобігати її збільшенню |
Останнім часом багато уваги приділяють середземноморській дієті. Основними складовими цієї дієти є оливкова олія, морська риба, овочі, фрукти, хліб, макарони, часник, а також сухе вино. Як показано в деяких дослідженнях, «сувора» дієта та фізичні тренування при ІХС дуже ефективні. Зниження ХС до нормального рівня вже через рік може зумовити зниження смертності на 60%.
Поряд з цим слід відзначити, що харчові добавки неефективні в лікуванні при дисліпопротеїнемії. Вплив антиоксидантів (вітамін С, Е, бета-каротин) на розвиток атеросклерозу вивчали у декількох рандомізованих дослідженнях. Встановлено, що застосування антиоксидантів супроводжується підвищенням ризику серцево-судинних ускладнень (!).
У Ліонському дієтичному дослідженні (1999) показано, що дотримання середземноморської дієти запобігає виникненню повторних загострень ІХС після першого ІМ. Вплив омега-3-ПНЖК на коронарний атеросклероз свідчить про те, що вживання продуктів, які містять ПНЖК, сповільнює прогресування коронарного атеросклерозу. Водночас доказовою медициною не визначено суттєвого впливу бета-каротидного компонента на розвиток основних ССЗ.
Стосовно вживання свіжих овочів і фруктів рекомендації Американської асоціації серця (ААС/AHA) такі: їх необхідно вживати 5 разів на тиждень. Харчові продукти необхідно варити, тушкувати, але не смажити. Потреба в калоріях для здорової людини в середньому становить 2000 ккал/добу. Щоб схуднути на 1 кг протягом 1 тиж, необхідно відмовитися від 1000 ккал. Слід пам’ятати, що біфштекс спричиняє виділення 800 ккал, смажена свиняча грудинка — 900 ккал, порція морозива з наповнювачем — 400 ккал, 100 г мигдального торта — 500 ккал.
Однак надмірно низьке вживання жирів і масел підвищує ризик недостатнього надходження до організму антиоксиданта вітаміну Е та незамінних жирних кислот, а також може призводити до негативних змін рівня ХС, ЛПВЩ. Вміст ХС у раціоні варто знизити до 300 мг/добу, особливо у людей з високим рівнем ХС у плазмі крові.
Для нормалізації маси тіла в більшості випадків обмежують калорійність їжі до 1200–1500 ккал/добу. Бажано не їсти після 18–19-ї години. При сильному відчутті голоду можна з’їсти небагато овочів або випити сік із м’якоттю. За 1 год ходьби зі швидкістю 5 км/год «спалюється» близько 300 ккал.
Потреба людини в кухонній солі становить 200 мг/добу; натомість більшість людей споживає 13–14 г/добу (тобто у 60–70 раз більше норми (!)). Вживання цукру не повинно перевищувати 10% добового калоражу. Додаткове обмеження вживання цукру може бути корисним при високому рівні ТГ у крові, метаболічному синдромі та ЦД.
3. Фізичні тренування мають велике значення для лікування пацієнтів із ССЗ. Хворим, які чекають на пересадку серця, рекомендовані фізичні навантаження, а при ІМ з другого дня призначають фізичні вправи. При ССЗ пацієнтам рекомендується щодня або 4–5 разів на тиждень займатися фізичними тренуваннями впродовж 20–30 хв з такою інтенсивністю, щоб виникала слабка задишка, а частота серцевих скорочень (ЧСС) досягала 100–130 уд./хв. Згідно з рекомендаціями американських медиків, достатньо щодня проходити 2,5 км за 30 хв. Якщо хворий здатний бігати, то можна бігати. Також корисними стануть плавання у басейні та тренування на тренажерах. Під впливом фізичного навантаження відбувається тренування міокарда, покращення функції судин, м’язи отримують більше кисню з крові. У хворих на АГ під впливом фізичних навантажень знижується АТ завдяки збільшенню синтезу депресорних факторів; при атеросклерозі зменшується вміст ХС та підвищується ХС ЛПВЩ, а також збільшується кількість антитромбоцитарних факторів. Отже, будь-яка лікувальна програма без фізичних тренувань буде недостатньо ефективною. Видатний український хірург М.М. Амосов на основі розробленої ним методики і власного досвіду рекомендував кожну фізичну вправу повторювати 100 разів щодня, а для профілактики захворювань суглобів виконувати не менше 300–400 рухів у кожному хворому суглобі.
4. Необхідно нормалізувати масу тіла (при ожирінні ІМТ потрібно знизити до 25–30 кг/м2; при надмірній масі тіла — до 25 кг/м2; окружність талії в нормі становить <94 см для чоловіків європейського походження і <80 см — для жінок). Навіть помірне зменшення маси тіла на 5–10% покращує ліпідний профіль і позитивно впливає на інші фактори серцево-судинного ризику.
Таким чином, здоровий спосіб життя є передумовою покращення здоров’я і запобігання виникненню ССЗ та їх ускладнень.
5. Ліпідознижувальні препарати. Медикаментозне лікування при дисліпідемії передбачає використання статинів (ловастатин, симвастатин, аторвастатин, розувастатин, пітавастатин), фібратів (фенофібрат) [60, 77].
ЄТК (2007) пропонує такі рекомендації:
1. Цільовий рівень загального ХС повинен бути <5 ммоль/л (<190 мг/дл), а ХС ЛПНЩ — <3 ммоль/л (<115 мг/дл). У пацієнтів із високим ризиком, особливо з клінічно встановленим ССЗ атеросклеротичного генезу, а також у пацієнтів із ЦД цільові рівні становлять: ХС <4,5 ммоль/л (<175 мг/дл), бажано <4 ммоль/л (9–15,5 мг/дл), для ХС ЛПНЩ — <2,5 ммоль/л (<100 мг/дл), бажано <1,8 ммоль/л (<80 мг/дл).
2. У разі, коли ступінь ризику ССЗ становить ≥5% за SСORE, необхідно проводити терапію статинами.
3. Успіх гіполіпідемічної терапії залежить від початкового рівня ризику: чим вищий ризик, тим більша ефективність.
4. Для пацієнтів із ССЗ без ЦД, особливо за наявності факторів ризику або мікроальбумінурії, рекомендується рання інтенсивна терапія статинами. Це також стосується хворих на ЦД 2-го типу з помірним ризиком ССЗ.
5. Переконливо доведено, що терапія статинами знижує не лише рівень ХС у крові, а й частоту серцево-судинних подій, смертності та необхідність проведення АКШ.
6. Фібрати застосовують в основному для зниження рівня ТГ і підвищення ХС ЛПВЩ. Омега-3-ПНЖК застосовують для зниження рівня ТГ; вони мають також антиаритмічну властивість і зменшують ризик ІМ, РСС.
Найефективнішою гіполіпідемічною групою препаратів є статини. Деякі автори роль статинів у лікуванні атеросклерозу порівнюють з ефективністю пеніциліну, який використовують для лікування при інфекційних захворюваннях, що свідчить про революційний переворот у кардіології наприкінці ХХ сторіччя.
Статинам властива багатогранна дія [5, 46]:
1) вони поліпшують функцію ендотелію, зменшують дисліпідемію (знижують вміст ХС, ТГ, ХС ЛПНЩ і підвищують ХС ЛПВЩ, нормалізують індекс атерогенності); пригнічують процеси запалення судин (знижують СРБ; стабілізують атеросклеротичну бляшку, що приводить до поліпшення перфузії міокарда; зменшують ішемію міокарда; пригнічують синтез металопротеїназ). Зниження рівнів ТГ більш виражене при застосуванні ліпофільних статинів (аторвастатину, симвастатину);
2) після 2-річного лікування статини запобігають прогресуванню старих бляшок і появі нових та зменшують існуючі атероми на 3% частіше (РКД МААS);
3) через ≥4 роки вони знижують кардіальну і загальну смертність (на 18–30%), запобігають серцево-судинним ускладненням, зменшують потребу в реваскуляризації (особливо у пацієнтів літнього віку, із супутнім ЦД, атеросклерозом мозкових і периферичних артерій);
4) зменшують кількість серцево-судинних ускладнень, розвиток ЦД (на 30%) та остеопорозу в 2 рази [60, 77].
За даними РКД 4S (1994), СARE (1996), HPS (2001), HS (2003), при порушенні ліпідного спектра крові найбільш ефективними є статини, які суттєво (на 30–40%) знижують серцево-судинну смертність у хворих як із підвищеним, так і з нормальним вмістом ХС. Найбільш вивчений аторвастатин, який є основним гіполіпідемічним засобом. У РКД FVERT показано, що застосування аторвастатину не менш ефективне, ніж проведення транслюмінальної балонної коронарної ангіопластики (ТБКА) зі стентуванням КА. У РКД СHESS продемонстровано, що симвастатин більшою мірою, ніж аторвастатин, підвищує ЛПВЩ. Останнім часом широко застосовують розувастатин.
На сьогодні за допомогою РКД обстежено більше ніж 100 тис. хворих, яких спостерігали до 10 років; доведено клінічну ефективність різних статинів у первинній та вторинній профілактиці ІХС, ГКС, стенокардії, інсультів, деменції, остеопорозу.
Відзначають такі плейотропні (неліпідні) ефекти статинів:
- стабілізація та регрес атеросклеротичної бляшки;
- протизапальний ефект;
- корекція NO-ендотеліальної дисфункції;
- імуномодуляторний ефект;
- зменшення проліферації гладком’язових клітин;
- антитромботична дія;
- вплив на апоптоз;
- зниження смертності, розвитку ІМ та його ускладнень [4, 6].
При ГКС лікування статинами рекомендують проводити впродовж 1–4 днів після госпіталізації хворих. Аторвастатин застосовують у дозі 40 мг/добу, розувастатин — 10–20 мг/добу з повторним визначенням ліпідних показників через 4–6 тиж з подальшою корекцією дози статинів. РКД встановлена позитивна дія аторвастатину при ІХС у пацієнтів із попередньо нормальним рівнем ХС ЛПНЩ.
Згідно з рекомендаціями ЄТК (2007), для пацієнтів із ІХС з високим ризиком ССЗ цільовими визнані такі показники:
- загальний ХС <4,5 ммоль/л; ТГ <1,7 ммоль/л;
- ЛПНЩ <2,5 ммоль/л;
- ЛПВЩ >1,0 ммоль/л у чоловіків і >1,2 ммоль/л — у жінок.
У зв’язку з домінуючою роллю запалення у клінічній дестабілізації ІХС, останнім часом з’явилася можливість впливати на цю ланку патогенезу ГКС. Результати декількох досліджень свідчать про те, що застосування статинів при ГКС суттєво поліпшує як госпітальний, так і подальший перебіг ІХС. Так, у дослідженні MІRAСL аторвастатин, призначений при ГКС, знизив частоту повторних епізодів його проявів. Аналіз Шведського реєстру ГКС показав, що смертність хворих, які приймали статини (переважно симвастатин) до чи під час ІМ, була вдвічі нижчою протягом наступного року, на відміну від тих, які не застосовували статинотерапії.
Вірогідно, механізмами протизапальної дії статинів є:
- покращення функції ендотелію, у тому числі бар’єрної функції ендотеліоцитів стосовно окиснених ЛПНЩ;
- пригнічення локального синтезу ХС у судинній стінці;
- активація продукції оксиду азоту та циклічного аденозинмонофосфату ендотелієм;
- гальмування скорочуваності гладком’язових клітин під впливом катехоламінів та ангіотензину ІІ;
- зниження інфільтрації судинної стінки макрофагами (за рахунок зменшення продукції ендотеліоцитами локальних медіаторів запалення).
Метааналіз 164 короткочасних клінічних досліджень показав, що зниження рівня ХС ЛПНЩ на тлі терапії 10 мг аторвастатином порівняно з ефективністю терапії 40 мг ловастином чи симвастатином в середньому становить 35%.
У разі, якщо не вдається досягти рекомендованого рівня ХС ЛПНЩ при застосуванні коректорів дисліпідемій в адекватній дозі, рекомендується зниження показника на ≥50% порівняно з початковим рівнем.
Статини мають певну особливість впливу на організм жінки, про що свідчать нові дані. Під їх впливом відбувається суттєвіше зниження частоти серцево-судинних подій, регрес атеросклеротичних бляшок у жінок порівняно з чоловіками. (табл 2.11) Статини частіше викликають розвиток м’язових симптомів у жінок, що призводить до відмови від їх подальшого застосування для цих пацієнток. Проте вони здатні знижувати ризик розвитку раку молочної залози, зменшують смертність та позитивно впливають на клінічний перебіг новоутворення, ніж у пацієнток без статинів. Ці препарати знижують розвиток тромбоемболічних ускладнень у жінок. Статини продемонстрували статистично значиму здатність підвищувати щільність кісткової тканини, зменшувати розвиток переломів кісток (у тому числі стегнової кістки).
Таблиця 2.11. Статинотерапія високої, середньої та низької інтенсивності (АСС/АНА, 2013)
|
Висока |
Середня |
Низька |
|
Високі дози терапії (їх використання приводить до зниження рівня ХС ЛПНЩ в середньому на ≥50%) |
Середні дози терапії (їх використання приводить до зниження рівня ХС ЛПНЩ в середньому на 30–50%) |
Низькі дози терапії (їх використання приводить до зниження рівня ХС ЛПНЩ в середньому на ≥30%) |
|
|
|
Інгібітори PCSK9 [32] — новий клас препаратів, що впливають на білок PCSK9, який бере участь у регуляції рецепторів ЛПНЩ на клітинній поверхні та призводить до деградації останнього. Ці препарати становлять собою моноклональні антитіла до зазначеного білка (ЄТК, ЄТБА, 2016). Нещодавно Європейське агентство з лікарських засобів та Управління з контролю харчових продуктів і лікарських засобів (FDA, США) схвалили цю групу препаратів. Ефективність цих препаратів у зниженні концентрацій ЛПНЩ у плазмі крові коливається в діапазоні 50–70% і не залежить від фонотерапії статинами та езетимібом тощо. Інгібітори PCSK9 знижують концентрацію ЛПНЩ, серцево-судинний ризик і суттєво не впливають на вміст ТГ та ЛПВЩ. Отже, ці препарати знижують рівні ХС ЛПНЩ в усіх пацієнтів і в клітинах печінки. Інгібітори PCSK9 застосовують у хворих з високим серцево-судинним ризиком і гетерозиготною сімейною гіперхолестеринемією. Їх застосовують по 150 мг підшкірно (п/ш) один раз на тиждень. Вивчення їх продовжується.
До можливих побічних реакцій належать свербіж у місці ін’єкції та грипоподібні симптоми. У тих випадках, коли хворі не переносять статини, препаратом вибору є інгібітори PCSK9. Однак слід зазначити, що PCSK9 дуже дорого коштують, тому їх зможуть застосовувати тільки в деяких країнах люди з високим достатком.
Етапність надання медичної допомоги [60]
Первинна допомога передбачає раннє виявлення та усунення факторів ризику на популяційному рівні для запобігання новим випадкам ССЗ. Такі профілактичні заходи включають відмову від тютюнопаління, формування здорових харчових звичок, регулярне фізичне навантаження, зменшення надмірної маси тіла, виявлення супутньої патології, яка може спричиняти виникнення дисліпідемій (ЦД, гіпотиреоз, синдром полікістозних яєчників, синдром Кушинга, нефротичний синдром, панкреатит тощо). Призначення ліпідознижувальної терапії — відповідно до виявленого варіанта дисліпідемії.
Вторинна допомога забезпечує подальше виявлення і корекцію факторів ризику та лікування з метою запобігання передчасному розвитку ускладнень і передчасної смерті від ССЗ. Рекомендації щодо модифікації способу життя та призначення ліпідознижувальної терапії — відповідно до виявленого варіанта дисліпідемії.
Третинна (високоспеціалізована) допомога полягає у призначенні ліпідознижувальної терапії відповідно до виявленого варіанта дисліпідемії. У рідкісних випадках пацієнтам із тяжкою гіперліпідемією, насамперед хворим із гомозиготною та вираженою гетерозиготною формами сімейної гіперхолестеринемії і тяжкою тригліцеридемією, необхідна консультація фахівця для вирішення питання про необхідність проведення плазмаферезу. Процедура плазмаферезу виконується тільки у спеціалізованих закладах кардіологічного профілю.
Особливості дії фармакологічних препаратів
1. Статини (симвастатин, аторвастатин, розувастатин, пітавастатин). Механізм дії: знижують синтез ХС у печінці шляхом конкурентного інгібування активності 3-гідрокси-метилглутарил-коензим-А (ГМГ-КоА)-редуктази. Зниження внутрішньоклітинної концентрації ХС спричиняє експресію рецепторів ЛПНЩ на поверхні гепатоцитів, що сприяє підвищенню екстракції ХС ЛПНЩ із крові та зниженню концентрації циркулюючого ХС ЛПНЩ та інших ліпопротеїнів.
2. Інгібітори всмоктування ХС (езетиміб). Механізм дії: езетиміб — перший лікарський засіб, призначений для зниження рівня ліпідів, який інгібує всмоктування в кишечнику ХС, що надходить з їжею та із жовчі, не впливаючи на всмоктування інших жиророзчинних харчових речовин. Інгібуючи всмоктування ХС на рівні ворсинчастої облямівки кишечнику, езетиміб знижує кількість ХС, що надходить до печінки з ремнантів хіломікронів. У відповідь на зниження надходження ХС печінка активує на своїй поверхні рецептори ЛПНЩ, що приводить до збільшення кліренсу ЛПНЩ із крові.
3. Фібрати (фенофібрат). Механізм дії: фібрати є агоністами ядерних альфа-рецепторів, активація яких приводить до проліферації пероксимом (PPAR-α), і діють через фактори транскрипції, що регулюють різні етапи метаболізму ліпідів і ліпопротеїнів. Взаємодіючи з PPAR-α, фібрати впливають на різні кофактори і регулюють експресію генів. У результаті фібрати ефективно знижують рівень ТГ у крові натще, а також постпрандіальний рівень ТГ і концентрацію ремнантних частинок ліпопротеїнів, багатих на ТГ. Фібрати помірно підвищують рівень ХС ЛПВЩ.
4. Омега-3-ПНЖК (ейкозапентаєнова і докозагексаєнова). Механізм дії: омега-3-жирні кислоти є компонентами риб’ячого жиру і входять до складу продуктів середземноморської дієти, яку використовують для зниження рівня ТГ. Омега-3-ПНЖК в лікарських дозах (>2 г/добу) впливають на рівень ліпідів і ліпопротеїнів у сироватці крові, передусім на концентрацію ЛПДНЩ. Механізм дії погано вивчений, хоча він може бути пов’язаний з їхньою здатністю взаємодіяти з ядерними рецепторами (PPAR) і зменшувати секрецію частинок апо-В.
Інтервенційні та хірургічні методи лікування. Хворим із гомозиготною і тяжкою гетерозиготною сімейною гіперхолестеринемією потрібна консультація фахівця для вирішення питання про необхідність проведення плазмаферезу ЛПНЩ у спеціалізованому центрі. Під час цієї процедури ЛПНЩ і ЛПДНЩ видаляються із плазми крові у процесі екстракорпорального кровообігу щотижня або раз на 2 тиж.
Лікування гіпертригліцеридемії. Після виключення чи лікування панкреатиту у тяжких випадках для швидкого зниження рівня ТГ можна використовувати плазмаферез. Статини є засобом першої лінії у зниженні як загального кардіоваскулярного ризику, так і рівня ТГ. Сильнодіючі статини (аторвастатин, розувастатин та пітавастатин) викликають значне зниження рівня ТГ, особливо у високих дозах. Омега-3-ПНЖК теж знижують концентрацію ТГ.
В останніх публікаціях доведено, що розувастатин у пацієнтів із ГКС приводить до більш ефективного зниження ХС ЛПНЩ і підвищення ХС ЛПВЩ, ніж аторвастатин [73]. Цей препарат запобігає виникненню кардіальних подій (смерть, ІМ, інсульт). Розувастатин зменшує епізоди ішемії міокарда та їх тривалість, підвищує дію антиаритмічних препаратів (ААП), позитивно впливає на показники ліпідного спектра крові, центральної гемодинаміки, сповільнює розвиток ремоделювання лівого шлуночка (ЛШ), покращує мікрогемодинаміку та позитивно впливає на прогноз ГКС. Доведено, що в США крива зниження серцево-судинної смертності проходить паралельно з кривою зниження середнього вмісту ХС у населення. При цьому в нормалізації гіперхолестеринемії статини найбільш ефективні [17, 60].
Останнім часом інтенсивно вивчається вплив ПНЖК при атеросклерозі. Відомо, що в плазмі крові існує 4 основних класи ліпопротеїнів: ХС та його ефіри, ТГ, фосфоліпіди та жирні кислоти. До ПНЖК належать омега-3 (альфа-ліноленова, ейкозапентаєнова і докозагексаєнова) і омега-6 (лінолева, гамма-лінолева та арахідонова кислоти), які синтезуються в організмі з продуктів розпаду вуглеводів (надходять з їжею). Омега-3-ПНЖК можуть синтезуватись в адекватній кількості лише у водоростях. Для людини джерелом омега-3-ПНЖК є деякі сорти морської риби (лосось, скумбрія, оселедець).
З метою лікування атеросклерозу широко застосовують омега-3-ПНЖК — як для первинної, так і для вторинної профілактики захворювання, а також терапії при ІМ та при високому ризику РСС. Омега-3-ПНЖК характеризуються антисклеротичною, антиаритмічною (зменшують вираженість шлуночкової аритмії), антифібриляторною, антиоксидантною дією, а також підвищують синтез оксиду азоту.
У проведеному РКД GІSSІ-Prevenzіone (1999), що охопило 11 325 хворих, після застосування омега-3-ПНЖК загальна і серцево-судинна смертність знизилися відповідно на 20 і 30%, а в дослідженні DART — на 29%. У дослідженнях GІSSІ-Prevenzіone, PHS та інших встановлено, що РСС зменшилась майже на 45%. Тому ці препарати необхідно застосовувати при високому ризику ССЗ і після перенесеного ІМ.
Нещодавно проведено метааналіз довготривалих (не менше 5 років) РКД зі статинами за участю 90 056 пацієнтів, який підтвердив, що зниження ХС ЛПНЩ на 1,0 ммоль/л/рік на 12% знижує загальну смертність і на 19% — коронарну смертність уже після першого року лікування. Протягом 5 років зниження ХС ЛПНЩ на 20% зменшує виникнення основних судинних подій на 48 випадків (на 1000 пацієнтів); на 30 випадків — ІМ, на 27 випадків — коронарних реваскуляризацій і на 8 випадків — ішемічних інсультів. При цьому частота виникнення злоякісних новоутворень за всі роки застосування статинів не підвищилася. Таким чином, впровадження лікування при ССЗ цільовими дозами статинів в Україні є першочерговим завданням у кардіологічній і терапевтичній практиці.
Варті уваги дані, отримані в РКД JUPІTER. Застосування розувастатину у дозі 20 мг/добу у практично здорових жінок віком ≥60 років протягом 1,9 року у разі відсутності гіперліпідемії, але за підвищеного рівня СРБ у крові зумовлює зниження ризику розвитку тяжких ускладнень ССЗ.
При застосуванні статинів виявлені деякі особливості у призначеннях лікарів різних спеціальностей: недостатньо широким є їхнє застосування невропатологами та судинними хірургами, недооцінюється призначення антитромбоцитарної терапії (ацетилсаліцилова кислота (асК) та клопідогрель). Однак слід пам’ятати, що статини можуть спричиняти не лише рабдоміоліз, біль та органічні зміни в м’язах (міопатію), а й мікрогематурію (можливо, вона спричинена пригніченням статинами проксимальної реабсорбції білка в канальцях, оскільки немає даних про органічне ураження канальців і прогресування ХХН). Відомо, що статини можуть підвищувати концентрацію дигоксину в крові та взаємодіяти з антидепресантами (інгібіторами зворотного захоплення серотоніну). Водночас при застосуванні статинів необхідно обмежувати вживання алкоголю, грейпфрутового соку та зеленого чаю.
Отже, рішення про призначення статинів має ґрунтуватися на оцінці усіх факторів, а не тільки рівня ліпідів. Чим вищий сумарний ризик судинних ускладнень, тим агресивнішою повинна бути терапія статинами.
Стандарти лікування атеросклерозу наведені в алгоритмі 2.2.
|
Алгоритм 2.2. Корекція порушень ліпідного спектра крові [60] Крок 1. Кращими препаратами в лікуванні при дисліпідемії, згідно з рекомендаціями доказової медицини, є статини (інгібітори ГМГ-КоА-редуктази), які знижують рівень ліпопротеїнів, багатих на ХС. Застосовують один із препаратів:
Максимальний гіполіпідемічний ефект спостерігається через 4–6 тиж. Крок 2. Комбіновані препарати:
Крок 3. У разі недостатньої ефективності лікування, високій (особливо сімейній) гіперхолестеринемії показана гемосорбція на курс 5 процедур або ЛПНЩ-імуносорбція. |
Тривалість лікування. Хворі потребують пожиттєвого немедикаментозного і медикаментозного лікування.
Критерії якості лікування (ВАКУ, 2018) [60]
У більшості пацієнтів з дисліпідеміями критерієм якості життя є досягнення цільових рівнів ХС і ХС ЛПНЩ.
1. Досягнення цільових рівнів ХС і ХС ЛПНЩ:
- для загальної популяції цільовий рівень ХС у плазмі крові повинен становити <5,0 ммоль/л (<190 мг/дл), а рівень ХС ЛПНЩ — <3 ммоль/л (<115 мг/дл);
- цільові рівні для пацієнтів з ІХС, клінічними проявами ССЗ і пацієнтів з ЦД: для загального ХС — <4 ммоль/л (<115 мг/дл), для ХС ЛПНЩ — <1,8 ммоль/л (<70 мг/дл) або ≥50% зниження, якщо досягнути цільових рівнів не вдалося.
2. Лікування спрямоване на досягнення цільового рівня ХС ЛПНЩ як у пацієнтів з високим ризиком (<2,5 ммоль/л, <100 мг/дл) чи за наявності ССЗ, так і у пацієнтів з дуже високим ризиком (<1,8 ммоль/л, <70 мг/дл). Якщо цільових рівнів досягти неможливо, слід намагатися максимально знизити рівень ХС ЛПНЩ шляхом застосування відповідних комбінацій препаратів та доз, які добре переносяться пацієнтом.
У хворих із сімейною гіперхолестеринемією чи іншими генетичними порушеннями метаболізму ліпідів лікування спрямоване на досягнення цільового рівня ХС ЛПНЩ як у пацієнтів з високим ризиком (<2,5 ммоль/л, <100 мг/дл) чи за наявності ССЗ, так і в пацієнтів із дуже високим ризиком (<1,8 ммоль/л, <70 мг/дл).
Зниження рівня загального ХС на 20% і ХС ЛПНЩ — на 30% є критерієм досягнення істотного клінічного ефекту.
Можливі побічні дії та ускладнення
Статини. Статини зазвичай добре переносяться; серйозні небажані явища розвиваються рідко. Хоча застосування статинів загалом є ефективним для профілактики ССЗ, відповідь на лікування, як і частота розвитку небажаних явищ, відрізняються в окремих пацієнтів.
Скелетні м’язи. Ймовірність розвитку небажаних явищ підвищується у пацієнтів літнього віку, при недостатній масі тіла, у жінок, за наявності порушень функції нирок і печінки, у післяопераційний період, при гіпотиреозі, поліорганних захворюваннях і зловживанні алкоголем. Найсерйознішим небажаним явищем, пов’язаним із застосуванням статинів, є міопатія, яка може прогресувати до розвитку рабдоміолізу, ниркової недостатності та смерті в особливо тяжких випадках. Основним маркером руйнування і загибелі клітин скелетних м’язів є підвищення у крові рівня креатинфосфокінази (КФК). Підвищення рівня КФК є кращим, хоч і не зовсім однозначним індикатором розвитку міопатії, індукованої статинами.
Печінка. Підвищення рівня печінкових трансаміназ (аспартатамінотрансфераза (АсАТ) і аланінамінотрансфераза (АлАТ)) визначається у 0,5–2,0% пацієнтів, які застосовують статини, і має дозозалежний характер. Загальним визначенням значного підвищення рівня печінкових ферментів є перевищення верхньої межі норми в 3 рази, що зберігається при двох послідовних вимірюваннях, які зазвичай проводять із коротким інтервалом між ними (від кількох днів до кількох тижнів). Прогресування уражень з розвитком печінкової недостатності відзначають дуже рідко.
Езетиміб. Немає даних про наявність клінічно значущого впливу віку, статі чи раси пацієнта на фармакокінетику езетимібу. Пацієнти з помірними порушеннями печінкової функції та помірними або вираженими порушеннями функції нирок не потребують зміни дози препарату. Його можна призначати в комбінації з будь-яким статином у будь-якій дозі. Не повідомлялося про розвиток серйозних небажаних явищ; найбільш поширеними небажаними явищами є помірне підвищення рівня печінкових ферментів та біль у м’язах.
Фібрати загалом добре переносяться, однак можуть спричиняти помірні побічні ефекти. Розлади функції органів ШКТ відзначали у 5% пацієнтів; шкірний висип — у 2%. Найвідомішими небажаними явищами, пов’язаними з дією фібратів, є міопатія, підвищення рівня печінкових ферментів і холелітіаз.
Омега-3-ПНЖК. Цей клас безпечний і позбавлений будь-якої клінічно значущої взаємодії, проте при застосуванні в поєднанні з АСК/клопідогрелем антитромботична дія препарату може підвищувати схильність до кровотеч.
Характеристика очікуваних кінцевих результатів лікування. Вибір цілі для лікування при дисліпідемії зазвичай ґрунтується на результатах клінічних досліджень. Практично в усіх дослідженнях, спрямованих на вивчення методів зниження рівня ліпідів, ХС ЛПНЩ вважали індикатором відповіді на лікування. Отже, рівень ХС ЛПНЩ залишається основною мішенню терапії при дисліпідемії (табл. 2.12).
Таблиця 2.12. Характеристика очікуваних результатів лікування [60]
|
Рекомендації, що стосуються аналізу очікуваних кінцевих результатів лікування |
Клас |
Рівень |
|
Рівень ХС ЛПНЩ рекомендований як основна ціль терапії |
І |
А |
|
Рівень загального ХС має розглядатись як ціль терапії у разі неможливості аналізу ліпідних фракцій |
ІІа |
А |
|
ТГ слід визначати під час лікування дисліпідемій з високим рівнем ТГ |
ІІа |
В |
|
ХС не-ЛПВЩ слід розглядати як додаткову ціль терапії у разі комбінованих гіперліпідемій та у хворих на ЦД, пацієнтів з метаболічним синдромом та ХХН |
ІІа |
В |
|
Рівень апо-В слід розглядати як додаткову ціль терапії |
ІІа |
В |
|
Рівень ХС ЛПВЩ не рекомендовано розглядати як ціль терапії (!) |
ІІІ |
С |
|
Співвідношення апо-В/апо-А1 і ХС не-ЛПВЩ/ХС ЛПВЩ не рекомендовано розглядати як ціль терапії |
ІІІ |
С |
Згідно з рекомендаціями доказової медицини, статини у пацієнтів із ІХС з гіперхолестеринемією, які застосовували упродовж 6 міс, зумовлюють гіполіпідемічний, антиішемічний, антиоксидантний та цитопротекторний ефект. Відзначені позитивні властивості статинів слід використовувати у вторинній профілактиці ІХС (алгоритм 2.3).
Таким чином, статинам притаманні кардіо-, вазо-, нефро- та церебропротекторні властивості; вони знижують смертність при ІМ, стенокардії, АГ, ЦД. Останніми роками для підвищення ефективності статинів (блокують синтез ХС) застосовують їх комбінацію з езетимібом у дозі 5 мг, який пригнічує всмоктування ХС в кишечнику. У поодиноких дослідженнях виявлений значний клінічний ефект, однак монотерапія езетимібом, як і комбінація його зі статинами, ще недостатньо вивчені; необхідне подальше широкомасштабне вивчення цієї комбінації препаратів [64].
|
Алгоритм 2.3. Вторинна профілактика ІХС шляхом застосування гіполіпідемічної терапії
|
Таким чином, статинам притаманні кардіо-, вазо-, нефро- та церебропротекторні властивості; вони знижують смертність при ІМ, стенокардії, АГ, ЦД. В останні роки для підвищення ефективності статинів (блокують синтез ХС) застосовують їх комбінацію з езетимібом у дозі 5 мг, який пригнічує всмоктування ХС в кишечнику. У поодиноких дослідженнях виявлений значний клінічний ефект, однак монотерапія езетимібом, як і комбінація його зі статинами, ще недостатньо вивчені; необхідне подальше широкомасштабне вивчення цієї комбінації препаратів [64].
Помилки та необґрунтовані призначення препаратів у разі невиконання рекомендацій доказової медицини:
1. Розвиток рабдоміолізу частіше відзначають у разі комбінованої терапії статинами та фібратами (чи цитостатиками), тому не слід застосовувати такі комбінації препаратів.
2. Небажано призначати нікотинову кислоту при ЦД та подагрі.
Підсумки профілактики атеросклерозу [10, 40]
Первинна профілактика атеросклерозу передбачає зменшення факторів ризику розвитку захворювання:
- раціональне харчування, обмеження вживання жирів і вуглеводів, відмова від тютюнопаління;
- дотримання дієти (зниження частки насичених жирів на 10% загальної калорійності);
- регулярні фізичні вправи (3–5 разів на тиждень), ходьба;
- досягнення оптимальної маси тіла (зменшення її на 10%);
- вживання не більше 20 г етанолу на добу для чоловіків і 10 г — для жінок;
- корекція АГ;
- корекція вуглеводного обміну;
- зниження споживання ХС до 300 мг/добу;
- часте споживання риби (бажано з північних морів, в жирі якої міститься значна кількість омега-3-ПНЖК, що мають протиатерогенну дію); вживання більшої кількості свіжих овочів і фруктів, грубої клітковини та соєвих продуктів (якщо вони добре переносяться);
- психологічна корекція із застосуванням психорелаксаційних програм.
Вторинна профілактика атеросклерозу передбачає тривале застосування антиатеросклеротичних препаратів статинів (протягом 0,5–1 року або постійно), які сповільнюють розвиток захворювання та його ускладнень, подовжують тривалість життя.
Резюме. Первинна профілактика (загальноприйняті рекомендації) та своєчасна рання діагностика атеросклерозу з подальшим застосуванням статинів зумовлюють зниження рівнів загального ХС, ХС ЛПНЩ, підвищення рівня ХС ЛПВЩ, нормалізації функції ендотелію, зниження рівнів СРБ та АТ, покращення якості життя, зменшення ризику розвитку ІМ, інсультів, РСС. Ці значні досягнення в лікуванні та профілактиці атеросклерозу дозволяють з більшою впевненістю дивитись у майбутнє з метою суттєвого зменшення епідемії атеросклерозу в ХХІ столітті.