Ригевидон таблетки, покрытые оболочкой блистер №63
Ригевидон инструкция по применению
Состав
Левоноргестрел - 0,15 мг
Этинилэстрадиол - 0,03 мг
Фармакологические свойства
фармакодинамика. Комбинированные эстроген-прогестагеновые противозачаточные таблетки (мини-пили).
Индекс Перля 0,1 на 100 женщино-лет.
Ригевидон — это комбинированный пероральный контрацептив (КПК), содержащий в своем составе этинилэстрадиол и левоноргестрел. Эффективность КПК обусловлена снижением секреции гонадотропинов, что вызывает угнетение активности яичников. Контрацептивный эффект в результате основывается на взаимодействии различных механизмов, важнейшим из которых является торможение овуляции.
Фармакокинетика
Этинилэстрадиол Абсорбция После приема внутрь этинилэстрадиол быстро и полностью всасывается в ЖКТ, Cmax достигается через 60-180 минут. После пресистемной конъюгации и первичного метаболизма абсолютная биодоступность составляет от 40% до 45%. АUC и Cmax могут со временем незначительно повышаться. Распределение Этинилэстрадиол на 98,8% связывается с белками плазмы крови, почти полностью с альбумином. Биотрансформация Этинилэстрадиол подвергается пресистемной конъюгации в слизистой оболочке тонкого кишечника и в печени. При гидролизе прямых конъюгатов этинилэстрадиола под действием кишечной флоры вновь образуется этинилэстрадиол, который может повторно всасываться, тем самым замыкая круг энтерогепатической циркуляции. Основной путь метаболизма этинилэстрадиола — гидроксилирование, опосредованное цитохромом Р450, в результате чего образуются основные метаболиты — 2-ОН-этинилэстрадиол и 2-метоксиэтинилэстрадиол. 2-ОН-этинилэтилестрадиол далее метаболизируется до химически активных метаболитов. Выведение T½ этинилэстрадиола из плазмы крови составляет примерно 29 ч (26–33 ч); плазменный клиренс варьируется в диапазоне 10-30 л/ч. Выведение конъюгатов этинилэстрадиола и его метаболитов происходит на 40% с мочой и на 60% с калом. Левоноргестрел Абсорбция После перорального применения левоноргестрел быстро и полностью всасывается в ЖКТ. Левоноргестрел полностью биодоступен. После приема внутрь Cmax левоноргестрела в плазме крови достигается через 30-120 минут. T½ составляет примерно 24–55 ч. Распределение Левоноргестрел связывается с альбумином и глобулином, связывающим половые гормоны (ГСПГ). Биотрансформация В основном он метаболизируется путем редукции цикла А с последующей глюкуронизацией. Метаболический клиренс отмечается значительной индивидуальной изменчивостью, которая может частично объяснить значительные различия в концентрации левоноргестрела, наблюдаемые у пациенток. Выведение T½ левоноргестрела составляет примерно 36 ч. Примерно 60% левоноргестрела выводятся с мочой и 40% — с калом.
Показания Ригевидон
пероральная контрацепция.
Решение о назначении препарата Ригевидон следует принимать с учетом индивидуальных факторов риска женщины, существующих на данный момент, в том числе факторов риска развития венозной тромбоэмболии (ВТЭ), а также риска ВТЭ, связанного с приемом препарата Ригевидон, по сравнению с другими комбинированными гормональными контрацептивами (КГК) (см. ПРОТИВОПОКАЗАНИЯ И ОСОБЫЕ УКАЗАНИЯ).
Применение Ригевидон
способ применения.
Как принимать Ригевидон. Внутрь, в порядке, указанном на упаковке, примерно в одно и то же время, по одной таблетке в сутки, запивая небольшим количеством жидкости.
Ригевидон применять ежедневно по 1 таблетке в сутки в течение 21 дня. Каждую следующую упаковку начинают после 7-дневного перерыва, во время которого обычно наступает менструальноподобное кровотечение. Как правило, оно начинается на 2–3-й день после приема последней таблетки и может не закончиться до начала применения таблетки из следующей упаковки.
Как начинать применение препарата Ригевидон
Если гормональные контрацептивы в предыдущем месяце не применяли. Прием таблеток следует начинать в 1-й день естественного цикла, то есть в первый день менструального кровотечения.
Переход с другого КГК (таблетки, вагинального кольца или трансдермального пластыря). Применение Ригевидона необходимо начинать на следующий день после приема последней активной таблетки предыдущего противозачаточного средства, но не позднее следующего дня после перерыва в приеме таблеток или таблетки плацебо, предыдущего противозачаточного средства.
Первую таблетку препарата необходимо принять в день удаления вагинального кольца или трансдермального пластыря, но не позднее дня, когда должен быть наклеен новый трансдермальный пластырь или введено новое кольцо.
Переход к применению препарата Ригевидон с препарата, содержащего только прогестаген (мини-пили, инъекции, имплантат или внутриматочная система с прогестагеном). Переход с мини-пили может быть осуществлен в любой день менструального цикла. Прием препарата Ригевидон следует начинать на следующий день после отмены мини-пили.
Переход с имплантата и внутриматочной системы — в день их удаления, с инъекции — в день, когда должна быть назначена следующая инъекция.
Во всех случаях рекомендуется дополнительно использовать барьерный метод контрацепции в течение первых 7 дней приема таблеток.
После аборта в I триместр беременности. Применение препарата следует начать немедленно в тот же день после операции. В таком случае нет необходимости применять дополнительные средства контрацепции.
После родов или после аборта во II триместр беременности.
Применение препарата следует начинать с 21–28-го дня после родов и при отказе кормления грудью или аборта во II триместр беременности, поскольку существует риск развития тромбоэмболических расстройств в течение послеродового периода. Если женщина начинает принимать таблетку позже, следует дополнительно применять барьерные методы контрацепции в течение первых 7 дней применения препарата. Однако если половой акт уже состоялся, то перед началом применения препарата следует исключить беременность или дождаться первой менструации.
В случае кормления грудью см. Применение в период беременности или кормления грудью.
Что делать в случае пропуска приема таблеток. Эффективность контрацепции может снизиться в случае пропуска приема таблеток, особенно если при этом увеличивается период между приемами последней таблетки из текущей блистерной упаковки и первой таблетки из следующей упаковки.
Если с тех пор, когда должна была быть принята очередная таблетка, прошло менее 12 ч, контрацептивная защита не снижается. Женщине следует принять пропущенную таблетку сразу же, как только она о ней вспомнит, следующую таблетку следует принять в обычное время.
Если с тех пор, когда должна была быть принята очередная таблетка, прошло более 12 ч, контрацептивная защита может снизиться. В таком случае необходимо руководствоваться двумя основными правилами:
- перерыв в приеме таблеток никогда не может превышать 7 дней;
- адекватное угнетение системы гипоталамус — гипофиз — яичники достигается непрерывным приемом таблеток в течение 7 дней.
В соответствии с вышеизложенным в повседневной жизни следует руководствоваться нижеприведенными рекомендациями:
1-я неделя. Последняя пропущенная таблетка должна быть принята немедленно после того, как женщина об этом вспомнит, даже если придется принять 2 таблетки одновременно. Далее прием таблеток продолжается в обычном режиме. Кроме того, в течение следующих 7 дней дополнительно следует использовать барьерные методы контрацепции (например презерватив). Если в течение предыдущих 7 дней состоялся половой акт, следует учитывать возможность наступления беременности. Чем больше приемов таблеток пропущено и чем ближе пропуск к 7-дневному перерыву в приеме препарата, тем выше риск беременности.
2-я неделя. Последняя пропущенная таблетка должна быть принята немедленно после того, как женщина об этом вспомнит, даже если она должна принять 2 таблетки одновременно. Далее прием таблеток продолжается в обычном режиме. Если женщина правильно принимала таблетки в течение 7 дней перед пропуском первой таблетки, нет необходимости использовать дополнительные противозачаточные средства. В противном случае или при пропуске более одной таблетки рекомендуется дополнительно использовать барьерный метод контрацепции в течение 7 дней.
3-я неделя. Риск критического снижения контрацептивной защиты неизбежен из-за предстоящего 7-дневного перерыва в применении препарата. Однако при соблюдении схемы приема таблеток можно избежать снижения контрацептивной защиты. Если придерживаться одного из следующих вариантов, то не возникнет необходимости использовать дополнительные контрацептивные средства при условии правильного приема таблеток в течение 7 дней до пропуска. Если это не так, рекомендуется придерживаться первого из предложенных далее вариантов и использовать дополнительные методы контрацепции в течение следующих 7 дней.
1. Последняя пропущенная таблетка должна быть принята сразу же, как женщина об этом вспомнила, даже если следует принять 2 таблетки одновременно. Далее прием таблеток продолжается в обычном режиме. Таблетки из следующей упаковки пациентка должна начать принимать на следующий день после приема последней таблетки из текущей упаковки, то есть паузы между упаковками быть не должно. Маловероятно, что начнется менструальноподобное кровотечение до окончания приема таблеток из второй упаковки, хотя могут наблюдаться мажущие кровянистые выделения или прорывное кровотечение.
2. Женщине можно также посоветовать прекратить прием таблеток из текущей упаковки. В этом случае пациентка должна сделать перерыв в применении препарата продолжительностью до 7 дней, включая дни, в которые она забыла принять таблетки, а потом начать принимать таблетки из следующей упаковки препарата. Если женщина пропустила прием таблеток и после этого у нее отсутствует менструальноподобное кровотечение во время перерыва в применении препарата, следует рассмотреть вероятность беременности.
Рекомендации в случае нарушений со стороны ЖКТ. В случае тяжелых нарушений со стороны ЖКТ (рвоты или диареи) возможно неполное всасывание препарата, поэтому необходимо применять дополнительные средства контрацепции. Если в течение 3–4 ч после приема таблетки возникли рвота или тяжелая диарея, необходимо как можно быстрее принять новую таблетку. По возможности новую таблетку следует принять не позднее 12 ч после привычного времени приема. Если прошло более 12 ч, необходимо соблюдать правила приема препарата, указанные в разделе Что делать при пропуске приема таблеток.
Если женщина не хочет изменять свою обычную схему приема препарата, ей необходимо принять дополнительную(ые) таблетку(и) из другой упаковки.
Как сместить время наступления менструации или задержать менструацию. Для задержки менструального кровотечения прием таблеток Ригевидон из новой упаковки следует начать на следующий день после окончания текущей упаковки, без паузы между ними. Во время данного периода может проявиться прорывное кровотечение или мажущие выделения. Регулярное применение препарата Ригевидон может быть возобновлено после привычного 7-дневного перерыва. Чтобы сместить время наступления менструации на другой день недели, 7-суточный перерыв в применении препарата сокращают на желаемое количество дней. Чем меньше перерыв в применении препарата, тем вероятнее, что менструальноподобное кровотечение не возникнет, а прорывные или мажущие кровотечения будут появляться во время приема таблеток из следующей упаковки (как в случае задержки наступления менструации). Важно подчеркнуть, что перерыв в применении препарата увеличивать нельзя. Способ применения Перорально.
Противопоказания
комбинированные пероральные контрацептивы (КПК) не следует применять при наличии хотя бы одного из нижеуказанных состояний. Если любое из этих заболеваний или состояний возникает впервые во время применения КПК, его прием следует немедленно прекратить.
— Наличие или риск возникновения ВТЭ:
- ВТЭ в настоящее время, в частности вследствие терапии антикоагулянтами или в анамнезе (например тромбоз глубоких вен или тромбоэмболия легочной артерии;
- известная наследственная или приобретенная склонность к ВТЭ, такая как резистентность к активированному протеину С (в том числе мутация фактора V Лейдена), недостаточность антитромбина III, недостаточность протеина С, недостаточность протеина S;
- большое оперативное вмешательство с длительной иммобилизацией (см. ОСОБЫЕ УКАЗАНИЯ);
- высокий риск ВТЭ вследствие наличия множественных факторов риска (см. ОСОБЫЕ УКАЗАНИЯ).
— Наличие или риск развития артериальной тромбоэмболии (АТЭ):
- наличие АТЭ в настоящее время или в анамнезе (например инфаркт миокарда) или продромальное состояние (например стенокардия);
- цереброваскулярные заболевания — инсульт в настоящее время или в анамнезе, или продромальное состояние (например, транзиторная ишемическая атака;
- установлена наследственная или приобретенная склонность к АТЭ, такая как гипергомоцистеинемия и наличие антифосфолипидных антител (антикардиолипиновые антитела, волчаночный антикоагулянт);
- наличие в анамнезе мигрени с очаговыми неврологическими симптомами;
- высокий риск развития АТЭ вследствие наличия множественных факторов риска (см. ОСОБЫЕ УКАЗАНИЯ) или наличие одного из следующих серьезных факторов риска: сахарный диабет с сосудистыми осложнениями; тяжелая АГ; тяжелая дислипопротеинемия.
— Наличие панкреатита в настоящее время или в анамнезе, связанного с тяжелой гипертриглицеридемией.
— Наличие тяжелого заболевания печени в настоящее время или в анамнезе, пока показатели функции печени не нормализуются.
— Наличие опухолей печени в настоящее время или в анамнезе (доброкачественных или злокачественных).
— Известные или предполагаемые гормонозависимые злокачественные опухоли (например половых органов или молочных желез).
— Вагинальное кровотечение неустановленной этиологии.
— Повышенная чувствительность к действующим веществам (левоноргестрелу, этинилэстрадиолу) или какому-либо вспомогательному веществу (см. СОСТАВ).
— Противопоказан прием препарата Ригевидон в сочетании с препаратами зверобоя (Hypericum perforatum) (см. ВЗАИМОДЕЙСТВИЯ). Ригевидон противопоказан для одновременного применения с лекарственными средствами, которые содержат омбитасвир/паритапревир/ритонавир, дасабувир, глекапревир/пибрентасвир и софосбувир/велпатасвир/воксилапревир (см. ОСОБЫЕ УКАЗАНИЯ и ВЗАИМОДЕЙСТВИЯ).
Побочные эффекты
при одновременном применении этинилэстрадиола и левоноргестела сообщалось о побочных реакциях, указанных ниже. Самые серьезные побочные эффекты, такие как венозная и артериальная тромбоэмболия, рак шейки матки, рак молочной железы и злокачественные опухоли печени, описаны в разделе ОСОБЫЕ УКАЗАНИЯ.
У женщин, принимавших КГК, наблюдался повышенный риск развития артериальных или венозных тромботических и тромбоэмболических осложнений, в том числе инфаркта миокарда, инсульта, транзиторной ишемической атаки, венозного тромбоза и тромбоэмболии легочной артерии. Более подробная информация представлена в разделе ОСОБЫЕ УКАЗАНИЯ.
Таблица 1
| Система оранов | Частота возникновения побочных реакций | ||||
| Часто (≥1/100, <1/10) | Нечасто (≥1/1000, <1/100) | Редко (≥1/10 000, <1/1000) | Очень редко (<1/10 000) | Частота неизвестна (невозможно определить по имеющимся данным) | |
| Инфекционные и паразитарные заболевания | Вагинит, включая вагинальный кандидоз | ||||
| Доброкачественные, злокачественные и неуточненные новообразования (включая кисты и полипы) | Гепатоцеллюлярная карцинома, доброкачественные опухоли печени (очаговая узелковая гиперплазия, аденома печени) | ||||
| Со стороны иммунной системы | Повышенная чувствительность, анафилактические реакции с очень редкими случаями крапивницы, ангиодема, нарушения кровообращения и тяжелые нарушения дыхания | Обострение системной красной волчанки | Усиление симптомов наследственного и приобретенного ангионевротического отека | ||
| Со стороны обмена веществ и питания | Изменения в аппетите (повышение или снижение) | Нарушение толерантности к глюкозе | Обострение порфирии | ||
| Со стороны психики | Изменения настроения, включая депрессию, изменение либидо | ||||
| Со стороны нервной системы | Головная боль, повышенная возбудимость, головокружение | Мигрень | Обострение хореи | ||
| Со стороны органа зрения | Непереносимость контактных линз | Неврит зрительного нерва, тромбоз сосудов сетчатки | |||
| Со стороны сосудов | АГ | ВТЭ, АТЭ | Усиление варикозной болезни вен | ||
| Со стороны ЖКТ | Тошнота, рвота, боль в животе | Диарея, колики в животе, вздутие живота | Ишемический колит | Воспалительные заболевания кишечника (болезнь Крона, язвенный колит) | |
| Со стороны печени и желчевыводящих путей | Холестатическая желтуха | Панкреатит, конкременты в желчном пузыре, холестаз | Повреждение клеток печени (например гепатит, нарушение функции печени) | ||
| Со стороны кожи и подкожной клетчатки | Акне | Сыпь, крапивница, хлоазма (меланодермия) с риском персистирования, гирсутизм, выпадение волос | Узловатая эритема | Мультиформная эритема | |
| Со стороны почек и мочевыводящих путей | Гемолитико-уремический синдром | ||||
| Со стороны репродуктивной системы и молочных желез | Боль, напряженность, отек и выделения из молочных желез, дисменорея, нарушение менструального цикла, эктопия шейки матки и вагинальные выделения, аменорея | ||||
| Общие расстройства | Задержка жидкости/отеки, изменение массы тела (увеличение или уменьшение) | ||||
| Исследования | Изменение уровня липидов в сыворотке крови, включая гипертриглицеридемию | Снижение содержания фолатов в сыворотке крови | |||
У женщин, применяющих КПК, зарегистрированы следующие серьезные побочные реакции, которые описаны в разделе ОСОБЫЕ УКАЗАНИЯ:
— венозные тромбоэмболические расстройства;
— артериальные тромбоэмболические расстройства;
— АГ;
— опухоли печени;
— болезнь Крона, неспецифический язвенный колит, порфирия, системная красная волчанка, герпес беременных, хорея Сиденгама, гемолитический уремический синдром, холестатическая желтуха.
Частота диагностирования рака молочной железы у женщин, принимающих КПК, несколько повышена. Поскольку рак молочной железы у женщин в возрасте до 40 лет отмечают редко, увеличение количества случаев диагностирования рака молочной железы у женщин, применяющих сейчас или недавно применявших КПК, является незначительным по уровню общего риска рака молочной железы. Взаимосвязь с применением КПК неизвестна. Подробную информацию см. в разделах ПРОТИВОПОКАЗАНИЯ и ОСОБЫЕ УКАЗАНИЯ.
Экзогенные эстрогены могут вызывать или усиливать симптомы наследственного или приобретенного ангионевротического отека.
Взаимодействия. Прорывные кровотечения и/или снижение контрацептивного действия могут возникнуть из-за взаимодействия других лекарственных средств (индукторов ферментов) с пероральными контрацептивами.
Сообщения о подозреваемых побочных реакциях в период постмаркетингового наблюдения очень важны. Это дает возможность осуществлять контроль за соотношением польза/риск для лекарственных средств. Медицинские работники должны сообщать о подозреваемых побочных реакциях.
Особые указания
особые предупреждения. При наличии каких-либо заболеваний/факторов риска, указанных ниже, следует оценить благоприятные эффекты КПК и возможные риски их применения у конкретной женщины и обсудить с ней соответствующие пользу и риск до того, как она примет решение о применении таких препаратов. В случае первого проявления, увеличения выраженности или обострения какого-либо из этих заболеваний или факторов риска необходимо проконсультироваться с врачом. Врач должен решить вопрос о необходимости прекращения приема КПК.
Циркуляторные расстройства.
Риск возникновения ВТЭ. На фоне применения какого-либо КГК повышается риск развития ВТЭ (например, ТГВ или ТЭЛА) по сравнению с отсутствием применения. Применение препаратов, содержащих левоноргестрел, норгестимат или норэтистерон, ассоциируется с более низким риском ВТЭ. Решение о применении препарата Ригевидон следует принимать только после обсуждения с женщиной. Необходимо убедиться, что она осознает риск развития ВТЭ, связанный с применением препарата Ригевидон, степень влияния имеющихся у нее факторов риска на уровень вышеуказанного риска и тот факт, что риск ВТЭ является самым высоким в течение первого года применения препарата. По некоторым данным, риск ВТЭ может возрастать при возобновлении применения КГК после перерыва продолжительностью от 4 нед и более.
Среди женщин, не применяющих КГК и не являющихся беременными, частота возникновения ВТЭ составляет примерно 2 случая на 10 000 женщин в год. Однако у любой отдельно взятой женщины уровень риска может быть значительно выше, в зависимости от имеющихся у нее основных факторов риска (см. ниже).
Установлено, что из 10 000 женщин, применяющих КПК, содержащих левоноргестрел, примерно у 61 женщин разовьется ВТЭ в течение 1 года.
Количество случаев ВТЭ за год меньше обычного ожидается в течение беременности или в послеродовом периоде.
ВТЭ может приводить к летальным исходам в 1–2% случаев.
1В среднем 5–7 случаев на 10 000 женщин-лет на основе расчета относительного риска применения КГК, содержащих левоноргестрел, по сравнению с таковым у женщин, которые не получают КГК (примерно 2,3–3,6 случая). 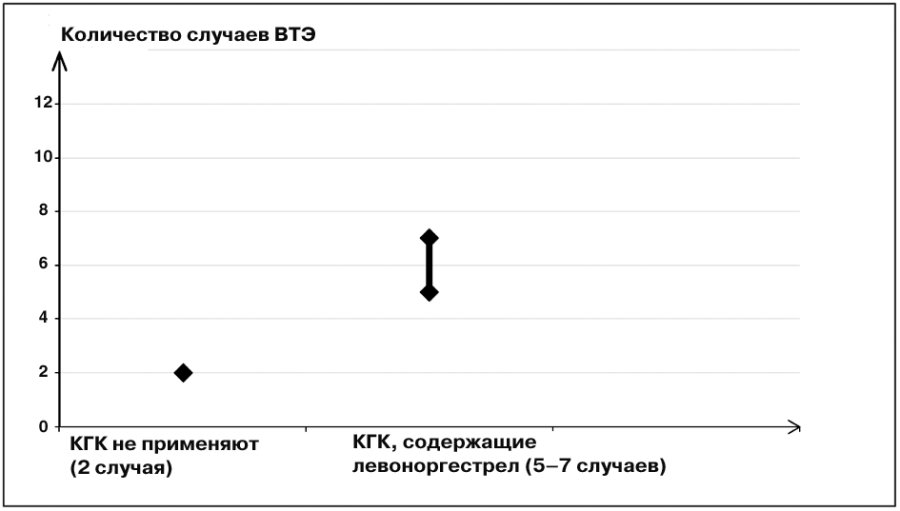
Рис. 1. Количество случаев ВТЭ на 10 000 женщин в год.
Очень редко сообщали о возникновении тромбоза в других кровеносных сосудах, например артериях и венах печени, почек, сетчатки или мезентериальных сосудах, у женщин, применяющих контрацептивные таблетки.
Факторы риска развития ВТЭ
На фоне применения КГК риск развития ВТЭ-осложнений может значительно повышаться у женщин с дополнительными факторами риска, особенно при наличии множественных факторов риска (табл. 2).
Препарат Ригевидон противопоказан женщинам с наличием множественных факторов риска, на основании которых ее можно отнести к группе высокого риска развития венозного тромбоза (см. ПРОТИВОПОКАЗАНИЯ). Если у женщины более чем один фактор риска, рост риска может быть больше, чем сумма рисков, ассоциированных с каждым отдельным фактором, в таком случае следует учитывать общий риск развития ВТЭ. КГК не назначают, если соотношение польза/риск оценивается как негативное (см. ПРОТИВОПОКАЗАНИЯ).
Таблица 2. Факторы риска развития ВТЭ
| Фактор риска | Примечание |
|---|---|
| Ожирение (индекс массы тела >30 кг/м2). | Риск значительно повышается при увеличении индекса массы тела. Особенно требует внимания наличие у женщин других факторов риска. |
| Длительная иммобилизация, большое оперативное вмешательство, любая операция на нижних конечностях или на органах малого таза, нейрохирургические вмешательства или большие травмы. Примечание: временная мобилизация, включая воздушный перелет больше 4 ч, также может быть фактором риска ВТЭ, особенно для женщин с другими факторами риска | В таких случаях рекомендуется прекратить применение пластыря/таблеток/вагинального кольца (в случае планового оперативного вмешательства — не менее чем за 4 нед) и не восстанавливать применение ранее чем через 2 нед после полного восстановления двигательной активности. Чтобы избежать нежелательной беременности, необходимо применять другие методы контрацепции. В том случае, если прием препарата Ригевидон не был прекращен заранее, рассматривают возможность проведения антитромботической терапии |
| Семейный анамнез (случаи ВТЭ у ближайших родственников — братьев, сестер или родителей, особенно в относительно молодом возрасте, то есть в возрасте до 50 лет) | Если возникает подозрение о наследственной предрасположенности, женщину необходимо направить на консультацию к специалисту до принятия решения о применении любого КГК |
| Другие состояния, связанные с ВТЭ | Рак, системная красная волчанка, гемолитико-уремический синдром, хроническое воспалительное заболевание кишечника (болезнь Крона или язвенный колит) и серповидно-клеточная анемия |
| Возраст | Особенно в возрасте старше 35 лет |
Нет единого мнения относительно возможного влияния варикозного расширения вен и поверхностного тромбофлебита на развитие или прогрессирование венозного тромбоза.
Следует также учитывать, что риск тромбоэмболических осложнений повышается в период беременности и в первые 6 нед после родов (см. Применение в период беременности или кормления грудью).
Симптомы ВТЭ (тромбоз глубоких вен и тромбоэмболия легочной артерии)
Женщины должны быть информированы о том, что в случае возникновения симптомов ВТЭ им следует обратиться за неотложной медицинской помощью и сообщить медицинскому работнику о применении КГК.
Симптомами тромбоза глубоких вен могут быть:
- односторонний отек ноги и/или стопы или участков вдоль вены на ноге;
- боль или повышенная чувствительность в ноге, может ощущаться только при стоянии или ходьбе;
- ощущение жара в пораженной ноге; покраснение или изменение цвета кожи на ноге.
Симптомами эмболии легочной артерии могут быть:
- внезапная одышка по неизвестной причине или учащенное дыхание;
- внезапный кашель без очевидной причины, возможно, с кровью;
- острая боль в грудной клетке;
- предобморочное состояние или головокружение;
- частое или неритмичное сердцебиение.
Некоторые из этих симптомов (например одышка, кашель) являются неспецифическими и могут быть ошибочно приняты за более распространенные или менее тяжелые заболевания (например инфекции дыхательных путей).
Другие признаки эмболии сосудов могут включать внезапную боль, отек и незначительное посинение конечности.
В случае эмболии сосудов глаза симптомы могут варьировать от нечеткости зрения (без болевых ощущений), которая может прогрессировать до потери зрения. Иногда полная потеря зрения развивается почти мгновенно.
Риск развития АТЭ
Результаты эпидемиологических исследований позволили ассоциировать применения КГК с повышенным риском развития АТЭ-осложнений (инфаркт миокарда) или нарушением мозгового кровообращения (например преходящее нарушение мозгового кровообращения, инсульт). Случаи АТЭ могут приводить к летальному исходу.
Факторы риска развития АТЭ
Риск развития АТЭ или нарушений мозгового кровообращения при применении КГК растет у женщин с факторами риска (табл. 3). Препарат Ригевидон противопоказан женщинам с одним серьезным фактором риска или множественными факторами риска развития АТЭ, на основе которых ее можно отнести к группе высокого риска развития артериального тромбоза (см. ПРОТИВОПОКАЗАНИЯ). Если женщина имеет более одного фактора риска, рост риска может быть больше, чем сумма рисков, ассоциированных с каждым отдельным фактором, поэтому необходимо учитывать общий риск развития АТЭ. КГК не следует назначать, если соотношение польза/риск оценивается как негативное (см. ПРОТИВОПОКАЗАНИЯ).
Таблица 3. Факторы риска развития АТЭ
| Фактор риска | Примечание |
|---|---|
| Возраст | Особенно в возрасте от 35 лет |
| Курение | Женщинам следует настойчиво рекомендовать отказаться от курения, если они хотят применять КГК. Женщинам в возрасте от 35 лет, не отказавшимся от курения, следует настойчиво рекомендовать другой метод контрацепции |
| АГ | |
| Ожирение (индекс массы тела >30 кг/м2) | Риск значительно повышается при увеличении индекса массы тела. Особенно требует внимания при наличии у женщин дополнительных факторов риска |
| Семейный анамнез (случаи АТЭ у ближайших родственников — братьев, сестер или родителей, особенно в относительно раннем возрасте, то есть в возрасте до 50 лет) | При подозрении на наследственную предрасположенность женщину необходимо направить на консультацию к специалисту до принятия решения по применению любого КГК |
| Мигрень | Повышение частоты или тяжести мигрени во время применения КГК (что может быть предвестником нарушения мозгового кровообращения) может стать обоснованием для немедленного прекращения применения КГК |
| Другие состояния, ассоциированные с нежелательными реакциями со стороны сосудов | Сахарный диабет, гипергомоцистеинемия, недостатки клапанов сердца и фибрилляция предсердий, дислипопротеинемия и системная красная волчанка |
Симптомы ATЭ
Женщин необходимо информировать о том, что в случае возникновения нижеприведенных симптомов им следует срочно обратиться за неотложной медицинской помощью и сообщить медицинскому работнику о применении КГК.
Симптомами нарушения мозгового кровообращения могут быть:
- внезапное онемение лица, слабость или онемение конечностей, особенно одностороннее;
- внезапное нарушение походки, головокружение, потеря равновесия или координации;
- внезапная спутанность сознания, нарушение речи или понимания;
- внезапное ухудшение зрения на один или оба глаза;
- внезапная сильная или продолжительная головная боль без определенной причины;
- потеря сознания или обморок с судорогами или без.
Временность симптомов может свидетельствовать о транзиторной ишемической атаке.
Симптомами инфаркта миокарда могут быть:
- боль, дискомфорт, давление, тяжесть, ощущение сжатия или распирания в груди, руке или
- за грудиной;
- дискомфорт с иррадиацией в спину, нижнюю челюсть, горло, руки, желудок;
- ощущение переполнения желудка, нарушения пищеварения или удушье;
- усиленное потоотделение, тошнота, рвота или головокружение;
- сильная слабость, беспокойство или одышка;
- быстрое или неритмичное сердцебиение.
Опухоли
Рак шейки матки. В некоторых эпидемиологических исследованиях сообщали о повышенном риске рака шейки матки у женщин, применявших КПК в течение длительного времени (>5 лет), однако это утверждение все еще противоречиво, поскольку окончательно не выяснено, насколько результаты исследований учитывают сопутствующие факторы риска, например половое поведение и инфицирование вирусом папилломы человека.
Рак молочной железы. Результаты метаанализа 54 эпидемиологических исследований свидетельствуют о незначительном повышении относительного риска (ОР=1,24) развития рака молочной железы у женщин, применяющих КГК. Этот повышенный риск постепенно исчезает в течение 10 лет после прекращения применения КГК. Поскольку рак молочной железы у женщин в возрасте до 40 лет отмечают редко, увеличение количества случаев диагностики рака молочной железы у женщин, применяющих в настоящее время или недавно применявших КГК, незначительное по уровню общего риска рака молочной железы. Результаты этих исследований не предоставляют доказательств существования причинно-следственной связи.
Повышение риска может быть обусловлено как более ранней диагностикой рака молочной железы у женщин, применяющих КГК, так и биологическим действием КГК или сочетанием обоих факторов. У женщин, применяющих пероральные контрацептивы, рак молочной железы диагностируется в более ранней стадии по сравнению с женщинами, не применявшими КГК.
Опухоли печени. В редких случаях у женщин, применяющих КГК, отмечали доброкачественные (аденома, очаговая узелковая гиперплазия), а еще реже — злокачественные опухоли печени. В отдельных случаях эти опухоли обусловливали внутрибрюшное кровотечение с угрозой для жизни. Следует иметь в виду наличие опухоли печени во время дифференциального диагностирования, когда у женщин, применяющих КГК, возникает серьезная боль в верхней части живота, увеличение печени или при появлении признаков внутрибрюшного кровоизлияния. Применение КГК в высоких дозах (50 мкг этинилэстрадиола) снижает риск рака эндометрия и яичников. Остается подтвердить, могут ли эти данные касаться и низкодозовых КПК.
Другие состояния
Депрессия. Депрессивное настроение и депрессия являются частыми побочными реакциями при применении гормональных контрацептивов (см. ПОБОЧНЫЕ ЭФФЕКТЫ). Депрессия может быть тяжелой и является известным фактором риска суицидального поведения и суицида. Женщин следует информировать о необходимости обратиться к врачу в случае перепадов настроения и симптомов депрессии, даже если они возникают вскоре после начала лечения.
Гипертриглицеридемия. У женщин с гипертриглицеридемией или семейным анамнезом гипертриглицеридемии при применении КГК следует учитывать возможное повышение риска развития панкреатита.
АГ. Хотя у многих женщин, принимающих КПК, было замечено незначительное повышение АД, клинически значимое повышение отмечается редко. Только в данных редких случаях немедленное прекращение применения КГК обоснованно. Если при применении КГК у пациентки с АГ постоянно повышается уровень АД или значительное повышение АД не отвечает в достаточной степени на противогипертоническое лечение, применение КГК следует прекратить. При необходимости прием КПК может быть восстановлен, если с помощью антигипертензивной терапии удалось достичь нормальных значений АД.
Заболевания печени. Острые или хронические нарушения функции печени могут требовать отмены КПК, пока показатели функции печени не нормализуются.
Ангиодема. Экзогенные эстрогены могут индуцировать или усугублять симптомы наследственного и приобретенного ангионевротического отека.
Толерантность к глюкозе/сахарный диабет. Несмотря на то что КГК могут влиять на периферическую инсулинорезистентность и толерантность к глюкозе, нет данных относительно необходимости изменять терапевтический режим у женщин, больных сахарным диабетом, принимающих низкодозированные КГК (содержащие <0,05 мг этинилэстрадиола). Однако женщины, больные сахарным диабетом, принимающие КГК, должны находиться под пристальным контролем.
Другие состояния. При рецидиве холестатической желтухи, впервые возникшей в период беременности или предварительного применения половых стероидных гормонов, применение КГК следует прекратить.
Поступали сообщения о развитии или обострении таких заболеваний при беременности и применении КГК (связь с применением КГК не выяснена): желтуха и/или зуд, связанный с холестазом; образование камней в желчном пузыре; порфирия; системная красная волчанка; гемолитико-уремический синдром; хорея Сиденгама; герпес беременных; потеря слуха, связанная с отосклерозом. При применении КГК наблюдалось усугубление течения эндогенной депрессии, эпилепсии, язвенного колита и болезни Крона.
Иногда может развиваться хлоазма (особенно у женщин с хлоазмой в период беременности в анамнезе). Женщинам со склонностью к хлоазме следует избегать воздействия солнечных лучей или ультрафиолетового излучения при применении КГК.
Особое внимание следует уделить пациенткам с гиперпролактинемией.
Медицинское обследование/консультация
До начала применения или повторного назначения препарата Ригевидон следует провести тщательный сбор анамнеза (включая семейный анамнез) и исключить беременность. Необходимо измерить АД, провести физикальное обследование, руководствуясь информацией о противопоказаниях (см. ПРОТИВОПОКАЗАНИЯ) и особыми предостережениями (см. ОСОБЫЕ УКАЗАНИЯ).
Важно обратить внимание женщин на риск возникновения венозного и артериального тромбоза, включая риск применения препарата Ригевидон по сравнению с другими КГК, на симптомы ВТЭ и АТЭ, а также установленные факторы риска и необходимые действия в случае подозрения на развитие тромбоза. Необходимо, чтобы женщина внимательно прочитала инструкцию по применению и придерживалась указанных в ней рекомендаций. Частота и характер осмотров должны основываться на существующих нормах медицинской практики с учетом индивидуальных особенностей каждой женщины.
Следует предупредить женщину, что гормональные контрацептивы не защищают от ВИЧ-инфекции (СПИДа) и других заболеваний, передающихся половым путем.
Снижение эффективности контрацепции
Эффективность КГК может снижаться в случае пропуска приема таблеток, расстройств желудочно-кишечного тракта (см. ПРИМЕНЕНИЕ) или при одновременном применении других лекарственных средств (см. ВЗАИМОДЕЙСТВИЯ).
Снижение контроля за циклом
Как и в случае со всеми КПК, могут развиться нерегулярные кровотечения (мажущие выделения или прорывные кровотечения), особенно в течение первых месяцев применения препарата, поэтому оценку любых нерегулярных кровотечений следует проводить только после завершения периода адаптации организма к препарату, что составляет примерно 3 цикла. Если нерегулярные кровотечения продолжаются или случаются после нескольких регулярных циклов, необходимо рассмотреть вопрос о негормональных причинах и провести соответствующие диагностические мероприятия для исключения злокачественных новообразований или беременности. Данные мероприятия могут включать кюретаж. У некоторых женщин может не наступить менструальное кровотечение во время привычного перерыва в приеме КПК. Если КПК применялись в соответствии с разделом ПРИМЕНЕНИЕ, то беременность маловероятна. Однако если указания раздела ПРИМЕНЕНИЕ перед первым отсутствием кровотечения отмены не были выполнены или если менструальное кровотечение отсутствует в течение двух циклов, то следует исключить беременность перед продолжением применения КПК.
Повышение уровня АлАТ
Известно, что в процессе клинических исследований у пациентов, получавших для лечения инфекций вирусного гепатита С лекарственные средства, содержащие омбитасвир/паритапревир/ритонавир и дасабувир с рибавирином или без него, выявлено повышение уровня АлАТ в более чем 5 раз выше верхней границы нормы, которое возникает чаще у женщин, получавших лекарственные средства, содержащие этинилэстрадиол, такие как КГК. Повышение уровня АлАТ также наблюдалось при применении противовирусных лекарственных средств, содержащих глекапревир/пибрентасвир и софосбувир/велпатасвир/воксилапревир (см. ПРОТИВОПОКАЗАНИЯ и ВЗАИМОДЕЙСТВИЯ).
Вспомогательные вещества. Ригевидон, таблетки, покрытые плёночной оболочкой, содержит лактозу, поэтому его не следует принимать женщинам с такими редкими наследственными заболеваниями, как непереносимость галактозы, лактазная недостаточность или синдром глюкозо-галактозной мальабсорбции.
Ригевидон, таблетки, покрытые плёночной оболочкой, содержит натрия кармелозу.
Одна таблетка, покрытая оболочкой, содержит менее 1 ммоль (23 мг)/дозу натрия, то есть лекарственное средство практически свободно от натрия.
Применение в период беременности и кормления грудью.
Беременность. Препарат Ригевидон противопоказан в период беременности. При наступлении беременности в период приема Ригевидона его следует немедленно отменить.
Результаты большого количества эпидемиологических исследований не выявили ни повышенного риска развития врожденных дефектов у детей, рожденных женщинами, применявшими КПК до беременности, ни тератогенного действия при непреднамеренном применении противозачаточных таблеток на ранних сроках беременности. При возобновлении применения препарата Ригевидон следует учитывать повышение риска развития ВТЭ в послеродовом периоде см. ПРИМЕНЕНИЕ и ОСОБЫЕ УКАЗАНИЯ).
Период кормления грудью. Пероральные гормональные контрацептивы могут оказывать влияние на лактацию, поскольку они могут снижать количество и изменять состав грудного молока. Ввиду этого применение КПК не рекомендуется до прекращения кормления грудью. Небольшие количества контрацептивных стероидов и/или метаболитов могут проникать в грудное молоко. Эти количества могут оказывать влияние на ребенка. Если женщина хочет кормить грудью, необходимо предложить ей другие средства контрацепции.
Дети. Препарат не предназначен для приема детьми.
Способность влиять на скорость реакции при управлении транспортными средствами и работе с другими механизмами. Исследования влияния на способность управлять транспортными средствами и другими механизмами не проводились. У женщин, применявших КГК, не наблюдалось какого-либо влияния на способность управлять транспортными средствами и механизмами.
Взаимодействия
следует ознакомиться с информацией относительно применяемого одновременно лекарственного средства для выявления потенциальных взаимодействий.
Взаимодействие между комбинированными контрацептивами и другими веществами может привести к увеличению или уменьшению концентрации эстрогена и гестагена в плазме крови.
Уменьшение концентрации эстрогена и прогестагена в плазме крови может привести к увеличению частоты межменструальных кровотечений и может снизить эффективность комбинированных контрацептивов.
Противопоказанные комбинации
Препараты зверобоя (Hypericum perforatum). Уменьшение концентрации гормональных контрацептивов в плазме крови из-за влияния препаратов зверобоя на индукцию ферментов, с последующим риском снижения или даже отсутствия эффективности, что может привести к серьезным последствиям (беременность).
Омбитасвир/паритапревир/ритонавир, дасабувир; глекапревир/пибрентасвир и софосбувир/велпатасвир/воксилапревир. Повышение гепатотоксичности.
Фармакодинамические взаимодействия
Одновременное применение с лекарственными средствами, содержащими омбитасвир/паритапревир/ритонавир, дасабувир, с рибавирином или без него, глекапревир/пибрентасвир и софосбувир/велпатасвир/воксилапревир, может повысить риск повышения АлАТ (см. ПРОТИВОПОКАЗАНИЯ И ОСОБЫЕ УКАЗАНИЯ). Поэтому пациенткам, принимающим Ригевидон, следует перейти на альтернативный метод контрацепции (например, контрацептивные препараты, содержащие только прогестаген или негормональные методы) до начала терапии вышеуказанными комбинированными препаратами. Применение препарата Ригевидон можно восстановить через 2 нед после завершения лечения.
Фармакокинетические взаимодействия
Воздействие других лекарственных средств на Ригевидон
Возможно взаимодействие с лекарственными средствами, индуцирующими микросомальные ферменты, в результате чего может увеличиваться клиренс половых гормонов и может возникнуть прорывное кровотечение и/или потеря эффективности контрацептива.
Терапия. Индукция ферментов может быть обнаружена уже через несколько дней лечения. Максимальная индукция ферментов в целом наблюдается спустя несколько недель. После отмены препарата индукция ферментов может длиться до 4 нед.
Краткосрочное лечение. Женщины, принимающие лекарственные средства, индуцирующие ферменты, должны временно использовать барьерный метод или другой метод контрацепции дополнительно к КПК. Барьерный метод контрацепции следует применять в течение всего периода лечения соответствующим препаратом и в течение 28 дней после прекращения его применения. Если терапия препаратом-индуктором продолжается после применения последних таблеток КПК из упаковки, содержащей 21 таблетку, прием таблеток из следующей упаковки КПК следует начать сразу после окончания предыдущего без перерыва в приеме.
Долгосрочное лечение. Женщинам при длительной терапии действующими веществами, индуцирующими ферменты печени, рекомендуется применять другой надежный негормональный метод контрацепции.
Следующие взаимодействия были зафиксированы согласно опубликованным данным.
Действующие вещества, увеличивающие клиренс КПК (снижение эффективности КПК из-за индукции ферментов), например барбитураты, бозентан, карбамазепин, фенитоин, примидон, рифампицин и препараты, применяемые для лечения ВИЧ-инфекции: ритонавир, невирапин и эфавиренз; также, возможно, фелбамат, гризеофульвин, окскарбазепин, топирамат и лекарственные средства, содержащие экстракт зверобоя (Hypericum perforatum).
Действующие вещества с непостоянным воздействием на клиренс КПК
При одновременном применении с КПК большое количество комбинаций ингибиторов ВИЧ-протеазы и ненуклеозидных ингибиторов обратной транскриптазы, включая комбинации с ингибиторами вируса гепатита C, могут повышать или снижать концентрацию эстрогена или прогестинов в плазме крови. Совокупное влияние таких изменений может оказаться клинически значимым в некоторых случаях. Поэтому для выявления потенциальных взаимодействий и любых других рекомендаций следует ознакомиться с информацией о медицинском применении лекарственного средства для лечения ВИЧ/вирусного гепатита С, принимаемого одновременно. При наличии каких-либо сомнений женщинам дополнительно следует использовать барьерный метод контрацепции при терапии ингибиторами протеазы или ингибиторами ненуклеозидной обратной транскриптазы.
Влияние препарата Ригевидон на другие лекарственные средства
КПК могут оказывать влияние на метаболизм других препаратов. Учитывая это, могут изменять концентрации действующих веществ в плазме крови и тканях — как повышать (например, циклоспорин), так и снижать (например, ламотриджин).
Нерекомендуемые комбинации
Индукторы ферментов
Противосудорожные лекарственные средства (фенобарбитал, фенитоин, фосфенитоин, примидон, карбамазепин, окскарбазепин), рифабутин, рифампицин, эфавиренц, невирапин, добрафениб, энзалутамид, эликарбазепин.
Снижение эффективности контрацептивов вследствие усиления печеночного метаболизма гормональных контрацептивов индуктором.
При применении этих комбинаций лекарственных средств и в течение следующего цикла рекомендуется использовать другой метод контрацепции, например механический.
Ламотриджин (см. также ниже Комбинации, требующие меры предосторожности при применении)
Риск снижения концентрации и эффективности ламотриджина в связи с усилением метаболизма в печени.
При подборе дозы ламотриджина не рекомендуется применять пероральные контрацептивы.
Ингибиторы протеаз в сочетании с ритонавиром
Ампренавир, атазанавир, даравир, фосампренавир, индинавир, лопинавир, ритонавир, саквинавир и типранавир. Риск снижения эффективности контрацепции за счет снижения концентрации гормональных контрацептивов в результате увеличения их метаболизма в печени с помощью ритонавира.
При применении этих комбинаций лекарственных средств и в течение следующего цикла рекомендуется использовать другой метод контрацепции, например презерватив или внутриматочную спираль.
Топирамат. Доза топирамата 200 мг/сут: риск снижения эффективности контрацепции из-за снижения концентрации эстрогена.
Рекомендуется использовать другой метод контрацепции, например механический.
Тролеандомицин. Может повысить риск внутрипеченочного холестаза при одновременном применении с КПК.
Модафинил. Существует риск снижения контрацептивного эффекта при приеме и в следующем цикле после прекращения приема модафинила, поскольку он является индуктором микросомальных ферментов печени.
Необходимо применять обычные пероральные контрацептивы (не низкодозированные) или другие методы контрацепции.
Вемурафениб. Существует риск снижения концентрации эстрогена и прогестагена с последующим риском отсутствия эффективности.
Перампанел. При применении перампанела в дозе, равной или превышающей 12 мг в сутки, существует риск снижения контрацептивного эффекта. Рекомендуется использовать другие методы контрацепции, преимущественно барьерные.
Улипристал. Существует риск угнетения прогестагена. Не следует восстанавливать прием комбинированных контрацептивов раньше, чем через 12 ч после прекращения приема улипристала.
Комбинации, требующие меры предосторожности при применении
Бозентан. Риск снижения эффективности контрацепции вследствие усиления метаболизма гормонального контрацептива в печени.
Следует использовать надежный, дополнительный или альтернативный метод контрацепции во время применения этой комбинации лекарственных средств и последующего цикла.
Гризеофульвин. Риск снижения эффективности контрацепции вследствие усиления метаболизма гормонального контрацептива в печени.
Желательно использовать другой метод контрацепции, особенно механический, во время применения этой комбинации лекарственных средств и последующего цикла.
Ламотриджин. Риск снижения концентрации и эффективности ламотриджина вследствие усиления метаболизма в печени.
Клинический мониторинг и адаптация дозирования ламотриджина в начале приема пероральных контрацептивов и после его прекращения.
Руфинамид. Приводит к умеренному снижению концентрации этинилэстрадиола. Рекомендуется использовать другие методы контрацепции, преимущественно барьерные.
Эльвитегравир. Снижены концентрации этинилэстрадиола с риском снижения контрацептивной эффективности. Кроме того, наблюдается повышение концентрации прогестагена.
Следует применять комбинированный контрацептив, содержащий не менее 30 мкг этинилэстрадиола.
Апрепитант. Снижение концентрации комбинированных контрацептивов или прогестагенов с риском снижения эффективности контрацепции.
Желательно использовать другой метод контрацепции, особенно механический, во время применения этой комбинации лекарственных средств и последующего цикла.
Боцепревир. Риск снижения эффективности контрацепции вследствие усиления печеночного метаболизма гормонального контрацептива боцепревиром.
Следует использовать надежный, дополнительный или альтернативный метод контрацепции во время применения этой комбинации лекарственных средств.
Телапревир. Риск понижения эффективности контрацепции вследствие усиления телапревиром печеночного метаболизма гормонального контрацептива.
Следует использовать надежный, дополнительный или альтернативный метод контрацепции при применении этой комбинации лекарственных средств и двух последующих циклов.
Комбинации, которые следует применять с осторожностью
Эторикоксиб. При одновременном применении с эторикоксибом наблюдается повышение концентрации этинилэстрадиола.
Лабораторные исследования
Применение контрацептивных стероидов может влиять на результаты отдельных лабораторных анализов, включая биохимические показатели функции печени, щитовидной железы, функции надпочечников и почек, а также уровень транспортных белков плазмы крови, таких как кортикостероидсвязывающий глобулин, и фракции липидов/липопротеинов; показатели углеводного обмена, коагуляции и фибринолиза. Изменения обычно происходят в пределах нормальных значений лабораторных показателей.
Передозировка
симптомы передозировки пероральных контрацептивов зарегистрированы у взрослых, подростков и детей в возрасте младше 12 лет.
Симптомы, которые могут наблюдаться при передозировке: тошнота, рвота, боль в грудных железах, головокружение, боль в животе, сонливость/слабость и вагинальное кровотечение у молодых девушек.
Антидотов не существует, лечение должно быть симптоматическим.
Условия хранения
при температуре не выше 25 °С. Хранить в недоступном для детей месте.
