Евра® пластир — трансдермальна терапевтична система №3
Евра інструкція із застосування
Склад
Діючі речовини: 1 пластир площею 20 см2 містить норелгестроміну 6,0 мг, етинілестрадіолу 0,60 мг;
кожен пластир протягом 24 год вивільняє 203 мкг норелгестроміну та 33,9 мкг етинілестрадіолу;
допоміжні речовини: адгезивна суміш поліізобутилену та полібутену, лауриллактат, кросповідон.
Норельгестромін - 6 мг
Етинілестрадіол - 0,6 мг
Фармакологічні властивості
фармакодинаміка. Евра® — контрацептив, що запобігає заплідненню завдяки механізму пригнічення гонадотропінів шляхом естрогенної і прогестагенної дії етинілестрадіолу та норелгестроміну. Первинний механізм дії полягає в інгібуванні овуляції, але зміни цервікального слизу та ендометрія також можуть посилювати ефективність препарату.
Таблиця 1
Індекси Перля
| Досліджувальна група | СONT-002 Евра | СONT-003 Евра | СONT-002 КПК* | СONT-002 Евра | СONT-002 КПК** | Всі пацієнти Евра |
| Кількість циклів | 10743 | 5831 | 4592 | 5095 | 4005 | 21669 |
| Індекс Перля (ДІ 95%) Загальний | 0,73 (0,15–1,31) | 0,89 (0,02–1,76) | 0,57 (0,0–1,35) | 1,28 (0,16–2,39) | 2,27 (0,59–3,96) | 0,90 (0,44–1,35) |
| Індекс Перля (ДІ 95%) Помилка методу | 0,61 (0,0–1,14) | 0,67 (0,0–1,42) | 0,28 (0,0–0,84) | 1,02 (0,02–2,02) | 1,30 (0,03–2,57) | 0,72 (0,31–1,13) |
* Дезогестрел 150 мкг + етинілестрадіол (ЕЕ) 20 мкг.
** Левоноргестрел 50 мкг + ЕЕ 30 мкг 1–6 дні, левоноргестрел 75 мкг + ЕЕ 40 мкг 7–11 дні, левоноргестрел 125 мкг + ЕЕ 30 мкг 12–21 дні.
Для визначення, чи пов’язані з вагітністю популяційні характеристики віку, раси та маси тіла, було проведено дослідницькі аналізи в дослідженнях III фази (n = 3319). Аналізи не показали ніякого зв’язку віку та раси пацієнтки з вагітністю. Щодо маси тіла, то 5 із 15 вагітностей, про які повідомлялося при застосуванні препарату Евра, були у жінок, початкова маса тіла яких дорівнювала або перевищувала 90 кг, що становило <3% досліджуваної популяції. При масі тіла менше 90 кг зв’язку між масою тіла та вагітністю не було. Хоча лише 10–20% варіабельності фармакокінетичних даних можна пояснити масою тіла (див. Фармакокінетика), більша частка вагітностей у жінок із масою тіла 90 кг або більше була статистично значущою, що вказує на те, що Евра менш ефективний у цих жінок.
При застосуванні більш високих доз КПК (50 мкг етинілестрадіолу) знижується ризик раку ендометрія та яєчників. Чи це також стосується комбінованих гормональних контрацептивів із меншою дозою, ще належить підтвердити.
Фармакокінетика.
Абсорбція. Рівноважна концентрація (плато) норелгестроміну та етинілестрадіолу у плазмі крові досягається приблизно через 48 год після аплікації пластиру (ТТС) Евра®. Стабільний рівень концентрації норелгестроміну та етинілестрадіолу протягом 1 тиж застосування пластиру становить майже 0,8 нг/мл i 50 пг/мл відповідно. При тривалому застосуванні трансдермального пластиру (ТТС) Евра® концентрації у плазмі крові (Css) i AUC незначною мірою збільшуються відносно концентрацій на 1-му тижні 1-го циклу.
Абсорбція норелгестоміну та етинілестрадіолу після наклеювання пластиру (ТТС) Евра® досліджувалися в умовах спортивного клубу (сауна, джакузі, бігова доріжка та інші вправи з аеробіки), а також у ванні з холодною водою. Результати свідчили, що для норелгестроміну не було суттєвих змін у Css і AUC порівняно з такими при звичайному способі життя. Для етинілестрадіолу ці значення дещо збільшувалися при фізичному навантаженні; однак рівень Css був у межах референтних значень. Холодна вода не впливала на ці параметри.
Результати дослідження застосування одного контрацептивного трансдермального пластиру (ТТС) Евра® впродовж 7 та 10 днів показали, що цільові значення Css норелгестроміну та етинілестрадіолу підтримувалися протягом 3 днів продовженого застосування пластиру (ТТС) Евра® (10 днів), тобто клінічна ефективність ТТС зберігається, навіть якщо жінка проведе чергову заміну пластиру (ТТС) Евра® на 2 повних дні пізніше запланованого терміну.
Розподіл. Норелгестромін і норгестрел (метаболіт норелгестроміну у плазмі крові) мають високий ступінь (>97%) зв’язування з білками плазми крові. Норелгестромін зв’язується з альбуміном, норгестрел — переважно з глобулінами, що зв’язують статеві гормони. Етинілестрадіол має високий ступінь зв’язування з альбуміном плазми крові.
Біотрансформація. Норелгестромін метаболізується у печінці з утворенням метаболіту норгестрелу, що переважно зв’язується з глобуліном, що зв’язує статеві гормони, а також різних гідроксильованих і кон’югованих метаболітів. Етинілестрадіол метаболізується до різних гідроксильованих продуктів і їх глюкуронідів та сульфатних кон’югатiв.
Елімінація. Після зняття пластиру середній Т½ норелгестроміну та етинілестрадіолу становить майже 28 i 17 год відповідно. Метаболіти норелгестроміну та етинілестрадіолу елімінуються з сечею та калом.
Трансдермальні та пероральні контрацептивні засоби. Фармакокінетичні профілі трансдермальних і пероральних комбінованих контрацептивів різні, і слід дотримуватися обережностi при методі прямого співставлення фармакокінетичних параметрів. У ході порівняння пластиру (ТТС) Евра® та пероральних контрацептивів, що містили норгестимат (попередник норелгестроміну) 250 мкг/етинілестрадіол 35 мкг, значення Сmax були у 2 рази вищі для норелгестроміну та етинілестрадіолу у піддослідних, які приймали пероральні контрацептиви, порівняно з відповідними показниками у групі Евра®, тоді як загальна експозиція (AUC та Css) були подібними у піддослiдних, які застосовували пластир (ТТС) Евра®. Міжсуб’єктна варіабельність (%СV) для фармакокінетичних параметрів доставки норелгестромiну та етинілестрадіолу від пластиру (ТТС) Евра® була вище відносно варіабельності, встановленої від пероральних контрацептивів.
Вплив вікy, маси тіла і площі поверхні тіла на фармакокінетику норелгестроміну та етинілестрадіолу вивчали з участю 230 жінок у ході 9 фармакокінетичних досліджень разового 7-денного застосування пластиру (ТТС) Евра®. Значения Css i AUC норелгестроміну і етинілестрадіолу незначною мірою знижуються зі збiльшенням віку, маси тіла і площі поверхні тіла. Однак лише мала частина (10–20%) загальної варіабельності фармакокінетики норелгестроміну та етинілестрадіолу наступного застосування пластиру (ТТС) Евра® може бути пов’язана з одним із вищезазначених параметрів.
Показання Евра
контрацепція у жінок.
Евра® показаний до застосування жінкам репродуктивного віку. Безпека та ефективність пластиру ТТС Евра® встановлені лише для жінок віком 18–45 років.
Рішення про призначення препарату Евра® повинно враховувати поточні фактори ризику для кожної жінки, особливо щодо венозної тромбоемболії (ВТЕ), з урахуванням ризику ВТЕ при застосуванні Евра® у порівнянні з іншими комбінованими гормональними контрацептивами (КГК) (див. ПРОТИПОКАЗАННЯ, ОСОБЛИВОСТІ ЗАСТОСУВАННЯ).
Застосування Евра
дози.
Для досягнення максимального контрацептивного ефекту жінка повинна застосовувати пластир (ТТС) Евра®, суворо дотримуючись інструкцій, що наведені нижче у розділі Як розпочати застосування пластиру (ТТС) Евра®.
Одночасно можна використовувати лише 1 пластир (ТТС) Евра®.
Кожен використаний пластир (ТТС) Евра® знімати та одразу замінювати новим в один і той же день тижня — «день заміни» — на 8-й і 15-й дні менструального циклу. Заміну використаного пластиру можна проводити у будь-який час «дня заміни». Протягом 4-го тижня, з 22-го дня циклу, пластир (ТТС) Евра® не застосовувати.
Новий контрацептивний цикл розпочинається з наступного дня після закінчення 4-го тижня; наступний пластир (ТТС) Евра® слід наклеювати, навіть якщо кровотечі відміни не було або вона не закінчилася.
Ні за яких обставин перерва у використанні пластиру (ТТС) Евра® не повинна перевищувати 7 днiв. Якщо відбулася перерва довше 7 днів, жінка може бути не захищена від настання вагітності. У таких випадках протягом 7 днів необхідно додатково використовувати бар’єрний метод контрацепції, оскільки ризик овуляції зростає з кожним днем збільшення рекомендованої тривалості періоду, вільного від застосування пластиру (ТТС) Евра®. У разі статевих зносин під час такого періоду слід враховувати імовірніcть зачаття.
Особливі категорії пацієнтів.
Маса тіла 90 кг або більше: у жінок з масою тіла 90 кг і більше ефективність контрацепції може бути знижена.
Ниркова недостатність: застосування лікарського засобу Евра® жінкам із нирковою недостатністю не вивчалося. Потреби знижувати дозу немає, проте дані свідчать про більш високий рівень незв’язаної фракції етинілестрадіолу, тому препарат Евра® цій категорії пацієнтів слід застосовувати під контролем.
Печінкова недостатність: застосування препарату Евра® жінкам із печінковою недостатністю не вивчалося. Евра® протипоказана жінкам із печінковою недостатністю (див. розділ ПРОТИПОКАЗАННЯ).
Пацієнти літнього віку: Евра® не призначена для застосування в якості гормональної замісної терапії жінкам у період постменопаузи.
Діти: безпека та ефективність пластиру (ТТС) Евра® встановлена для жінок віком від 18 років. Не рекомендується застосовувати Евра® до настання першої менструації.
Спосіб застосування. Пластир (ТТС) Евра® слід наклеювати на чисту, суху, інтактну і здорову шкіру сідниць, живота, зовнішню поверхню верхньої частини плеча або верхньої частини тулуба без оволосіння, на ділянках, де вона не буде контактувати з одягом, який щільно прилягає до тіла. Пластир (ТТС) Евра® не можна приклеювати на груди або ділянки шкіри з почервонінням, подразненням або порізами. Щоб уникнути можливого подразнення, кожен наступний пластир (ТТС) Евра® необхідно наклеювати на іншу ділянку шкіри, це можна робити у межах однієї і тієї самої анатомічної ділянки.
Пластир (ТТС) Евра® необхідно щільно притиснути, щоб його краї добре прилягали до шкіри.
Для запобігання зниженню адгезивних властивостей пластиру (ТТС) Евра® не можна наносити макіяж, креми, лосьйони, пудри та інші локальні засоби на ті ділянки шкіри, де він приклеєний або буде приклеєним.
Жінка повинна щоденно оглядати трансдермальний пластир для того, щоб бути впевненою в його щільному приклеюванні.
Пластир (ТТС) Евра® не можна розрізати, пошкоджувати або змінювати будь-яким чином, оскільки це може поставити під загрозу ефективність контрацепції.
Використаний трансдермальний пластир необхідно утилізувати відповідно до інструкцій, наведених у розділі Особливі заходи безпеки.
Як розпочати застосування пластиру (ТТС) Евра®?
Якщо під час попереднього менструального циклу жінка не застосовувала гормональний контрацептив. Контрацепцію за допомогою пластиру (ТТС) Евра® розпочинати у 1-й день менструації. Приклеювати до шкіри 1 пластир (ТТС) Евра® і носити його весь тиждень (7 днів). День приклеювання першого пластиру (ТТС) Евра® (l-й день/день початку) визначає наступні дні заміни. День заміни буде приходитися на цей самий день кожного тижня (8-й, 15-й, 22-й дні циклу та 1-й день наступного циклу). На 22-й день циклу пластир Евра® знімати, і протягом четвертого тижня циклу жінка не застосовує пластир (ТТС) Евра®.
Якщо жінка розпочинає застосування трансдермального пластиру (ТТС) Евра® не з першого дня циклу, то слід одночасно використовувати бар’єрні методи контрацепції протягом 7 перших днів першого контрацептивного циклу.
Якщо жінка переходить із застосування комбінованого перорального контрацептиву (КПК) на використання пластиру (ТТС) Евра®. Пластир (ТТС) Евра® слід наклеювати на шкіру у 1-й день менструації, що розпочинається після припинення прийому КПК. Якщо протягом 5 днiв після прийому контрацептивної таблетки менструація не розпочинається, перед початком застосування пластиру (ТТС) Евра® необхiдно виключити вагітність. Якщо застосування Евра® розпочати пізніше першого дня менструації, то протягом 7 днів необхідно одночасно використовувати бар’єрні методи контрацепції.
Якщо після прийому останньої контрацептивної таблетки пройшло більше 7 днів, то у жінки може виникнути овуляція, і тому вона повинна проконсультуватися з лікарем перед тим, як розпочати застосування пластиру (ТТС) Евра®. Статеві зносини під час цього збільшеного періоду, вільного від прийому контрацептивних таблеток, можуть призвести до настання вагітності.
Якщо жінка переходить із застосування препаратів, що містять лише прогестаген, на застосування пластиру (ТТС) Евра®. Жінка може у будь-який день перейти із застосування препарату, що містить лише прогестаген (у день видалення імплантату, в день, коли потрібно зробити чергову ін’єкцію), на застосування пластиру (ТТС) Евра®, але протягом перших 7 днів застосування пластиру (ТТС) Евра® слід використовувати бар’єрний метод для посилення контрацептивного ефекту.
Після аборту або викидня до 20-го тижня вагітності можна одразу розпочинати застосування пластиру (ТТС) Евра®. Якщо жінка починає використовувати пластир (ТТС) Евра® одразу після аборту або викидня, застосовувати додатковий метод контрацепції не обов’язково. Жінка повинна знати, що овуляція може відбутися протягом 10 днів після аборту або викидня.
Після аборту або викидня на 20-му тижні вагітності і пізніше застосування пластиру (ТТС) Евра® можна розпочинати на 21-й день після аборту або викидня або у перший день першої менструації. Частота виникнення овуляції на 21-й день після аборту (на 20-му тижні вагітності) невідома.
Після пологів. Жінки, які не годують дитину грудьми, можуть розпочинати застосування пластиру (ТТС) Евра® не раніше ніж через 4 тиж після пологів. Якщо жінка починає застосовувати пластир (ТТС) Евра® пізніше, то протягом перших 7 днів слід додатково використовувати бар’єрний метод контрацепції. Якщо були статеві зносини, то необхідно виключити імовірність вагітності перед тим, як розпочинати застосування пластиру (ТТС) Евра®, або жінка повинна дочекатися першої менструації.
Щодо застосування пластиру жінкам, що годують грудьми, див. розділ Застосування у період вагітності або годування грудьми.
При повному або частковому відклеюванні пластиру (ТТС) Евра®.
Якщо пластир (ТТС) Евра® повністю або частково відклеївся, то у кров надходить недостатня кількість його активних компонентів.
Навіть при частковому відклеюваннi пластиру (ТТС) Евра®:
– менш ніж протягом доби (24 год) слід знову приклеїти пластир (ТТС) Евра® на ту саму ділянку тіла або одразу ж замінити його новим трансдермальним пластирем (ТТС) Евра®. Додаткові контрацептиви не потрібні. Наступний пластир Евра® необхідно приклеїти у звичайний «день заміни»;
– більш ніж протягом доби (24 год), а також якщо жінка не знає точно, коли пластир (ТТС) Евра® частково або повністю відклеївся: можливе настання вагітності. Жінка повинна одразу ж почати новий цикл, наклеївши новий пластир (ТТС) Евра®, і вважати цей день першим днем контрацептивного циклу. Бар’єрні методи контрацепції слід одночасно застосовувати лише у перші 7 днів нового циклу.
Не слід намагатися приклеїти пластир (ТТС) Евра®, якщо він втратив свої адгезивні властивості; заміcть цього необхідно одразу приклеїти новий пластир (ТТС) Евра®. Не можна застосовувати додаткові липкі стрічки або пов’язки для утримання на місці пластиру (ТТС) Евра®.
Якщо пропущені чергові дні заміни пластиру (ТТС) Евра®.
• На початку будь-якого контрацептивного циклу (1-й тиждень/1-й день): жінка може бути не захищена від вагітності: вона повинна приклеїти перший пластир (ТТС) Евра® нового циклу одразу ж, як тільки згадає про це. Цей день вважається новим «1-м днем» і від нього відраховується новий «день заміни». Протягом перших 7 днiв нового циклу слід одночасно застосовувати негормональну контрацепцію. У разі статевих зносин під час такого подовженого періоду без застосування пластиру (ТТС) Евра® може відбутися запліднення.
• У середині циклу (2-й тиждень/8-й день або 3-й тиждень/15-й день):
– якщо від дня заміни пластиру пройшла 1 або 2 доби (до 48 год), жінка повинна одразу наклеїти новий пластир (ТТС) Евра®. Наступний пластир (ТТС) Евра® необхідно приклеїти у звичайний «день заміни». Якщо протягом 7 днів, що передують першому пропущеному дню наклеювання пластиру (ТТС) Евра®, жінка правильно використовувала пластир, то додаткова контрацепція не потрібна;
– якщо від дня заміни пластиру пройшло більше 2 діб (48 год і більше), жінка може бути не захищена від настання вагітності. Вона повинна припинити поточний контрацептивний цикл і одразу ж розпочати новий 4-тижневий цикл, наклеївши новий пластир (ТТС) Евра®. Цей день вважається новим «1-м днем» і відраховується від нього «день заміни». Бар’єрну контрацепцію слід одночасно застосовувати протягом 7 перших днів нового циклу.
• Наприкінці циклу (4-й тиждень/22-й день): якщо трансдермальний пластир (ТТС) Евра® не знято у кінці 4-го тижня (22-й день), його необхідно зняти якнайшвидше. Черговий цикл контрацепції потрібно розпочинати у звичайний «день заміни», який є наступним днем після 28-го дня. Додаткова контрацепція не потрібна.
Зміна «дня заміни».
Щоб відкласти менструацію на один цикл, жінка повинна приклеїти новий пластир Евра® на початку 4-го тижня (22-й день), пропустивши тим самим період, вільний від застосування пластиру Евра®. Можуть виникнути міжменструальні кровотечі або мажучі виділення. Після 6 тиж поспіль застосування пластиру (ТТС) Евра® необхідно зробити 7-денний інтервал, вільний від застосування пластиру (ТТС) Евра®. Після закінчення цього інтервалу відновити регулярне застосування препарату.
Якщо жінка хоче змінити день заміни пластиру, вона повинна закінчити поточний цикл, зняти третій пластир (ТТС) Евра® у призначений для цього день. Протягом тижня, вільного від застосування пластиру (ТТС) Евра®, жінка може вибрати новий день заміни, наклеївши перший пластир (ТТС) Евра® наступного циклу в обраний день. Період, вільний від застосування пластиру (ТТС) Евра®, ні в якому разі не повинен перевищувати 7 днів. Чим коротший цей період, тим вища імовірність того, що у жінки не буде наступної менструації, а під час наступного контрацептивного циклу можуть виникати міжменструальні кровотечі або мажучі виділення.
При незначному подразненні шкіри. Якщо застосування пластиру (ТТС) Евра® спричиняє подразнення шкіри, можна приклеїти новий пластир Евра® на іншу ділянку шкiри і носити його до наступного «дня заміни». Одночасно можна застосовувати лише 1 пластир Евра®.
Діти. Пластир (ТТС) Евра® не рекомендується застосовувати дітям (до 18 років) через недостатність даних щодо безпеки та ефективності застосування. Не рекомендується застосовувати лікарський засіб Евра® до настання першої менструації.
Протипоказання
КГК не можна застосовувати при наявності одного з нижченаведених станів. Якщо будь-який з цих станів виникає під час застосування лікарського засобу Евра®, його застосування слід негайно припинити.
• ВТЕ або ризик її розвитку:
– ВТЕ (з лікуванням антикоагулянтами) або ВТЕ в анамнезі (тромбоз глибоких вен (ТГВ) або емболія легень);
– cпадкова або набута схильність до ВТЕ, наприклад резистентність до активованого протеїну С (включаючи фактор V Ляйдена), недостатність антитромбіну ІІІ, протеїну С, протеїну S;
– обширне оперативне втручання з тривалою іммобілізацією (див. ОСОБЛИВОСТІ ЗАСТОСУВАННЯ);
– підвищений ризик ВТЕ внаслідок наявності множинних факторів ризику (див. ОСОБЛИВОСТІ ЗАСТОСУВАННЯ).
• Артеріальна тромбоемболія (АТЕ) або ризик її розвитку:
– АТЕ, у тому числі в анамнезі (наприклад, інфаркт міокарда), або продромальна стадія тромбозу (наприклад, стенокардія);
– цереброваскулярні захворювання: гострі порушення мозкового кровообігу, інсульт в анамнезі або продромальна стадія тромбозу (наприклад, транзиторна ішемічна атака);
– спадкова або набута схильність до артеріального тромбозу, наприклад гіпергомоцистеїнемія та антифосфоліпідні антитіла (антикардіоліпін-антитіла, вовчаковий антикоагулянт);
– мігрень з фокальними неврологічними симптомами в анамнезі;
– підвищений ризик АТЕ внаслідок наявності множинних факторів ризику (див. ОСОБЛИВОСТІ ЗАСТОСУВАННЯ) або одного з перелічених нижче серйозних факторів ризику:
• цукровий діабет із судинними симптомами;
• тяжка АГ;
• тяжка дисліпопротеїнемія.
• Підвищена чутливість до діючих речовин препарату або до будь-якої з допоміжних речовин.
• Підтверджена або підозрювана карцинома молочних залоз.
• Рак ендометрія або інші підтверджені або підозрювані естрогензалежні новоутворення.
• Порушення функції печінки внаслідок гострої або хронічної гепатоцелюлярної хвороби.
• Аденома або карцинома печінки.
• Недіагностована генітальна кровотеча.
• Одночасне застосування з лікарськими засобами, що містять омбітасвір/паритапревір/ритонавір та дасабувір, лікарськими засобами, що містять глекапревір/пібрентасвір або софосбувір/велпатасвір/воксилапревір (див. розділи ОСОБЛИВОСТІ ЗАСТОСУВАННЯ та ВЗАЄМОДІЯ З ІНШИМИ ЛІКАРСЬКИМИ ЗАСОБАМИ).
Побічна дія
найчастішими побічними реакціями, що спостерігалися під час клінічних досліджень, були головний біль, нудота та чутливість молочних залоз, які розвивалися приблизно у 21%, 16,6% та 15,9% випадків відповідно. Побічні реакції, що можуть з’являтися на початку лікування, але зазвичай зникають після перших трьох циклів, включають мажучі виділення, нагрубання молочних залоз та нудоту.
У жінок, які застосовують КГК, спостерігається підвищений ризик артеріальних та венозних тромботичних та тромбоемболічних порушень, включаючи інфаркт міокарда, інсульт, транзиторні ішемічні атаки, тромбоз вен та емболію легень (див. ОСОБЛИВОСТІ ЗАСТОСУВАННЯ).
Безпека пластиру (ТТС) Евра® оцінювалася з участю 3322 жінок, які вели активне статеве життя та брали участь у клінічних дослідженнях ІІІ фази, що проводилися з метою оцінки контрацептивної ефективності. Ці жінки застосовували контрацепцію впродовж 6 або 13 циклів (пластир (ТТС) Евра® або пероральний контрацептив для порівняння), прийняли хоча б одну дозу досліджуваного препарату та надали інформацію щодо побічних реакцій. У табл. 1 зазначені побічні реакції, що спостерігалися під час клінічних досліджень та у постмаркетинговому періоді. Частота побічних реакцій оцінена як дуже часто (≥1/10); часто (≥1/100 до <1/10); нечасто (≥ 1/1000 до <1/100); рідко (≥ 1/10 000 до <1/1000); дуже рідко (<1/10 000), невідомо (не може бути встановлена з доступних даних).
Таблиця 1
Частота побічних реакцій
| Системи органів/частота | ||||
| Дуже часто | Часто | Нечасто | Рідко | Невідомо |
| Інфекції та інвазії | ||||
| (Вульво)вагінальні грибкові інфекції, вагінальний кандидоз | Пустульозні висипи*, пустули у місці застосування | |||
| Доброякісні новоутворення, злоякісні та невстановлені (включаючи кісти та поліпи) | ||||
| Печінкові новоутворення*†, рак молочної залози*†, рак шийки матки*†, печінкова аденома*†, маткова лейоміома, фіброаденома молочної залози | ||||
| З боку імунної системи | ||||
| Реакції гіперчутливості | Анафілактичні реакції* | Загострення симптомів спадкового та набутого ангіоневротичного набряку* | ||
| Метаболічні порушення | ||||
| Гіперхолестеринемія, затримка рідини, підвищення апетиту | Гіперглікемія*, резистентність до інсуліну* | |||
| Психічні розлади | ||||
| Зміни настрою, лабільність емоційних реакцій, занепокоєння | Безсоння, зниження лібідо | Агресія*, засмученість*, підвищення лібідо | ||
| З боку центральної та периферичної нервової системи | ||||
| Головний біль | Мігрень, запаморочення | Гострі порушення мозкового кровообігу**†, мозкова кровотеча*†, спотворення смаку* | ||
| З боку органів зору | ||||
| Непереносимість контактних лінз* | ||||
| З боку серця | ||||
| Артеріальна тромбоемболія, (гострий) інфаркт міокарда*† | ||||
| З боку судинної системи | ||||
| Артеріальна гіпертензія | Гіпертензивний криз*, артеріальний тромбоз**†, венозний тромбоз**†, тромбоз*†, венозна тромбоемболія | |||
| З боку дихальної системи | ||||
| Легеневий (артеріальний) тромбоз*†, легенева емболія† | ||||
| З боку травної системи | ||||
| Нудота | Біль у животі, блювання, діарея, здуття живота | Коліт* | ||
| З боку гепатобіліарної системи | ||||
| Холецистит, холелітіаз†, ураження печінки*, холестатична жовтяниця*†, холестаз*† | ||||
| З боку шкіри та підшкірної тканини | ||||
| Акне, висипання, свербіж, шкірні реакції, подразнення шкіри | Алопеція, алергічний дерматит, екзема, реакції фоточутливості, контактний дерматит, кропив’янка, еритема | Ангіоневротичний набряк*, еритема (мультиформна, вузликова)*, хлоазма†, ексфоліативні висипання*, генералізований свербіж, висипання (еритематозні, свербіжні), себорейний дерматит* | ||
| З боку кістково-м’язової системи | ||||
| Спазми м’язів | ||||
| З боку репродуктивної системи | ||||
| Нагрубання молочних залоз | Дисменорея, маткові кровотечі та менструальні розлади**†, спазм матки, дискомфорт у грудях, вагінальні розлади | Галакторея, передменструальний синдром, вульвовагінальна сухість | Дисплазія шийки матки*, погіршення лактації, генітальні виділення | |
| Загальні розлади та реакції у місці введення | ||||
| Нездужання, підвищена втомлюваність, реакції у місці застосування (еритема, подразнення, свербіж, висипання) | Генералізований набряк, периферичний набряк, реакції у місці застосування** | Набряк обличчя*, точковий набряк*, набряки, реакції у місці застосування* (абсцес, ерозія), локалізований набряк* | ||
| Результати лабораторних досліджень | ||||
| Збільшення маси тіла | Підвищення артеріального тиску, порушення рівня тригліцеридів крові** | Зниження рівня глюкози крові*†, порушення рівня глюкози крові*† | ||
*Побічні реакції, виявлені у післяреєстраційний період.
**Включаючи побічні реакції, виявлені у ході клінічних досліджень та післяреєстраційного періоду.
†Див. ОСОБЛИВОСТІ ЗАСТОСУВАННЯ.
Особливості застосування
якщо присутній будь-який із зазначених нижче станів/факторів ризику, слід розглянути користь від застосування лікарського засобу Евра® та можливі ризики для кожної жінки індивідуально та обговорити з жінкою перед тим, як вона вирішить розпочати застосовувати пластир Евра®.
Жінці слід пояснити, що у разі погіршення, загострення або появи одного з цих станів або факторів ризику їй необхідно звернутися до лікаря, який вирішить, чи варто припиняти застосування препарату.
Немає клінічних доказів того, що трансдермальний пластир у будь-якому аспекті є безпечнішим за КПК.
Лікарський засіб Евра® не показаний у період вагітності (див. Застосування у період вагітності або годування грудьми).
Ризик ВТЕ. Застосування будь-якого КГК, у тому числі лікарського засобу Евра®, підвищує ризик ВТЕ порівняно з тим, коли такі препарати не застосовують. Засоби, які містять левоноргестрел, норгестимат або норетистерон асоціюються з найменшим ризиком ВТЕ. Інші засоби, такі як Евра®, можуть мати вдвічі вищий рівень ризику розвитку ВТЕ. Рішення про застосування лікарського засобу слід приймати тільки після обговорення з жінкою, впевнившись у тому, що вона усвідомлює ризик розвитку ВТЕ при застосуванні пластиру Евра® і розуміє, як наявні у неї фактори ризику впливають на цей ризик і що ризик ВТЕ є найвищим протягом першого року використання пластиру. Існують також деякі свідчення того, що ризик зростає, коли КПК призначають повторно після перерви у використанні 4 тиж і більше.
Приблизно у 2 з 10 000 жінок, які не застосовують КГК і не вагітні, розвивається ВТЕ протягом 1 року. Проте у кожної жінки цей ризик може бути набагато вищим залежно від наявних у неї факторів ризику (див. нижче).
Встановлено, що з 10 000 жінок, які застосовують низькі дози КГК, що містять левоногестрел, приблизно у 6 розвивається ВТЕ протягом 1 року. Дослідження дозволяють припустити, що частота розвитку ВТЕ у жінок, які застосовують пластир Евра®, є у 2 рази вищою порівняно з тими, які застосовують левоноргестрелвмісні контрацептиви, що відповідає 6–12 випадкам ВТЕ на 10 000 жінок, що застосовують пластир Евра®, на рік.
Кількість випадків ВТЕ на рік при застосуванні КГК є нижчою, ніж кількість випадків ВТЕ, що розвивається у жінок під час вагітності або у післяпологовий період.
ВТЕ може мати летальний наслідок у 1–2% випадків.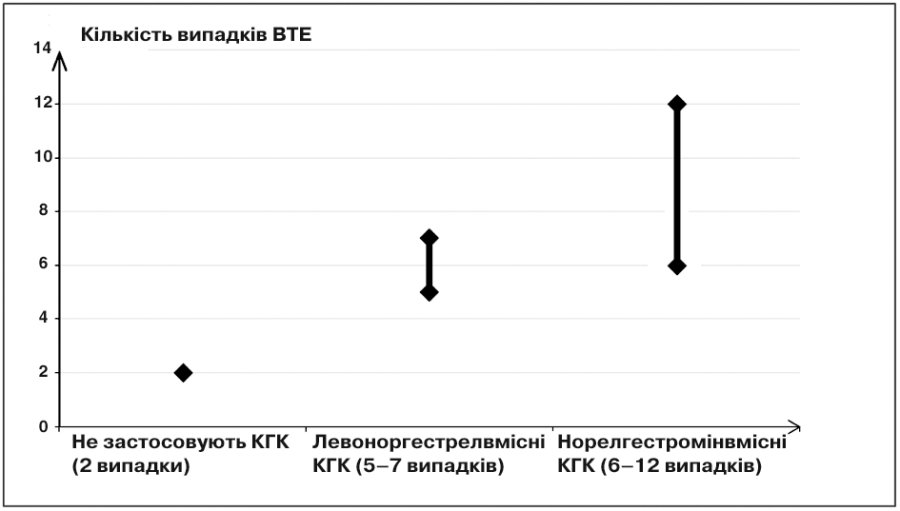
Рис. 1. Кількість випадків ВТЕ на 10 000 жінок за 1 рік.
Дуже рідко повідомлялося про випадки тромбозу інших кровоносних судин, наприклад печінкової, брижової, ниркової вен або вен/артерій сітківки, серед жінок, які застосовували КГК.
Фактори ризику ВТЕ. Ризик розвитку венозних тромбоемболічних ускладнень у жінок, що застосовують КГК, значно підвищується при наявності додаткових факторів ризику, особливо множинних (табл. 2).
Застосування пластиру Евра® протипоказане жінкам, які мають множинні фактори ризику розвитку венозного тромбозу (див. ПРОТИПОКАЗАННЯ). Якщо жінка має більше ніж один фактор ризику, не виключено, що загальний ризик є більшим, ніж сума окремих факторів — у цьому випадку слід зважити загальний ризик ВТЕ у жінки. Якщо співвідношення ризику та користі вважається негативним, КГК не слід призначати (див. ПРОТИПОКАЗАННЯ).
Таблиця 2
Фактори ризику ВТЕ
| Фактор ризику | Коментар |
| Надмірна маса тіла (індекс маси тіла більше 30 кг/м2) | Ризик значно підвищується при збільшенні індексу маси тіла. Особливо важливо враховувати наявність інших факторів ризику |
| Довготривала іммобілізація, обширні оперативні втручання, операції на нижніх кінцівках або тазу, нейрохірургія, серйозні травми Примітка: тимчасова іммобілізація, включаючи авіа перельоти тривалістю >4 год, також може бути фактором ризику ВТЕ, особливо у жінок з іншими факторами ризику | У таких випадках рекомендується припинити застосування пластиру (у випадку планової операції — щонайменше за 4 тиж до втручання) та не продовжувати поки не мине 2 тиж з моменту повного відновлення рухів. Слід використовувати інший метод контрацепції для попередження небажаної вагітності. Слід розглянути необхідність застосування антикоагулянтів якщо застосування пластиру Евра® не було припинене завчасно |
| Обтяжений сімейний анамнез (наприклад, ВТЕ у брата/сестри або батьків у відносно молодому віці) | При підозрі на спадкову схильність жінка повинна звернутися за порадою до спеціаліста перед прийняттям рішення щодо застосування КГК |
| Інші медичні стани, асоційовані з ВТЕ | Злоякісна пухлина, системний червоний вовчак, гемолітичний уремічний синдром, хронічні запальні захворювання кишечнику (наприклад, хвороба Крона або виразковий коліт), серповидноклітинна анемія |
| Збільшення віку | Особливо понад 35 років |
Не існує загальноприйнятої думки щодо можливої ролі варикозу вен та поширеного тромбофлебіту в етіології ВТЕ.
Слід брати до уваги підвищений ризик тромбоемболії під час вагітності, і особливо протягом 6-тижневого періоду після пологів (для додаткової інформації див. Застосування у період вагітності або годування грудьми).
Симптоми ВТЕ (ТГВ та емболія легень).
Жінки, які застосовують комбіновані контрацептиви, повинні негайно повідомити лікаря про появу симптомів тромбозу.
Симптоми ТГВ включають:
- односторонній набряк ноги та/або стопи або набряк уздовж вени на нозі;
- біль або болісні відчуття в нозі, які відчуваються тільки при стоянні і ходьбі;
- підвищену температуру ураженої ноги, почервоніння або блідість шкіри ноги.
Симптоми емболії легень (ЕЛ) включають:
- раптове порушення дихання або прискорене дихання;
- раптовий кашель, який може супроводжуватися кровохарканням;
- різкий біль у грудях;
- переднепритомний стан або запаморочення;
- швидке або нерегулярне серцебиття.
Деякі з цих симптомів є неспецифічними (наприклад, порушення дихання, кашель) і можуть бути прийняті за ознаки іншого більш поширеного і менш тяжкого стану (наприклад, інфекції дихальних шляхів).
Інші ознаки оклюзії судин включають: раптовий біль, набряк і незначне посиніння кінцівки.
Якщо оклюзія відбувається у судинах ока, симптоми можуть варіювати від безболісного погіршення зору до його втрати. Іноді втрата зору відбувається майже моментально.
Ризик АТЕ. Епідеміологічні дослідження пов’язують використання КГК з підвищеним ризиком АТЕ (інфаркт міокарда) або порушенням мозкового кровообігу (наприклад, транзиторна ішемічна атака, інсульт). АТЕ може мати летальний наслідок.
Фактори ризику АТЕ.Ризик артеріальних тромбоемболічних ускладнень або порушення мозкового кровообігу у пацієнтів, які застосовують КГК, збільшується у жінок з факторами ризику (табл. 2). Застосування пластиру Евра® протипоказане жінкам, які мають серйозні або множинні фактори ризику розвитку АТЕ (див. ПРОТИПОКАЗАННЯ). Якщо жінка має більше ніж один фактор ризику, не виключено, що загальний ризик є більшим, ніж сума окремих факторів — у цьому випадку слід зважити загальний ризик АТЕ у жінки. Якщо співвідношення ризику та користі вважається негативним, КГК не слід призначати (див. ПРОТИПОКАЗАННЯ).
Таблиця 3
Фактори ризику АТЕ
| Фактор ризику | Коментар |
| Збільшення віку | Особливо понад 35 років. |
| Паління | Жінкам настійно рекомендується не палити, якщо вони хочуть застосовувати КГК. Жінкам віком від 35 років, які продовжують палити, рекомендовано застосовувати інші методи контрацепції |
| АГ | |
| Надмірна маса тіла (індекс маси тіла більше 30 кг/м2) | Ризик значно підвищується при збільшенні індексу маси тіла. Особливо важливо враховувати наявність інших факторів ризику |
| Обтяжений сімейний анамнез (наприклад, АТЕ у брата або у батьків у відносно молодому віці, тобто менше 50 років) | При підозрі на спадкову схильність жінка повинна звернутися за порадою до спеціаліста перед прийняттям рішення щодо застосування гормональних контрацептивів |
| Мігрень | Збільшення частоти або тяжкості випадків мігрені під час застосування КГК (що може бути продромальним станом порушення мозкового кровообігу) може бути причиною негайного припинення застосування пластиру. |
| Інші медичні стани, асоційовані з небажаними судинними порушеннями | Цукровий діабет, гіпергомоцистеїнемія, захворювання клапанів серця та миготлива аритмія, дисліпопротеїнемія, системний червоний вовчак |
Симптоми АТЕ. Жінки, які застосовують комбіновані контрацептиви, повинні негайно повідомити лікаря при появі симптомів АТЕ.
Симптоми порушення мозкового кровообігу включають:
- раптова слабкість або оніміння обличчя, руки або ноги, особливо на одній стороні тіла;
- раптове утруднення ходьби, запаморочення, втрата рівноваги або координації;
- раптова сплутаність свідомості, проблеми з мовою або розумінням;
- раптові проблеми із зором одного або обох очей;
- раптовий, сильний або тривалий головний біль без певної причини;
- втрата свідомості або непритомність з конвульсіями або без.
Тимчасові симптоми дозволяють підозрювати транзиторну ішемічну атаку.
Симптоми інфаркту міокарда включають:
- біль, дискомфорт, тиск, тяжкість, відчуття здавлювання або розпирання в грудях, руці, або нижче грудини;
- дискомфорт з іррадіацією в спину, щелепу, горло, руки, живіт;
- відчуття переповнення шлунку, розладу шлунка або задуха;
- пітливість, нудота, блювання і запаморочення;
- сильна слабкість, занепокоєння або задишка;
- швидке або нерегулярне серцебиття.
Жінки, які застосовують комбіновані контрацептиви, повинні негайно повідомити лікаря про можливі симптоми тромбозу. У випадку підозрюваного або підтвердженого тромбозу прийом гормональних контрацептивів необхідно припинити. Адекватну контрацепцію потрібно розпочати через тератогенність антикоагулянтної терапії (кумарини).
Пухлини. У ході деяких епідеміологічних досліджень повідомлялося про підвищений ризик розвитку раку шийки матки при довготривалому застосуванні КПК, але досі не встановлено, наскільки це відкриття залежить від поєднання впливу статевої поведінки та інших факторів, таких як вірус папіломи людини (ВПЛ).
Метааналіз 54 епідеміологічних досліджень показав, що існує дещо підвищений ризик (відносний ризик 1,24) виникнення раку грудей у жінок, які приймають КПК. Ризик поступово зменшується протягом 10 років після припинення застосування КПК. Оскільки рак грудей є рідкісним серед жінок віком до 40 років, кількість діагнозів раку грудей у осіб, які застосовували або застосовують КПК, є малою порівняно із загальним ризиком раку грудей. Рак молочної залози, діагностований у постійних користувачів КПК, як правило, менш клінічно поширений, ніж у жінок, які ніколи не приймали контрацептиви.
Підвищений ризик може бути пов’язаний з ранньою діагностикою раку грудей серед пацієнтів, які застосовують КПК, біологічними ефектами КПК або з комбінацією обох причин.
Рідко повідомлялося про доброякісні пухлини печінки та ще рідше про злоякісні пухлини печінки серед пацієнтів, які застосовували КПК. В окремих випадках ці пухлини призвели до внутрішньочеревних кровотеч, що загрожували життю.
Таким чином, слід проводити диференціальну діагностику з печінковою пухлиною при скаргах на гострий біль у животі, збільшенні печінки та ознаках внутрішньочеревної кровотечі у жінок, які застосовували лікарський засіб Евра®.
Підвищення рівня АлАТ. У ході клінічних досліджень за участю пацієнтів, які отримували лікування інфекції вірусу гепатиту С лікарськими засобами, що містять омбітасвір/паритапревір/ритонавір та дасабувір, з рибавірином або без, підвищення рівня трансаміназ (АлАТ) у 5 разів від верхньої межі норми виникало значно частіше у жінок, які використовували лікарські засоби, що містять етинілестрадіол, наприклад КГК (див. ПРОТИПОКАЗАННЯ та ВЗАЄМОДІЯ З ІНШИМИ ЛІКАРСЬКИМИ ЗАСОБАМИ).
Розлади з боку психіки. Відомими побічними ефектами застосування гормональних контрацептивів є пригнічення настрою та депресія (див. ПОБІЧНА ДІЯ). Депресія може бути тяжкою і є добре відомим фактором ризику суїцидальної поведінки та суїциду. Жінок слід проінструктувати про необхідність звернутися до лікаря у разі виникнення змін настрою та симптомів депресії, включно з такими, що виникли невдовзі після початку застосування КПК.
Інші стани. Контрацептивна ефективність може бути знижена у жінок, маса тіла яких становить або перевищує 90 кг (див. ЗАСТОСУВАННЯ).
Жінки з гіпертригліцеридемією або з такими випадками у сімейному анамнезі мають підвищений ризик розвитку панкреатиту при застосуванні КГК.
Хоча незначне підвищення АТ спостерігалося у багатьох жінок, які приймали гормональні контрацептиви, клінічно суттєве підвищення спостерігалося рідко. Зв’язок між застосуванням гормональних контрацептивів та клінічною АГ не був встановлений. Якщо під час застосування КГК на тлі існуючої АГ спостерігається постійне або значне підвищення АТ, яке не відповідає на антигіпертензивне лікування, застосування КГК потрібно припинити. КГК можна знову застосовувати, якщо антигіпертензивна терапія забезпечує контроль нормального рівня АТ.
Такі стани з’являлися або погіршувалися або у період вагітності, або при застосуванні КПК, але докази зв’язку з застосуванням КПК непереконливі: жовтяниця та/або свербіж, пов’язаний з холестазом; захворювання жовчного міхура, включаючи холецистит і жовчнокам’яну хворобу; порфірія; системний червоний вовчак; гемолітичний уремічний синдром; хорея Сиденхама; герпес вагітних; втрата слуху, пов’язана з отосклерозом.
Гострі та хронічні порушення печінкової функції можуть потребувати припинення комбінованої гормональної контрацепції до моменту, коли печінкові маркери повернуться до норми. Рецидив свербежу, пов’язаного з холестазом, що виник у період попередньої вагітності або попереднього застосування статевих стероїдів, потребує припинення прийому КГК.
Незважаючи на те, що КГК можуть вплинути на периферичну інсулінорезистентність та переносимість глюкози, немає доказів необхідності зміни терапевтичного режиму при цукровому діабеті у період застосування гормональних контрацептивів. Однак жінки, хворі на цукровий діабет, повинні постійно перебувати під контролем лікарів, особливо на ранніх стадіях застосування лікарського засобу Евра®.
Під час застосування КПК повідомлялося про ускладнення ендогенної депресії, епілепсії, хвороби Крона або виразкового коліту.
Екзогенні естрогени можуть індукувати або посилювати симптоми спадкового та набутого ангіоневротичного набряку.
Хлоазма може виникнути при застосуванні гормональних контрацептивів, особливо у жінок з хлоазмою вагітних в анамнезі. Пацієнти зі схильністю до хлоазми повинні уникати сонця або УФ опромінення при застосуванні Евра®. Хлоазма часто є необоротною.
Медичний огляд/консультація. Перед початком або поновленням прийому Евра® необхідно розглянути повну історію хвороби (включаючи сімейний анамнез) та виключити вагітність. Потрібно виміряти АТ та провести фізичний огляд для встановлення наявності протипоказань (див. ПРОТИПОКАЗАННЯ) та попереджень (див. ОСОБЛИВОСТІ ЗАСТОСУВАННЯ). Важливо звернути увагу жінки на інформацію щодо венозного та артеріального тромбозу, у тому числі щодо ризику застосування пластиру Евра® у порівнянні з іншими КГК, симптоми ВТЕ і АТЕ, відомі фактори ризику та поведінки у разі підозри на тромбоз.
Жінка має бути проінструктована уважно ознайомитися з інструкцією до медичного застосування лікарського засобу та дотримуватись наданих рекомендацій. Частота та обсяг наступних медичних оглядів мають бути встановлені відповідно до існуючої клінічної практики та клінічного стану жінки.
Жінці потрібно повідомити про те, що гормональні контрацептиви не захищають від ВІЛ-інфекції (СНІД) та інших хвороб, що передаються статевим шляхом.
Порушення режиму кровотеч. Як і при застосуванні інших КГК, упродовж перших місяців застосування можуть спостерігатися нерегулярні кровотечі (мажучі виділення або проривні кровотечі). Тому консультація спеціаліста може бути корисною лише після періоду звикання тривалістю приблизно 3 цикли. Якщо проривні кровотечі зберігаються постійно або виникають після регулярної кровотечі у попередніх циклах при застосуванні лікарського засобу Евра® відповідно до рекомендацій, потрібно розглянути існування іншої причини. Слід звернути увагу на негормональні причини та, при необхідності, вжити діагностичних заходів для виключення органічного захворювання чи вагітності. Ці заходи можуть включати вискоблювання. У деяких жінок менструація може не виникнути у період, вільний від застосування пластиру. Якщо лікарський засіб Евра® застосовували відповідно до рекомендацій розділу ЗАСТОСУВАННЯ, малоймовірно, що жінка вагітна. Вагітність не можна виключити, якщо пластир Евра® застосовували не у відповідності до інструкції перед першою або другою пропущеними менструаціями.
У деяких жінок може бути аменорея або олігоменорея після переривання гормональної контрацепції, особливо при наявності цих станів у анамнезі.
Застосування у період вагітності або годування грудьми
Вагітність. Пластир Евра® не показаний для застосування у період вагітності.
Епідеміологічні дослідження продемонстрували відсутність збільшеного ризику вроджених дефектів у дітей, народжених жінками, які застосовували гормональні контрацептиви перед вагітністю. Більшість нещодавних досліджень також не показали тератогенних ефектів при ненавмисному застосуванні пероральних гормональних контрацептивів на початку вагітності.
Обмежені дані щодо застосування препарату Евра® вагітним жінкам не дають можливості зробити висновок щодо безпеки цього засобу протягом вагітності.
У ході досліджень на тваринах були випадки побічних реакцій у період вагітності або годування грудьми. Тому не слід виключати ризик виникнення побічних реакцій внаслідок гормонального порушення при застосуванні лікарського засобу Евра®, хоча загальний досвід застосування КПК у період вагітності не показав жодних ознак небажаних ефектів у людини.
Якщо вагітність виникла протягом застосування пластиру Евра®, його застосування слід негайно припинити.
Слід враховувати підвищений ризик розвитку ВТЕ у післяпологовому періоді при прийнятті рішення щодо відновлення застосування пластиру Евра® (див. ЗАСТОСУВАННЯ, ОСОБЛИВОСТІ ЗАСТОСУВАННЯ).
Годування грудьми. Також застосування КГК у післяпологовому періоді може негативно вплинути на кількість та якість грудного молока. Матерям, які годують грудьми, не слід застосовувати пластир (ТТС) Евра® до завершення періоду годування грудьми.
Фертильність. Після припинення застосування препарату Евра® може спостерігатися затримка запліднення.
Здатність впливати на швидкість реакції при керуванні транспортними засобами або іншими механізмами. Пластир (ТТС) Евра® не впливає або незначно впливає на швидкicть реакції при керуванні транспортними засобами або роботі з іншими механізмами.
Взаємодія з іншими лікарськими засобами
слід ознайомитися з інструкцією для медичного застосування супутнього лікарського засобу для визначення можливих взаємодій.
Фармакодинамічні взаємодії. ОПід час клінічних досліджень за участю пацієнтів, які отримували лікарські засоби для лікування інфекцій вірусного гепатиту С (HCV), що містять омбітасвір/паритапревір/ритонавір і дасабувір з рибавірином або без нього, було виявлено підвищення трансамінази (АлАТ) більше ніж у 5 разів вище верхньої межі норми (ВМН). Це відбувалося зі значно більшою частотою у жінок, які застосовували лікарські засоби, що містять етинілестрадіол, зокрема і комбіновані гормональні контрацептиви (КГК). Крім того, також у разі лікування глекапревіром/пібрентасвіром або софосбувіром/велпатасвіром/воксилапревіром спостерігалося підвищення АлАТ у жінок, які приймали лікарські засоби, що містять етинілестрадіол, такі як КГК (див. ПРОТИПОКАЗАННЯ). Тому жінки, які використовують Евра®, повинні почати застосовувати альтернативні методи контрацепції (наприклад, контрацептиви, що містять тільки прогестагени або негормональні методи контрацепції), до того як розпочати лікування за цією схемою. Застосування Евра® можна розпочати знову через 2 тижні після завершення лікування за цією комбінованою схемою.
Вплив інших лікарських засобів на Евра®. Можуть спостерігатися взаємодії з лікарськими засобами, які посилюють дію печінкових ензимів, що призводить до збільшення кліренсу статевих гормонів, що, в свою чергу, може призвести до проривної кровотечі та/або втрати контрацептивного ефекту. Були описані нижчезазначені взаємодії.
Лікарські засоби, що збільшують кліренс КГК (знижена ефективність КГК, спричинена індукцією ферментів): барбітурати, бозентан, карбамазепін, фенітоїн, примідон, рифампіцин, модафініл, ВІЛ-препарати ритонавір, невірапін, ефавіренц та, можливо, фелбамат, гризеофульвін, окскарбазепін, топірамат і продукти, що містять екстракт звіробою (Hypericum perforatum).
Управління ризиками. Підвищення рівня ферментів може спостерігатися через декілька днів після початку лікування. Максимальна активація ферментів загалом проявлялася протягом 10 днів та потім трималася протягом 4 тиж після припинення терапії.
Короткострокове лікування. Жінки, які проходять короткострокове лікування будь-якими із зазначених класів лікарських засобів або окремих активних речовин, що індукують печінкові ферменти, повинні тимчасово використовувати бар’єрний метод захисту додатково до Евра® протягом одночасного застосування лікарського засобу та 28 днів після його припинення.
Якщо одночасний прийом лікарського препарату продовжується після закінчення одного тижня застосування пластиру, наступний трансдермальний пластир потрібно приклеїти без звичайної перерви у його застосуванні.
Довгострокове лікування. Жінкам, які проходять довгострокове лікування будь-якими із зазначених класів лікарських засобів, рекомендується застосовувати інший надійний негормональний спосіб контрацепції.
Лікарські засоби, що впливають на кліренс КГК. При одночасному застосуванні з КГК різноманітні комбінації інгібіторів протеази ВІЛ та ненуклеозидних інгібіторів зворотної транскриптази, включаючи комбінації препаратів для лікування інфекції вірусу гепатиту С, можуть підвищувати або знижувати концентрацію естрогену та прогестинів у плазмі крові. У деяких випадках результат таких змін концентрації може бути клінічно важливим.
Тому перед одночасним застосуванням слід ознайомитися з інструкціями для медичного застосування лікарських засобів для лікування ВІЛ-інфекції в частині можливих взаємодій та пов’язаних з ними рекомендацій щодо застосування. При виникненні сумнівів жінкам, які застосовують інгібітори протеази або ненуклеозидні інгібітори зворотної транскриптази, слід застосовувати додатковий бар’єрний метод контрацепції.
Пригнічення метаболізму етинілестрадіолу. Еторикоксиб проявив підвищення рівня етинілестрадіолу у плазмі крові (на 50–60%) при одночасному прийомі з пероральними трифазними гормональними контрацептивами. Вважається, що еторикоксиб підвищує рівні етинілестрадіолу за рахунок пригнічення активності сульфотрансферази, таким чином пригнічуючи метаболізм етинілестрадіолу.
Вплив Евра® на інші лікарські засоби. Гормональні контрацептиви можуть впливати на метаболізм деяких інших активних речовин. Відповідно, концентрації у плазмі крові та тканинах можуть підвищитися (наприклад, циклоспорину). Може виникнути необхідність у регулюванні дозування супутнього лікарського засобу.
Ламотриджин: КГК значно знижують концентрації ламотриджину у плазмі крові при одночасному застосуванні за рахунок індукції глюкуронідації ламотриджину. Це може знижувати терапевтичний ефект; може знадобитися корекція дози ламотриджину.
Лабораторні показники. Застосування гормональних контрацептивів може вплинути на результати деяких лабораторних аналізів, включаючи біохімічні показники печінки, щитовидної залози, надниркових залоз та нирок, рівень білків (переносників) у плазмі крові, наприклад кортикостероїдзв’язуючого глобуліну та фракції жирів/ліпопротеїдів, параметри метаболізму вуглеводів та параметри коагуляції та фібринолізу. Зміни загалом залишаються у межах лабораторних норм.
Передозування
при випадковому застосуванні високих доз пероральних контрацептивів не повідомлялося про серйозні побічні реакції. Передозування може спричиняти нудоту або блювання. У деяких жінок можуть виникати піхвові кровотечі. При підозрі на передозування необхідно зняти пластир (ТТС) Евра® та провести симптоматичну терапію.
Умови зберігання
в оригінальній упаковці при температурі не вище 30 °С у недоступному для дітей місці. Не зберігати у холодильнику або морозильній камері.
