Ферсінол (Fersinol)
Ферсінол інструкція із застосування
Склад
Допоміжна речовина: вода для ін’єкцій.
Гідроксиду заліза (III) полімальтозний комплекс - 100 мг
Фармакологічні властивості
фармакодинаміка. Після в/м введення майже все залізо з полімальтозного комплексу гідроксиду заліза (III) у вигляді активного інгредієнта надходить у ретикуло-ендотеліальну систему печінки, а також захоплюється трансферином, апоферитином, селезінкою і кістковим мозком. Там воно сполучається з гемоглобіном, міоглобіном і залізовмісними ферментами, а також зберігається в організмі у вигляді феритину. Зміни показників крові при парентеральному введенні заліза відбуваються не швидше, ніж при пероральному прийомі солей заліза. Як і інші препарати заліза, препарат не впливає на еритропоез і неефективний при анеміях, не пов’язаних із дефіцитом заліза.
Фармакокінетика. Після в/м введення комплекс потрапляє до кровотоку. Cmax заліза досягається приблизно через 24 год після ін’єкції. У крові залізо зв’язується із трансферином. З плазми крові макромолекулярний комплекс потрапляє в ретикуло-ендотеліальну систему, де розщеплюється на гідроксид заліза й полімальтозу. У тканинах зберігається у складі феритину, у кістковому мозку сполучається з гемоглобіном і використовується в процесі еритропоезу.
Виводиться з організму лише невелика кількість заліза. Полімальтоза метаболізується шляхом окиснення та виводиться.
У невеликій кількості незмінений комплекс може проходити через плацентарний бар’єр і незначна його кількість проникає у грудне молоко. Залізо, зв’язане з феритином чи трансферином, може проходити через плацентарний бар’єр, а у складі лактоферину виділяється у грудне молоко в невеликій кількості.
Включення заліза у протопорфірин залежить від ступеня залізодефіцитної анемії. Воно інтенсивніше в разі низького рівня гемоглобіну і зменшується відповідно до нормалізації рівня гемоглобіну.
Ступінь утилізації заліза не може бути вищим, ніж залізозв’язувальна здатність транспортних білків.
Показання Ферсінол
лікування залізодефіцитної анемії у таких випадках:
– у разі протипоказання до проведення пероральної терапії;
– у разі порушення всмоктування заліза в кишечнику;
– у разі недотримання пацієнтом режиму лікування пероральними препаратами заліза або їх стійка шлунково-кишкова непереносимість.
Застосування Ферсінол
препарат призначений для глибокого в/м введення. В/в введення протипоказане.
Спосіб застосування. Перед ін’єкцією ампули та їх вміст слід уважно оглянути. До використання прийнятні лише ампули, що не містять осаду та не мають пошкоджень. Вводити лікарський засіб слід відразу після розкриття ампули.
Техніка ін’єкції має важливе значення. Р-н заборонено вводити в плече або в пошкоджені зони. У разі неправильного введення можуть виникнути болісність і забарвлення шкіри в місці ін’єкції.
Препарат рекомендується вводити у вентроглютеальну ділянку за Хохштеттером замість звичайного введення у верхній зовнішній квадрант сідничного м’яза.
Довжина голки повинна бути не менше 5–6 см. Просвіт голки не повинен бути надто широким.
Техніка ін’єкції. Визначити місце ін’єкції таким чином (рис. 1): знайти точку А, що відповідає передній поверхні гребеня клубової кістки. Наприклад, якщо хворий лежить на правому боці, середній палець лівої руки слід розмістити в точці А. Вказівний палець відставити від середнього таким чином, щоб він містився під лінією клубового гребеня в точці В. 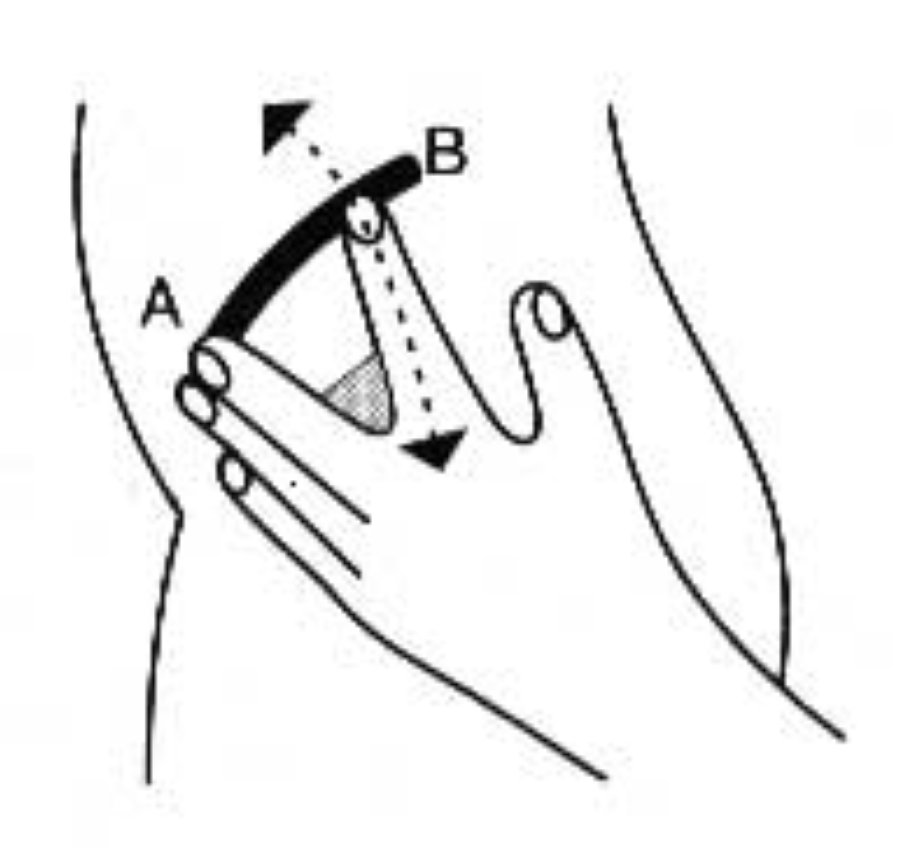
Рис. 1.
Трикутник, розташований між проксимальними фалангами середнього і вказівного пальців, є місцем ін’єкції (рис. 2). Дезінфекція проводиться звичайним методом.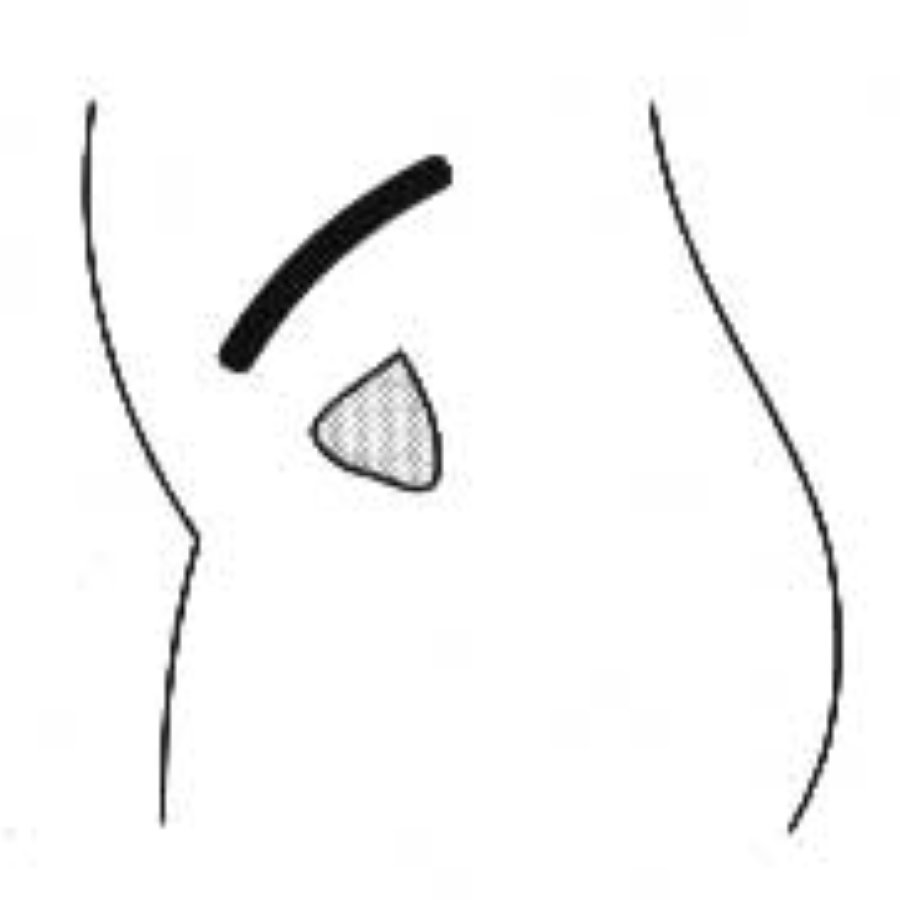
Рис. 2.
Перш ніж ввести голку, відтягнути шкіру від місця ін’єкції приблизно на 2 см (рис. 3) для того, щоб надати каналу проколу S-подібної форми. Це запобігає зворотному витіканню введеного р-ну в підшкірні тканини і забарвленню шкіри.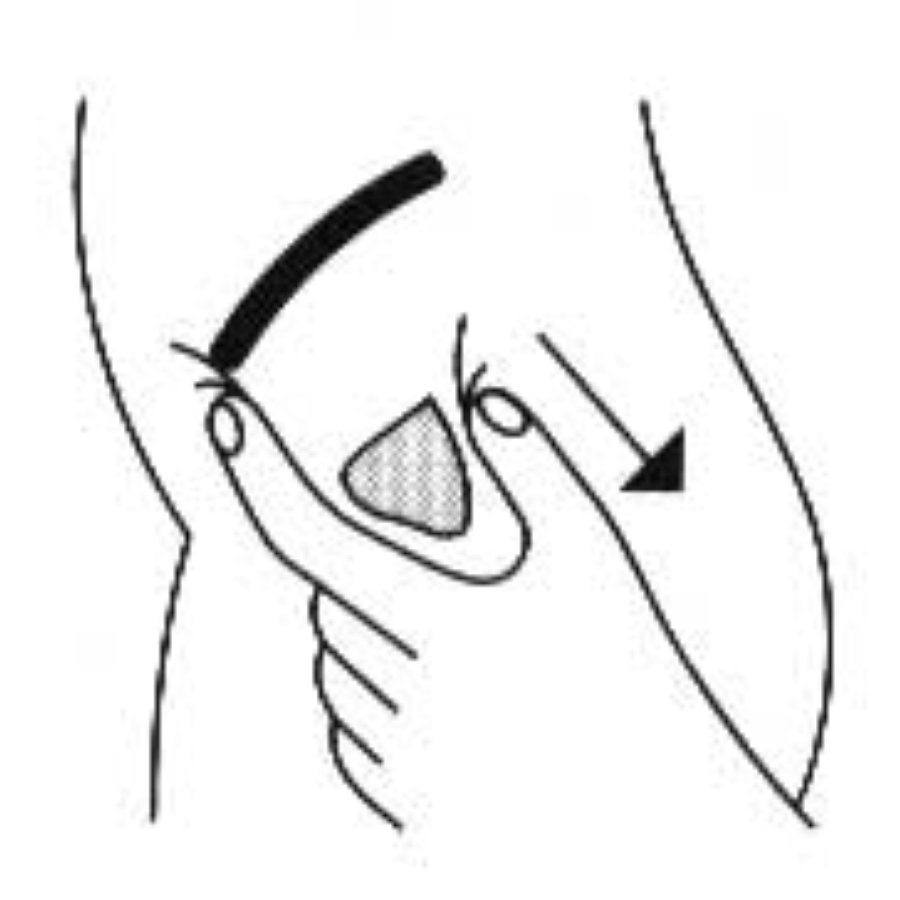
Рис. 3.
Ввести голку майже вертикально відносно поверхні шкіри під кутом, більшим до точки клубового зчленування, ніж до точки стегнового суглоба (рис. 4).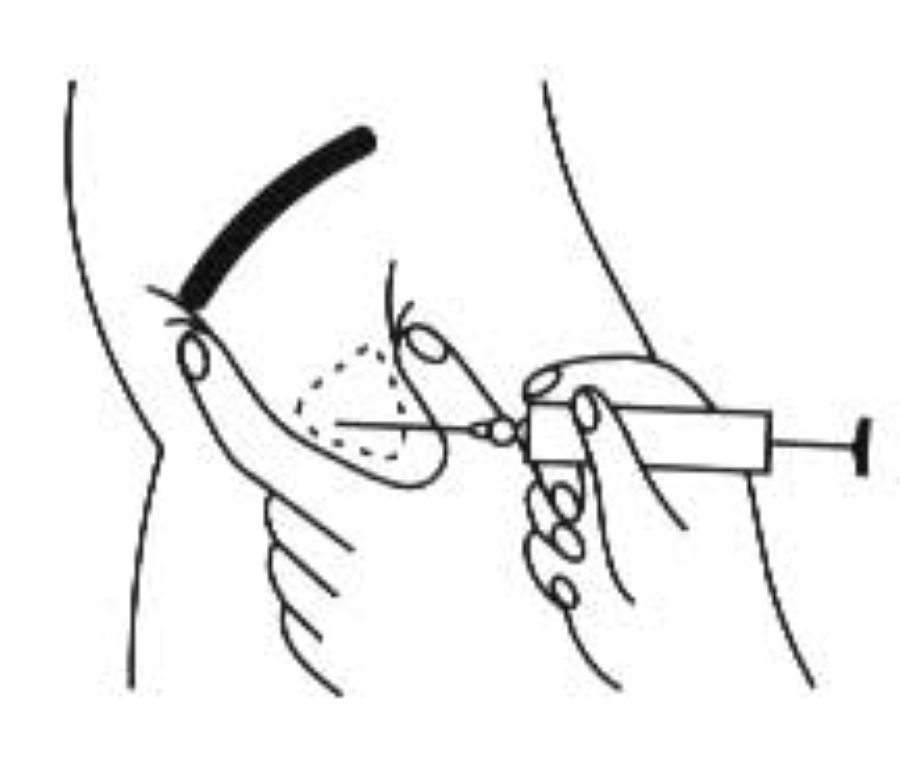
Рис. 4.
Після ін’єкції повільно вийняти голку і притиснути пальцем ділянку шкіри, що прилягає до місця ін’єкції. Потримати близько 1 хв.
Після ін’єкції пацієнту слід порухатися.
Дозування
Розрахунок дози. Дозу препарату розраховують індивідуально, відповідно до загального дефіциту заліза за такою формулою:
| Доза заліза (мг) | = | маса тіла (кг) · (нормальний рівень Hb — рівень Hb хворого) (г/л) · 0,24* + залізо запасів (мг) |
*Фактор 0,24 = 0,0034 · 0,07 · 1000 (вміст заліза в гемоглобіні — 0,34%/об’єм крові — 7% маси тіла/фактор 1000 — переведення із грамів у міліграми).
Вищенаведена формула може бути також використана для розрахунку сумарного дефіциту заліза.
При масі тіла <35 кг: нормальний рівень Hb 130 г/л, що відповідає залізу запасів 15 мг/кг маси тіла.
При масі тіла ≥35 кг: нормальний рівень Hb 150 г/л, що відповідає залізу запасів 500 мг.
Таблиця дозувань для визначення необхідного сумарної кількості лікарського засобу
| Маса тіла, кг | Hb 60 г/л | Hb 75 г/л | Hb 90 г/л | Hb 105 г/л | ||||
| мл | ампули | мл | ампули | мл | ампули | мл | ампули | |
| 5 | 3 | 1,5 | 3 | 1,5 | 3 | 1,5 | 2 | 1 |
| 10 | 6 | 3 | 6 | 3 | 5 | 2,5 | 4 | 2 |
| 15 | 10 | 5 | 9 | 4,5 | 7 | 3,5 | 6 | 3 |
| 20 | 13 | 6,5 | 11 | 5,5 | 10 | 5 | 8 | 4 |
| 25 | 16 | 8 | 14 | 7 | 12 | 6 | 11 | 5,5 |
| 30 | 19 | 9,5 | 17 | 8,5 | 15 | 7,5 | 13 | 6,5 |
| 35 | 25 | 12,5 | 23 | 11,5 | 20 | 10 | 18 | 9 |
| 40 | 27 | 13,5 | 24 | 12 | 22 | 11 | 19 | 9,5 |
| 45 | 30 | 15 | 26 | 13 | 23 | 11,5 | 20 | 10 |
| 50 | 32 | 16 | 28 | 14 | 24 | 12 | 21 | 10,5 |
| 55 | 34 | 17 | 30 | 15 | 26 | 13 | 22 | 11 |
| 60 | 36 | 18 | 32 | 16 | 27 | 13,5 | 23 | 11,5 |
| 65 | 38 | 19 | 33 | 16,5 | 29 | 14,5 | 24 | 12 |
| 70 | 40 | 20 | 35 | 17,5 | 30 | 15 | 25 | 12,5 |
| 75 | 42 | 21 | 37 | 18,5 | 32 | 16 | 26 | 13 |
| 80 | 45 | 22,5 | 39 | 19,5 | 33 | 16,5 | 27 | 13,5 |
| 85 | 47 | 23,5 | 41 | 20,5 | 34 | 17 | 28 | 14 |
| 90 | 49 | 24,5 | 43 | 21,5 | 36 | 18 | 29 | 14,5 |
Препарат слід вводити в/м у дозі 2 мл через день до отримання сумарної дози або вводити 4 мл через більш тривалі інтервали.
Під час застосування препарату рекомендується проводити регулярне визначення рівня гемоглобіну.
Максимальна добова доза
Діти з масою тіла <5 кг: 0,5 мл = 25 мг заліза (¼ ампули).
Діти з масою тіла 5–10 кг: 1 мл = 50 мг заліза (½ ампули).
Пацієнти з масою тіла 10–45 кг: 2 мл = 100 мг заліза (1 ампула) на добу.
Дорослі з масою тіла ≥45 кг: 4 мл = 200 мг заліза (2 ампули).
Протипоказання
– гіперчутливість до полімальтозного комплексу гідроксиду заліза;
– анемії, не пов’язані з дефіцитом заліза (наприклад гемолітична анемія, мегалобластна анемія, порушення еритропоезу, гіпоплазія кісткового мозку);
– надлишок заліза в організмі (гемосидероз, гемохроматоз);
– синдром Ослера — Рандю — Вебера;
– хронічний поліартрит;
– БА;
– інфекційні захворювання нирок у гострій стадії;
– неконтрольований гіперпаратиреоз;
– некомпенсований цироз печінки;
– інфекційний гепатит;
– I триместр вагітності;
– тяжке запалення або інфекція нирок або печінки (внаслідок здатності елементарного заліза до накопичення в запалених тканинах).
Побічна дія
побічні реакції виникають нечасто. Після застосування парентеральних препаратів заліза можуть виникати нижченаведені побічні реакції.
З боку крові та лімфатичної системи: генералізована лімфаденопатія.
З боку імунної системи: анафілаксія.
З боку травного тракту: нудота, блювання.
З боку нервової системи: головний біль, запаморочення.
З боку дихальної системи, органів грудної клітки та середостіння: бронхоспазм із диспное.
З боку серцево-судинної системи: втрата свідомості, непритомність, тахікардія, артеріальна гіпотензія, циркуляторний колапс.
З боку шкіри та підшкірних тканин: висип, кропив’янка, ангіоневротичний набряк.
З боку скелетно-м’язової системи та сполучної тканини: біль у суглобах та м’язах, артралгія, відчуття скутості в руках, ногах або м’язах обличчя, гіпофосфатемічна остеомаляція.
Загальні розлади і реакції у місці введення: приплив крові до обличчя, біль за грудниною та у спині, біль у місці введення, місцеве запалення з паховою лімфаденопатією, біль у нижньому квадранті живота.
Побічні реакції можуть виникати із затримкою на 1–2-й день після лікування.
Повідомлення про підозрювані побічні реакції, що виникли після реєстрації лікарського засобу, дуже важливі. Це дає змогу постійно спостерігати за співвідношенням користі/ризику при застосуванні лікарського засобу. Працівники системи охорони здоров’я повинні повідомляти про будь-які підозрювані побічні реакції через національну систему фармаконагляду.
Особливості застосування
лікарський засіб слід застосовувати лише при підтвердженому відповідними дослідженнями залізодефіцитному стані (наприклад визначення рівня феритину у плазмі крові, гемоглобіну, гематокриту, кількості еритроцитів, а також їх параметрів — середнього об’єму еритроцита, середньої концентрації гемоглобіну в еритроциті).
Необґрунтоване застосування парентеральних препаратів заліза у пацієнтів, у яких анемія не пов’язана з дефіцитом заліза (наприклад із гемоглобулінопатією), може призводити до надмірного накопичення заліза і розвитку синдрому, подібного до гемосидерозу.
Оскільки парентеральне застосування препаратів заліза призводило до розвитку анафілактоїдних реакцій з летальним наслідком, лікарський засіб слід застосовувати тільки у пацієнтів із чітко встановленим показанням та після підтвердження стану хворого результатами лабораторних аналізів. У разі виникнення слабкої алергічної реакції слід застосовувати антигістамінні засоби.
При парентеральному застосуванні препаратів заліза існує ризик виникнення реакцій гіперчутливості та анафілактоїдних реакцій при введенні кожної дози. Анафілактоїдні реакції найчастіше виникають у перші кілька хвилин після введення та зазвичай характеризуються раптовим утрудненням дихання, розвитком тахікардії та артеріальної гіпотензії. Застосування пробної дози не потрібне, оскільки відсутність такої реакції при застосуванні пробної дози не означає відсутність реакції при наступних дозах.
Лікарський засіб можна вводити лише за умови, що медичний персонал, який має навички оцінювання та лікування анафілактичних реакцій, готовий до негайних дій, та за наявності приміщення, належним чином обладнаного засобами для проведення реанімаційних заходів. Кожного пацієнта слід обстежити щодо проявів побічних реакцій щонайменше через 30 хв після кожного в/в введення залізовмісних препаратів. При виникненні будь-яких алергічних реакцій або ознак непереносимості під час введення лікарського засобу лікування слід негайно припинити.
Пацієнти з БА, низькою здатністю зв’язувати залізо та/або з дефіцитом фолієвої кислоти належать до групи високого ризику розвитку алергічних або анафілактичних реакцій.
Лікарський засіб слід з обережністю застосовувати у пацієнтів з алергією, печінковою і нирковою недостатністю або серцево-судинним захворюванням.
Пацієнти з ревматоїдним артритом та, можливо, іншими запальними захворюваннями (наприклад анкілозивний спондиліт, системний червоний вовчак) можуть мати підвищений ризик розвитку відстрочених реакцій, включаючи жар і загострення або реактивацію болю в суглобах.
У післяреєстраційний період повідомляли про симптоматичну гіпофосфатемію, яка спричиняла остеомаляцію та переломи, що потребувало клінічного втручання, включаючи хірургічне втручання. Пацієнтам слід рекомендувати звертатися до лікаря, якщо виявлені посилення втоми з міалгією або біль у кістках. У разі тривалого застосування лікарського засобу або застосування його у високих дозах, а також за наявності факторів ризику гіпофосфатемії слід здійснювати моніторинг рівня фосфатів у плазмі крові. У разі тривалої гіпофосфатемії необхідно переглянути застосування лікарського засобу.
Застосування у період вагітності чи годування грудьми
Вагітність. Лікарський засіб протипоказаний для застосування протягом І триместру вагітності. Дані досліджень на тваринах або за участю вагітних відсутні. У тварин, які отримували в/в препарати заліза, відзначалася ембріофетальна токсичність.
Протягом ІІ і ІІІ триместрів вагітності лікарський засіб можна застосовувати тільки тоді, коли очікувана користь для матері перевищує потенційний ризик для плода.
Період годування грудьми. Дані досліджень за участю жінок, які годують грудьми, відсутні. Слід враховувати ймовірність потрапляння заліза в грудне молоко. У разі застосування лікарського засобу в період годування грудьми слід враховувати очікувану користь для матері та потенційний ризик для дитини.
Діти. Можна застосовувати у дітей віком від 4 міс.
Здатність впливати на швидкість реакції при керуванні транспортними засобами чи роботі з іншими механізмами. Відповідні дослідження відсутні.
Взаємодія з іншими лікарськими засобами
як і всі інші парентеральні препарати заліза, Ферсінол не слід застосовувати одночасно з пероральними залізовмісними препаратами, оскільки всмоктування останніх у травному тракті знижується. Тому лікування пероральними залізовмісними препаратами варто починати не раніше ніж через 1 тиж після останньої ін’єкції.
Одночасний прийом інгібіторів АПФ (наприклад еналаприлу) може спричинити посилення системних ефектів парентеральних препаратів заліза, наприклад еритеми, спазмів у животі, нудоти, блювання та артеріальної гіпотензії.
Взаємодія з результатами лабораторних тестів. Високі в/в дози препаратів заліза (250 мг заліза або більше) можуть призводити до фарбування в коричневий колір плазми в зразках крові, взятих через 4 год після їх застосування.
Препарати заліза можуть спричиняти хибне підвищення рівня білірубіну в плазмі крові та хибне зниження рівня кальцію в плазмі крові. Визначення рівня плазмового заліза (особливо колориметричним методом) може не бути інформативним протягом 3 тиж після застосування препаратів заліза. Результати вимірювань заліза в плазмі крові, отримані протягом 1–2 тиж після прийому високих доз препаратів заліза, слід інтерпретувати з обережністю.
Вивчення запасів заліза в кістковому мозку може бути неінформативним протягом тривалого часу після лікування, оскільки лікарський засіб може залишатися в ретикулоендотеліальних клітинах.
Сканування кісток скелета з використанням 99mТс дифосфонату, виконане через 1–6 днів після в/м ін’єкції препарату заліза, може показати щільні ділянки активності в стегновій кістці, що повторюють контури гребеня клубової кістки. Сканування кісток скелета з використанням візуалізуючих засобів, мічених 99mТс, за наявності високих концентрацій феритину в плазмі крові або після в/в інфузій препаратів заліза може демонструвати зниження кісткового поглинання, виражену активність нирок, надмірне кровонаповнення та депонування в м’яких тканинах.
Препарати заліза можуть знижувати поглинання 67Ga-цитрату під час візуалізації пухлин та/або абсцесів, що є результатом конкуренції за одні й ті самі місця зв’язування.
Наявність заліза може призводити до отримання хибнопозитивних результатів ортотолуїдинової проби.
Несумісність. Ферсінол, р-н для ін’єкцій, не слід змішувати з іншими препаратами. Лікарський засіб сумісний тільки зі стерильним 0,9% р-ном натрію хлориду. Будь-які інші р-ни не повинні використовуватися.
Передозування
про випадки передозування препарату Ферсінол повідомлень немає.
Передозування може спричинити гостре перевантаження залізом, що проявляється симптомами гемосидерозу. Терапія симптоматична.
Хронічне перевантаження залізом може бути виражене як гемохроматоз. Це можливо, коли анемія, несприйнятлива до лікування, була неправильно діагностована як залізодефіцитна анемія.
Періодичний контроль рівня феритину в сироватці крові може допомогти у своєчасному розпізнаванні прогресуючого навантаження заліза.
За необхідності застосовують речовини, що зв’язують залізо (хелати), наприклад дефероксамін в/в.
При введенні препарату Ферсінол у надто високих дозах комплекс не може бути виведений з організму шляхом гемодіалізу у зв’язку з високою молекулярною масою діючої речовини.
Умови зберігання
при температурі не вище 25 °С у недоступному для дітей місці.
